Содержание
- 2. «Мощь и сила науки – во множестве фактов, цель – в обобщении этого множества» Д.И.Менделеев
- 3. Неметаллы – химические элементы, которые образуют в свободном виде простые вещества, не обладающие физическими свойствами металлов
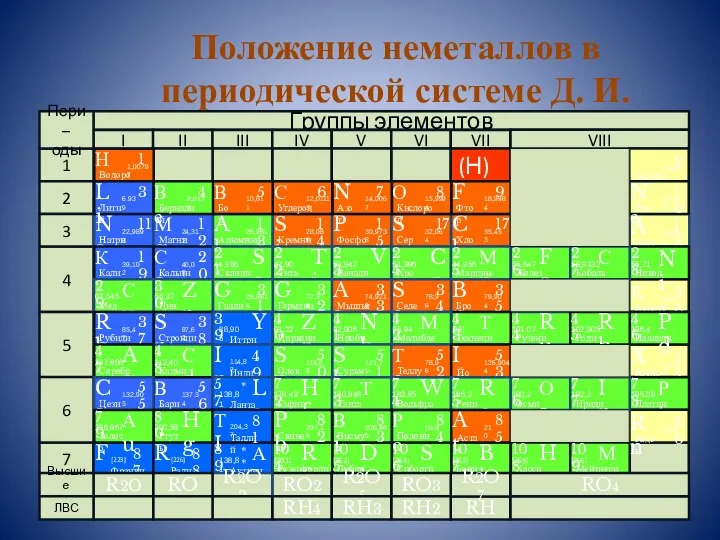
- 4. Положение неметаллов в периодической системе Д. И. Менделеева
- 5. Особенности атомного строения неметаллов Небольшой атомный радиус На внешнем уровне 4-8 электронов Располагаются только в главных
- 6. Химическая связь В простых веществах атомы неметаллов связаны ковалентной неполярной связью. Благодаря этому формируется более устойчивая
- 7. Физические свойства неметаллов Ковкость отсутствует Блеска нет Теплопроводность (только графит) Цвет разнообразный: желтый, желтовато-зеленый, красно-бурый. Электропроводность
- 8. Агрегатное состояние Жидкое (Br 2) Твердое (C) Газообразное (N2)
- 9. Цветовая гамма ЖЕЛТЫЙ (S) Синий (Ne) Серый (Si)
- 10. Температура плавления -210 oC (N2) 3800oC (графит )
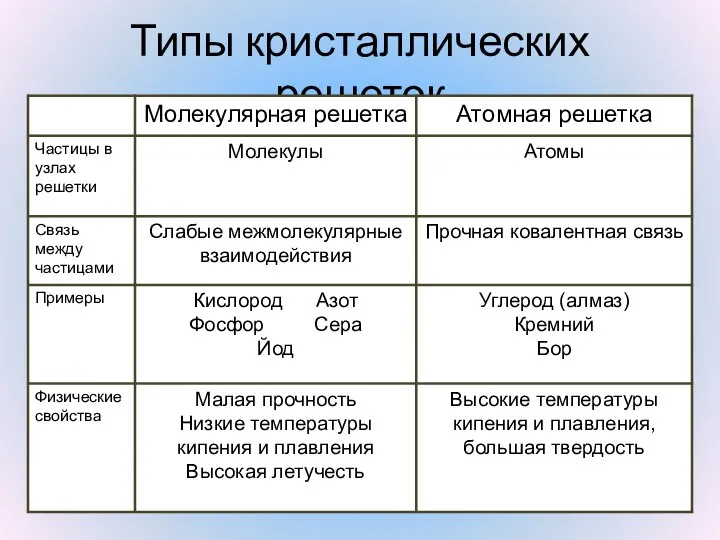
- 11. Типы кристаллических решеток
- 12. Аллотропия Определение: Аллотропия - это существование одного и того же химического элемента в виде нескольких простых
- 13. Аллотропия Разное типы кристаллических решеток Р - фосфор Красный фосфор - атомная Белый фосфор - молекулярная
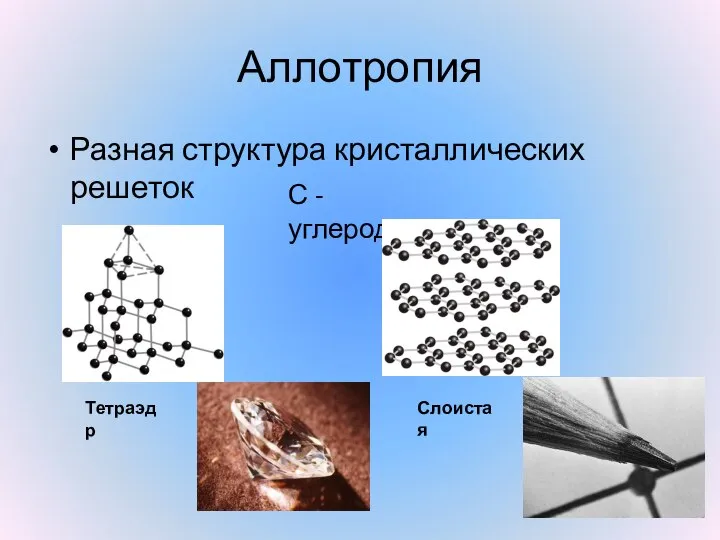
- 14. Аллотропия Разная структура кристаллических решеток С - углерод Тетраэдр Слоистая
- 15. Аллотропия Разный состав молекул О - кислород Кислород Озон
- 16. Озон О3 Светло - синий газ с сильным запахом Имеет запах свежести Появляется после грозы
- 17. Озон в природе Содержится в воздухе сосновых лесов и морского побережья
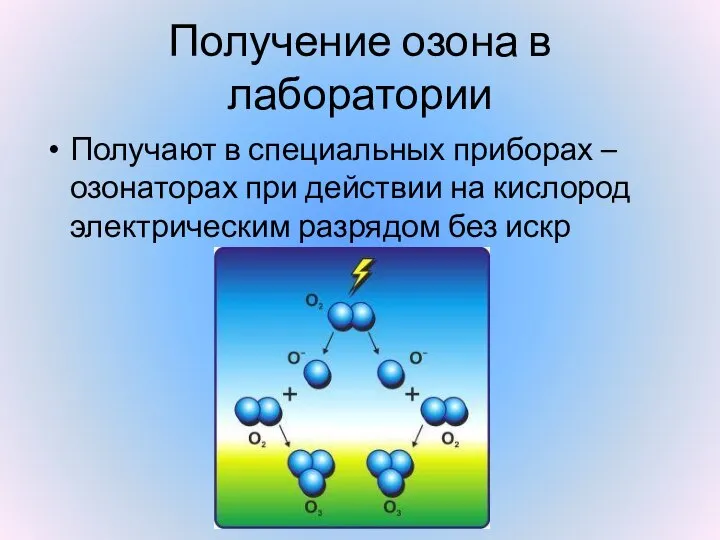
- 18. Получение озона в лаборатории Получают в специальных приборах – озонаторах при действии на кислород электрическим разрядом
- 19. Значение озона для Земли Задерживает ультрафиолетовые лучи, которые разрушительно действуют на клетки живых организмов Озоновый слой
- 20. В конце 18 века А-Л. Лавуазье установил, что воздух – не простое вещество. а смесь газов
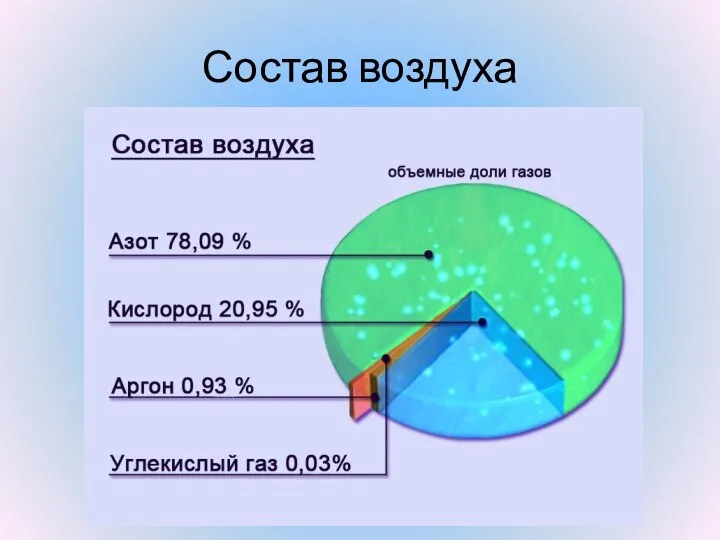
- 21. Состав воздуха
- 22. Постоянные составные воздуха Азот Кислород Благородные газы
- 23. Переменные составные воздуха Углекислый газ Водяные пары Озон
- 24. Случайные составные воздуха Пыль Микроорганизмы Пыльца растений Оксиды серы и азота
- 25. Химические свойства Для атомов неметаллов, а следовательно, и для образованных ими простых веществ характерны как окислительные,
- 26. Окислительные свойства сульфид натрия хлорид железа(III) нитрид магния
- 27. Окислительные свойства сероводород хлороводород аммиак t◦ свет p,t◦, катал.
- 28. Окислительные свойства H, Si, As, P, Se, C, S, I, Br, Cl, N, O, F Усиление
- 29. Окислительные свойства
- 30. Окислительные свойства
- 31. Окислительные свойства свет
- 32. Восстановительные свойства t◦ t◦ несолеобразующий оксид солеобразующий кислотный оксид
- 33. Восстановительные свойства t◦ t◦
- 34. Восстановительные свойства
- 35. Выходной контрольный тест 1. В каком ряду представлены простые вещества-неметаллы: А) хлор, никель, серебро Б) алмаз,
- 36. Выходной контрольный тест 2. Неметаллы встречаются среди А) лантаноидов и актиноидов Б) элементов VII группы В)
- 37. Выходной контрольный тест 3. Полностью из элементов неметаллов состоит главная подгруппа А) седьмой группы Б) шестой
- 38. Выходной контрольный тест 4. С уменьшением порядкового номера в А (главных) подгруппах периодической системы Д.И.Менделеева неметаллические
- 39. Выходной контрольный тест 5. Неметаллические свойства в ряду элементов Si → P → S → Cl
- 40. Выходной контрольный тест 6. Атомы неметаллов обладают следующими характеристиками А) большим радиусом Б) небольшим радиусом В)
- 41. Выходной контрольный тест 7. Неметаллические свойства усиливаются с… А) ростом числа эл-в на внешнем уровне и
- 42. Выходной контрольный тест 8. Укажите вещества, имеющие молекулярную кристаллическую решетку А) кремний Б) кислород В) азот
- 43. Выходной контрольный тест 9. Какие физические свойства являются общими для большинства неметаллов А) блеск Б) ковкость
- 44. Выходной контрольный тест 10. Явление аллотропии не свойственно элементам А) фосфору Б) водороду В) углероду Г)
- 45. Ответы контрольного теста 1. Г 2. БВ 3. АГ 4. Б 5. Б 6. БГ 7.
- 47. Скачать презентацию







































 Алкины. Строение, номенклатура, изометрия, физические свойства
Алкины. Строение, номенклатура, изометрия, физические свойства Электроотрицательность (ЭО)
Электроотрицательность (ЭО) Химическае препараты
Химическае препараты Туф вулканический
Туф вулканический 9_OSNOVY_KOLANALIZA
9_OSNOVY_KOLANALIZA получение Ме презентация
получение Ме презентация Ионообменные материалы для сорбции биологически активных веществ
Ионообменные материалы для сорбции биологически активных веществ Селективная экстракция отдельных групп БАВ сверхкритическими флюидами
Селективная экстракция отдельных групп БАВ сверхкритическими флюидами Обобщение. Неметаллы
Обобщение. Неметаллы Опыты по теме Свойства основных классов неорганических соединений
Опыты по теме Свойства основных классов неорганических соединений Процессы переработки нефти
Процессы переработки нефти Аналитические методы в современных исследованиях химии
Аналитические методы в современных исследованиях химии Расчеты по уравнениям химических реакций
Расчеты по уравнениям химических реакций Химия в нашей жизни
Химия в нашей жизни Соли
Соли Уравнения диссоциации
Уравнения диссоциации Сера. Физические и химические свойства. Нахождение в природе
Сера. Физические и химические свойства. Нахождение в природе Техника безопасности на уроках химии
Техника безопасности на уроках химии История развития технологий термического крекинга в России и мире
История развития технологий термического крекинга в России и мире Пиримидин (шестичленный гетероцикл с двумя атомами азота)
Пиримидин (шестичленный гетероцикл с двумя атомами азота) Вещество и тело. Чистые вещества и смеси
Вещество и тело. Чистые вещества и смеси Минералы
Минералы Газовые смеси. Способы задания газовых смесей. Лекция 5
Газовые смеси. Способы задания газовых смесей. Лекция 5 способы разделения смесей
способы разделения смесей (+)-Plumisclerin A. Плюмисклин А
(+)-Plumisclerin A. Плюмисклин А Растворы полимеров
Растворы полимеров Получение бутандиола, как способ переработки природного газа
Получение бутандиола, как способ переработки природного газа Основной органический синтез
Основной органический синтез