Содержание
- 2. Мы здоровы и полны энергии. У нас все в жизни хорошо. Мы молоды, мы счастливы, мы
- 3. «Их получают путем горения Или сложных веществ разложения. В них два элемента, один – кислород. Я
- 4. «Они имеют кислый вкус. В них изменяет цвет лакмус. А если активный металл попадет, Получим мы
- 5. «В каких веществах у фенолфталеина Бывает не жизнь, а сплошная малина?» Щелочи NaOH, Ca(OH)2
- 6. NO HNO NaOH HNO 2 3 К какому классу соединений относятся вещества (дать им названия)
- 7. CO 2 2 H CO Mg(OH) 2 3 H SO 2 3 H SO 2 4
- 8. О каком веществе идёт речь? Войны за это вещество происходили в разные эпохи: за нее сражались
- 9. «Хлориды и нитраты, Сульфаты, карбонаты Я без труда и боли Объединю в класс...» Соли
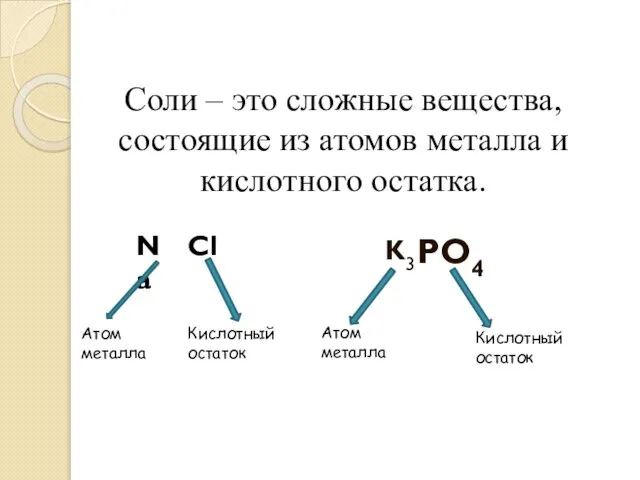
- 10. Соли – это сложные вещества, состоящие из атомов металла и кислотного остатка. PO4 K3
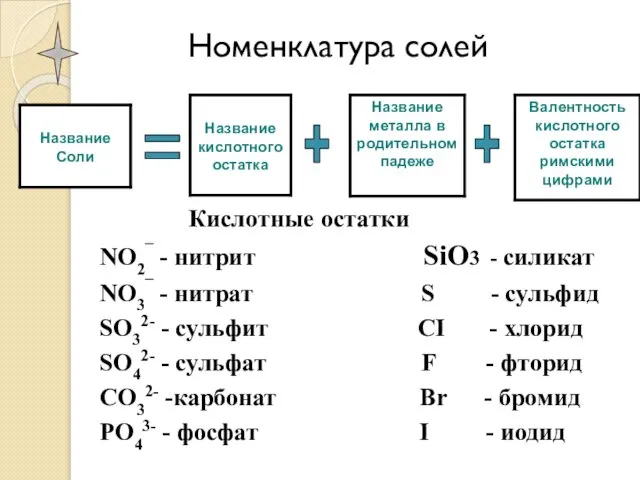
- 11. Номенклатура солей + + =
- 12. Помни каждый ученик, Знай любая кроха: Безопасность- хорошо, А халатность – плохо. Техника безопасности в кабинете
- 13. Техника безопасности в кабинете химии Категорически запрещается входить в кабинет химии без ...учителя В кабинете химии
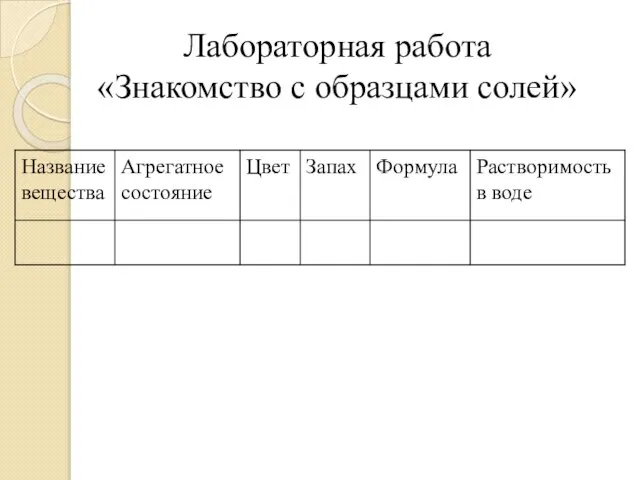
- 14. Лабораторная работа «Знакомство с образцами солей»
- 15. Физические свойства Соли – это твердые вещества разного цвета с различной растворимостью в воде
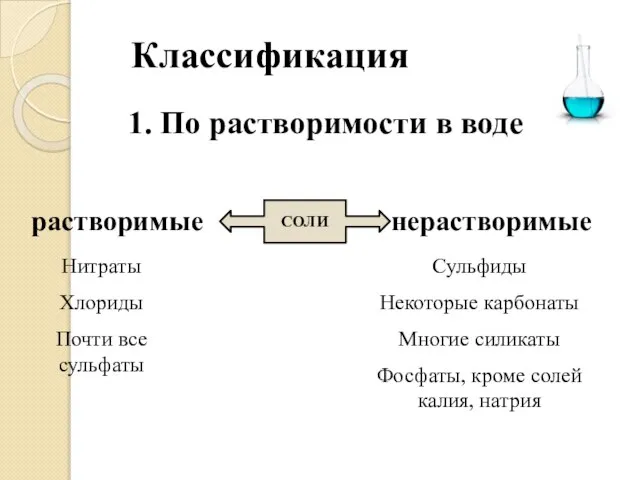
- 16. Классификация 1. По растворимости в воде СОЛИ растворимые нерастворимые Нитраты Хлориды Почти все сульфаты Сульфиды Некоторые
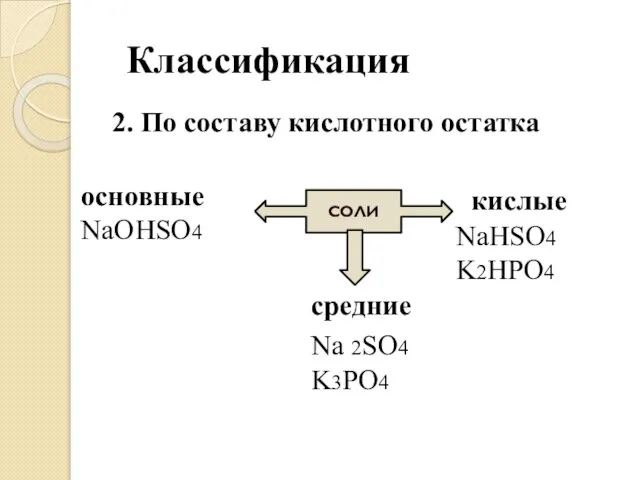
- 17. Классификация 2. По составу кислотного остатка
- 18. Тренажер для глаз Базарнова В. Ф.
- 19. Упражнения для улучшения мозгового кровообращения «Наклоны головы» Вперед – назад Вправо - влево
- 20. Упражнения для снятия утомления с плечевого пояса и рук «Рывки руками» «Сжимание кисти в кулак»
- 21. Упражнение для снятия напряжения с мышц туловища «Наклоны в сторону»
- 22. Задания: Назвать соли: KCl, LiNO3, BaSO4; Составьте формулы солей по названию: йодид натрия, сульфид цинка.
- 23. Критерии оценивая Оценка «5» - одна ошибка Оценка «4» - две ошибки Оценка «3» - три
- 24. Соляная зависимость самая древняя и самая сильная.Но люди не всегда испытывали такую зависимость от соли. Соли
- 25. Соли Гипс – кристаллогидрат сульфата кальция СаSO4 * 2H2O
- 26. Из мрамора (СаСО3) сделан дворец в Индии Тадж- Махал
- 27. Косметические соли
- 28. Лечение и профилактика заболеваний:
- 29. Рефлексия
- 30. Домашнее задание: Параграф 33 упр.3 стр. 112 Используя дополнительные источники информации, найдите примеры солей имеющих наибольшее
- 31. Спасибо за внимание!!!
- 33. Скачать презентацию
























 Химические формулы
Химические формулы 9-8 кислоты в свете ТЭД (1)
9-8 кислоты в свете ТЭД (1) Спирты
Спирты Адсорбционно-десорбционные взаимодействия фосфатов кальция и аминокислот
Адсорбционно-десорбционные взаимодействия фосфатов кальция и аминокислот Соли как производные кислот и оснований
Соли как производные кислот и оснований Интерактивная интеллектуальная игра Юный химик
Интерактивная интеллектуальная игра Юный химик Класс оксиды
Класс оксиды Обобщение знаний об углеводородах
Обобщение знаний об углеводородах ЕГЭ по химии: документы, регламентирующие структуру и содержание контрольных измерительных материалов
ЕГЭ по химии: документы, регламентирующие структуру и содержание контрольных измерительных материалов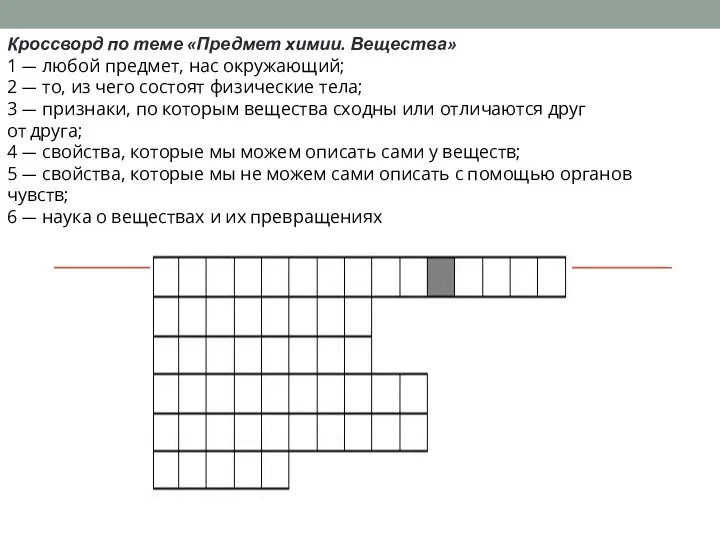 Предмет химии. Вещества
Предмет химии. Вещества 3bc28ca0711047a6880d20a6763f17db
3bc28ca0711047a6880d20a6763f17db Общая характеристика оксидов
Общая характеристика оксидов Золото
Золото Органическая химия. Ароматические углеводороды
Органическая химия. Ароматические углеводороды Методы получения нафтиридинов (всех изомеров)
Методы получения нафтиридинов (всех изомеров) Нефть и её переработка
Нефть и её переработка Оксид кремния
Оксид кремния Основания: номенклатура, классификация, применение, физические свойства
Основания: номенклатура, классификация, применение, физические свойства Алмаз. Свойства алмазов
Алмаз. Свойства алмазов Презентация на тему Соединения серы
Презентация на тему Соединения серы  Свойства солей, оксидов, оснований
Свойства солей, оксидов, оснований Модель химического образования на основе технологического подхода. Методическая система учителя химии
Модель химического образования на основе технологического подхода. Методическая система учителя химии Техника титрования и лабораторная посуда
Техника титрования и лабораторная посуда Уровень С1 в ГИА
Уровень С1 в ГИА Задачи. Периодическая система. Строение атома. Повторение
Задачи. Периодическая система. Строение атома. Повторение Азотсодержащие гетероциклические соединения пиррол
Азотсодержащие гетероциклические соединения пиррол Предельные углеводороды. Тест 19
Предельные углеводороды. Тест 19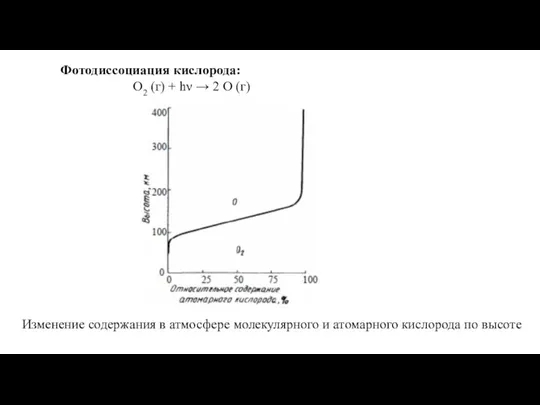 Фотодиссоциация кислорода
Фотодиссоциация кислорода