Содержание
- 2. Фосфины. Гомологические ряды Идентифицировано и описано около 85 фосфинов Существует как минимум 11 гомологических рядов: PnHn+2
- 3. Фосфин. Получение Гидролиз и алкоголиз фосфидов металлов (например, AlP, Ca3P4 (побочный продукт – P2H4)) Пиролиз фосфористой
- 4. Фосфин. Физические свойства Бесцветный ядовитый газ со специфическим запахом, напоминающим запах гнилой рыбы (чувствуется при концентрации
- 5. Фосфин. Химические свойства Раствор фосфина в воде – амфотерное соединение Самовоспламеняется на воздухе Сильный восстановитель Фосфин
- 6. Дифосфин (P2H4) При н. у. – бесцветная легколетучая жидкость, легко разлагается (ΔfH° ~21 кдж/моль) Оценочная температура
- 7. Продукты разложения дифосфина (E. Fluck, 1973)
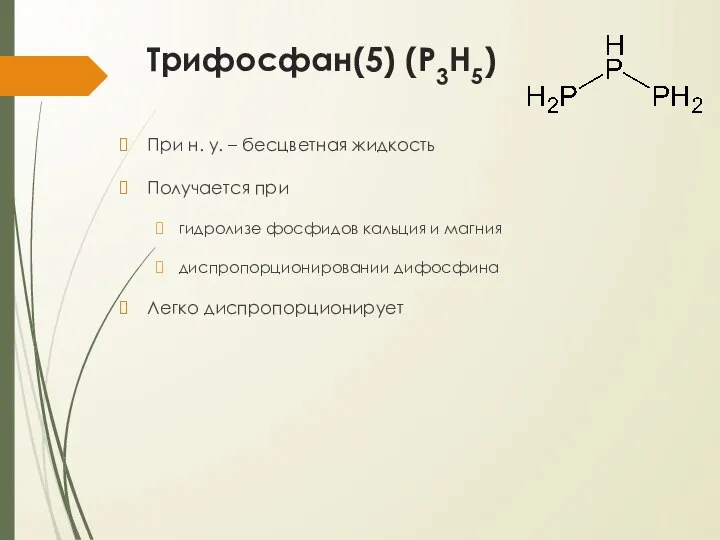
- 8. Трифосфан(5) (P3H5) При н. у. – бесцветная жидкость Получается при гидролизе фосфидов кальция и магния диспропорционировании
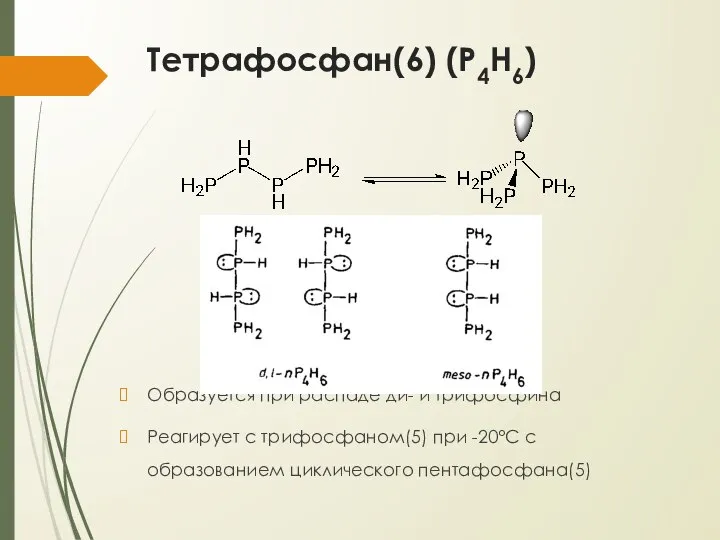
- 9. Тетрафосфан(6) (P4H6) Образуется при распаде ди- и трифосфина Реагирует с трифосфаном(5) при -20°С с образованием циклического
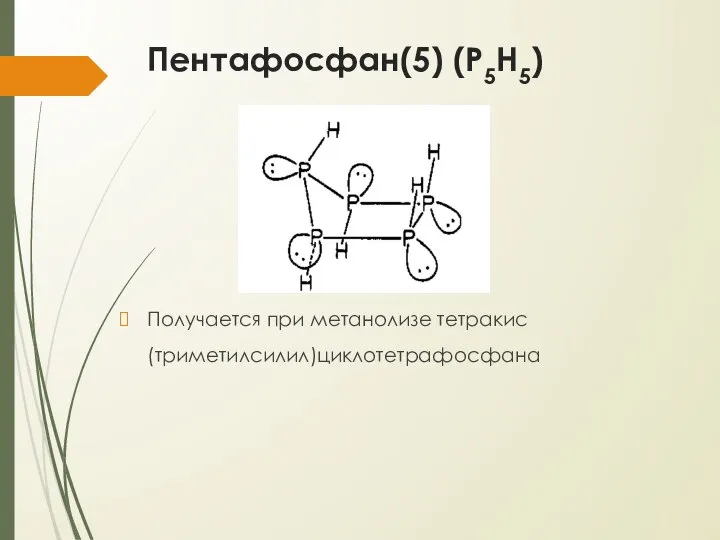
- 10. Пентафосфан(5) (P5H5) Получается при метанолизе тетракис(триметилсилил)циклотетрафосфана
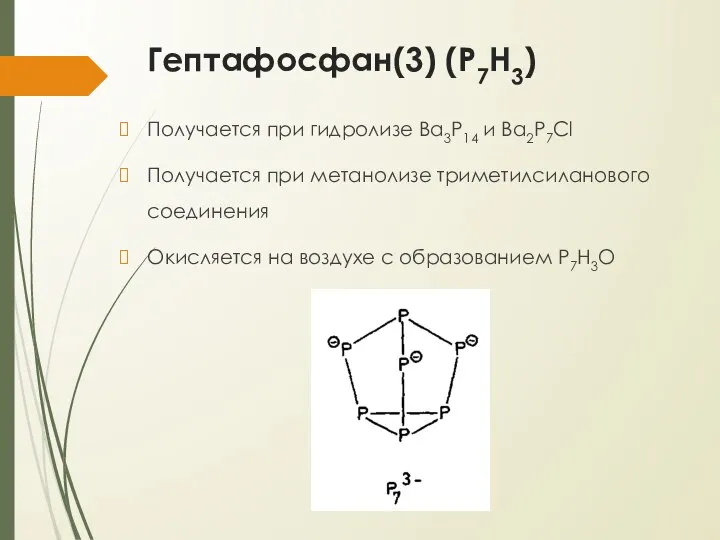
- 11. Гептафосфан(3) (P7H3) Получается при гидролизе Ba3P14 и Ba2P7Cl Получается при метанолизе триметилсиланового соединения Окисляется на воздухе
- 12. Галогениды фосфора Фосфор образует 3 ряда галогенидов – P2X4, PX3 и PX5 Все 12 существуют (PI5?)
- 13. Галогениды фосфора
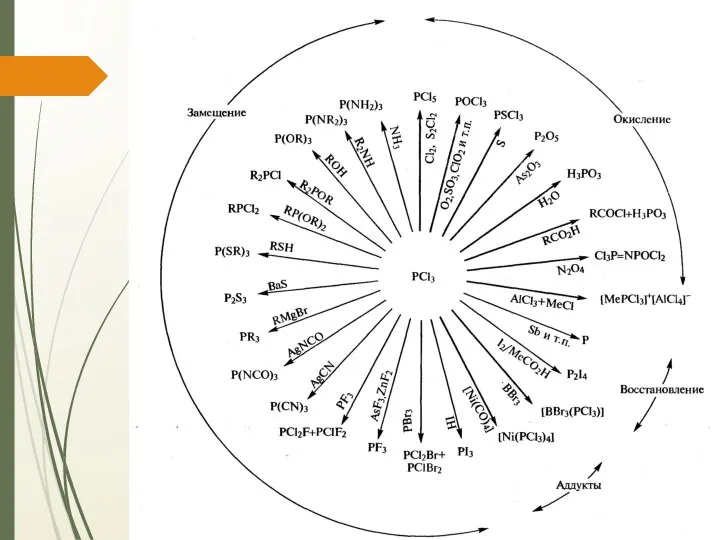
- 14. Тригалогениды фосфора Летучие и химически активные Получают косвенным путем и прямым синтезом Гидролизуются водой с образованием
- 16. Тетрагалогениды фосфора Получают из смешанных галогенидов … тригалогенидов … прямым синтезом
- 17. Пентагалогениды фосфора PF5 имеет молекулярное строение PCl5 в газовой фазе имеет молекулярное строение, в твердой фазе
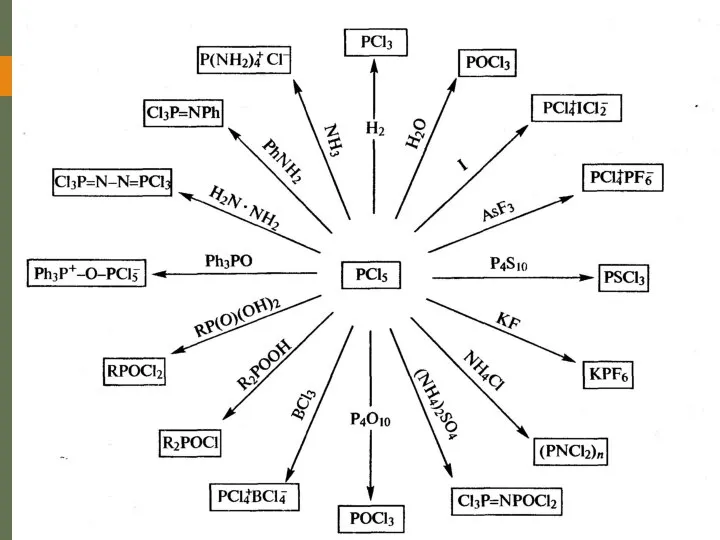
- 18. Пентагалогениды фосфора. Получение Замещение атомов галогенов Прямой синтез в избытке галогена Реакция галогена с тригалогенидом
- 19. Пентагалогениды фосфора
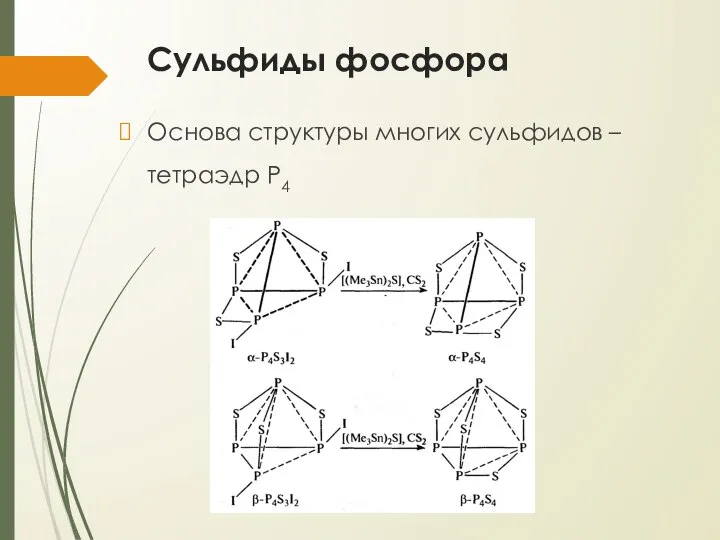
- 20. Сульфиды фосфора Основа структуры многих сульфидов – тетраэдр P4
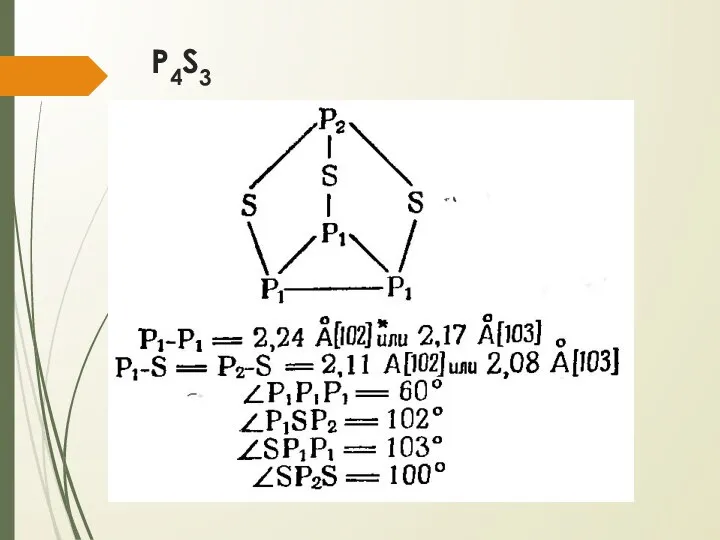
- 21. P4S3 Самый устойчивый сульфид Получается при нагревании серы с красным фосфором при t > 180°C в
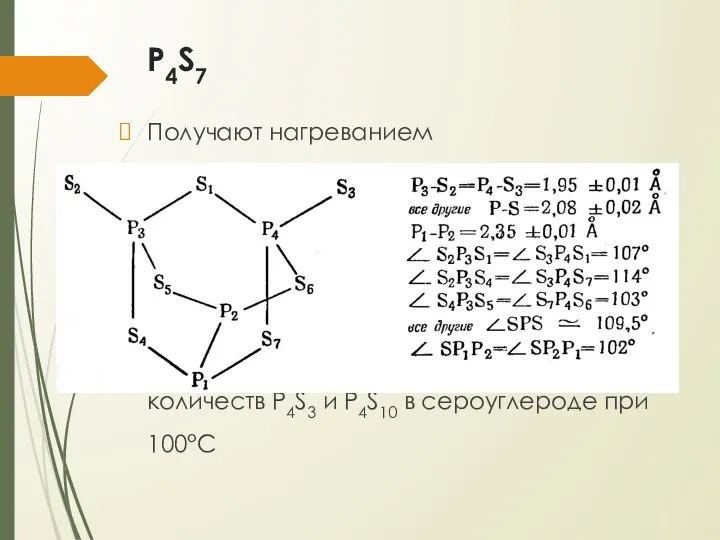
- 22. P4S7 Получают нагреванием стехиометрических количество фосфора и серы в присутствии 5% P4S3 в трубке из тугоплавкого
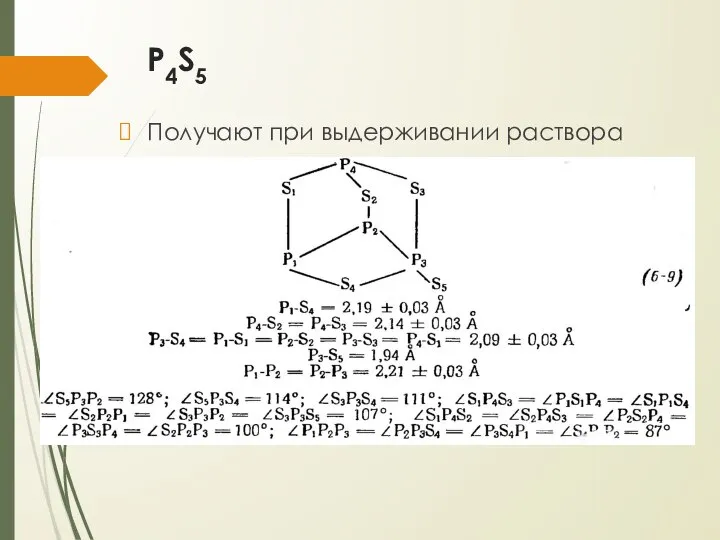
- 23. P4S5 Получают при выдерживании раствора стехиометрических количеств P4S3 и серы со следами иода на рассеянном дневном
- 24. Фосфорные кислоты
- 25. Фосфорные кислоты с двумя и более атомами Р Дифосфористая (пирофосфористая) H4P2O5 Фосфорноватая (гипофосфорная) H4P2O6 Дифосфорная (пирофосфорная)
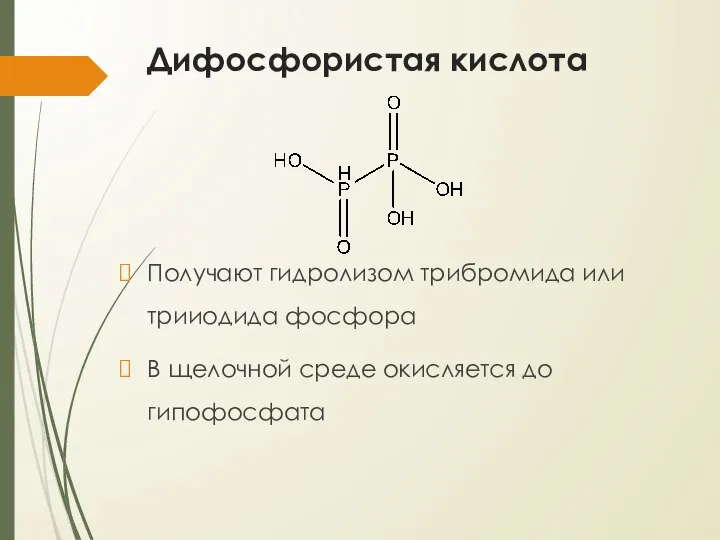
- 26. Дифосфористая кислота Получают гидролизом трибромида или трииодида фосфора В щелочной среде окисляется до гипофосфата
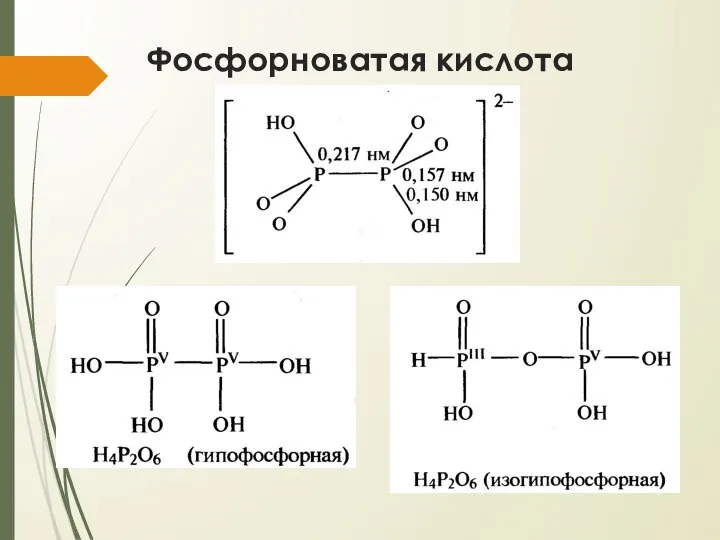
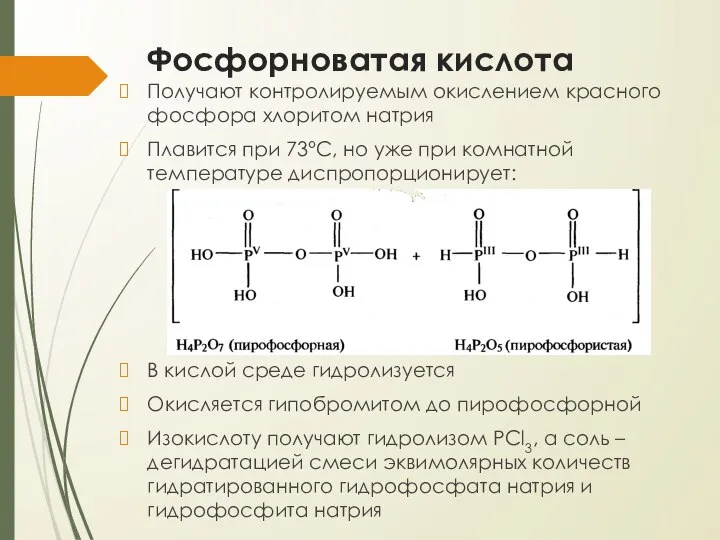
- 27. Фосфорноватая кислота
- 28. Фосфорноватая кислота Получают контролируемым окислением красного фосфора хлоритом натрия Плавится при 73°С, но уже при комнатной
- 30. Скачать презентацию














 Выращивание кристаллов
Выращивание кристаллов Презентация на тему Химические синонимы
Презентация на тему Химические синонимы  5 группа элементов
5 группа элементов Horľaviny. Horľavá látka
Horľaviny. Horľavá látka Презентация на тему Роль йода в организме
Презентация на тему Роль йода в организме 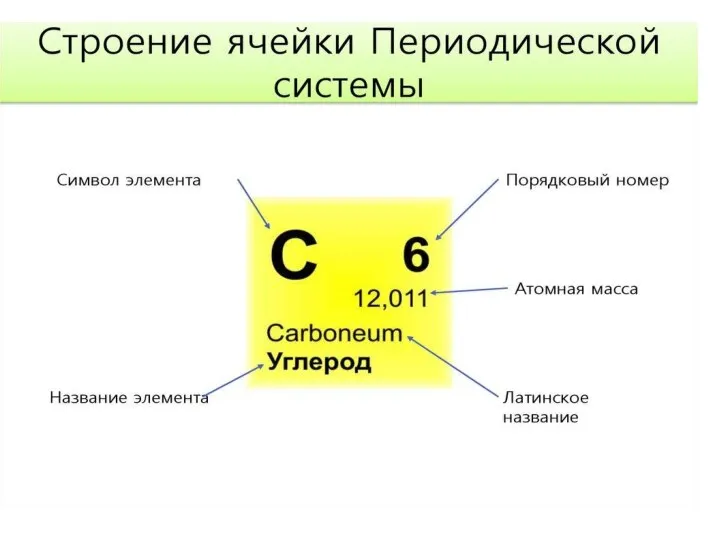 Строение ячейки периодической системы Менделеева
Строение ячейки периодической системы Менделеева Соли. Состав солей
Соли. Состав солей Разбор ДЗ. Титрование – общие моменты
Разбор ДЗ. Титрование – общие моменты Закон сохранения массы веществ. Уравнения химических реакций.
Закон сохранения массы веществ. Уравнения химических реакций. Комплексные соединения
Комплексные соединения Относительная атомная и молекулярная масса
Относительная атомная и молекулярная масса Алкены
Алкены Алюминий
Алюминий Теория электролитической диссоциации
Теория электролитической диссоциации Фотометрический анализ
Фотометрический анализ Углеродные материалы. Основные понятия и определения. Области их применения
Углеродные материалы. Основные понятия и определения. Области их применения Презентация на тему Строение атома и атомного ядра
Презентация на тему Строение атома и атомного ядра  Температурная зависимость скорости химической реакции
Температурная зависимость скорости химической реакции Драгоценные камни
Драгоценные камни Объёмный анализ
Объёмный анализ Непредельные углеводороды
Непредельные углеводороды Сера
Сера Оксиды. Классификация оксидов
Оксиды. Классификация оксидов Химия металлов. Влияние металлов на организм человека
Химия металлов. Влияние металлов на организм человека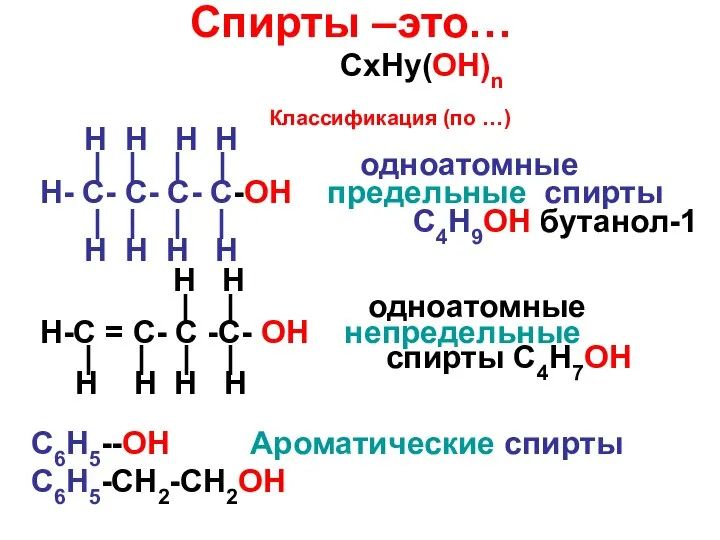 Спирты –это…
Спирты –это… Алюминийорганические соединения
Алюминийорганические соединения Презентация на тему Алмазы Индии
Презентация на тему Алмазы Индии  Химическая связь
Химическая связь