Содержание
- 2. Реакцию, уравнение которой N2(г) + 3Н2(г) ⮀ 2NН3(г) + Q относят к реакциям: 1) обратимым, экзотермическим
- 3. К обратимым реакциям не относятся: 1) MgCO3 ⭢ MgO + CO2 2) C2H6 ⭢ C2H4 +
- 4. К реакциям замещения относится взаимодействие: 1) метана и кислорода 2) брома и водорода 3) бутана и
- 5. Простое вещество может быть получено в реакциях 1) соединения и замещения 2) замещения и разложения 3)
- 6. Окислительно-восстановительная реакция соединения протекает между: 1) хлороводородом и аммиаком 2) аммиаком и кислородом 3) кислородом и
- 7. Скорость химической реакции горения угля в кислороде уменьшится при: 1) увеличении концентрации кислорода 2) повышении температуры
- 8. С наибольшей скоростью при комнатной температуре протекает реакция: 1) Zn и HCl(1%ный р-р) 2) Zn и
- 9. Скорость прямой реакции в системе: 2SO2 + O2 ⮀ 2SO3 + Q при увеличении давления в
- 10. Скорость реакции при повышении температуры на 40°С и температурном коэффициенте реакции, равном 2, увеличится в: 1)
- 11. Химическое равновесие сместится вправо при увеличении давления в системе: 1) H2 + Cl2 ⮀ 2HCl 2)
- 12. Химическое равновесие в системе С3Н8 ⮀ С3Н6 + Н2 – Q можно сместить в сторону продуктов
- 13. В соответствии с термохимическим уравнением 3Fe3O4+8Al=9Fe+4Al2O3+ 3330кДж при образовании 2 моль оксида алюминия: 1) выделяется 1655
- 14. Укажите все возможные способы смещения химического равновесия в сторону прямой реакции: NH3(г) + H2S(г) ⮀ NH4HS(тв)
- 15. Химическое равновесие в системе: N2(г) + 3Н2(г) ⮀ 2NН3(г) установилось при равновесных концентрациях: [NН3] = 0,4моль/л,
- 17. Скачать презентацию













 Предельные углеводороды. Алканы, насыщенные углеводороды, парафины, циклоалканы
Предельные углеводороды. Алканы, насыщенные углеводороды, парафины, циклоалканы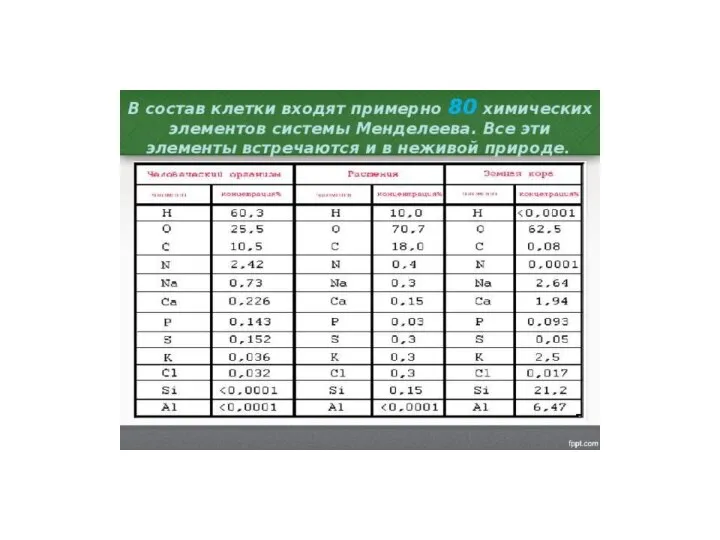 Состав клетки
Состав клетки Необратимый (совместный) гидролиз
Необратимый (совместный) гидролиз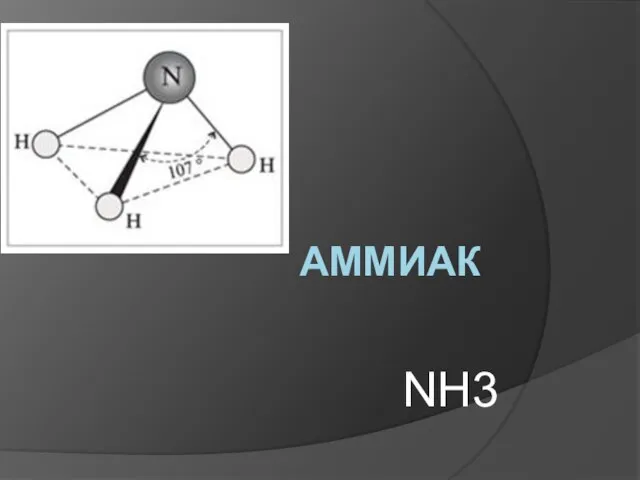 Аммиак NH3
Аммиак NH3 Химические свойства металлов
Химические свойства металлов Презентация на тему Процессы в растворах электролитическая диссоциация
Презентация на тему Процессы в растворах электролитическая диссоциация  9. Потомки светоносного элемента
9. Потомки светоносного элемента ЗАДАЧИ 9 класс
ЗАДАЧИ 9 класс Современные оборудования в лаборатории
Современные оборудования в лаборатории Химическое расследование. Химические свойства галогенов
Химическое расследование. Химические свойства галогенов Изомерия
Изомерия Элемент протактиний
Элемент протактиний Химические свойства металлов. Электрохимический ряд напряжения металлов
Химические свойства металлов. Электрохимический ряд напряжения металлов Добыча золота в России По теме «Внешние эффекты и права собственности»
Добыча золота в России По теме «Внешние эффекты и права собственности» AB-Polymerchemie Referenze
AB-Polymerchemie Referenze Порядок констант ССВ JHH в бензоле. Задачи
Порядок констант ССВ JHH в бензоле. Задачи Условия, замедляющие выход водорастворимых питательных веществ из удобрений на примере аммофоса
Условия, замедляющие выход водорастворимых питательных веществ из удобрений на примере аммофоса Азотная кислота
Азотная кислота Chimie bioorganique
Chimie bioorganique Бензол. Cвойства, реакции, применение
Бензол. Cвойства, реакции, применение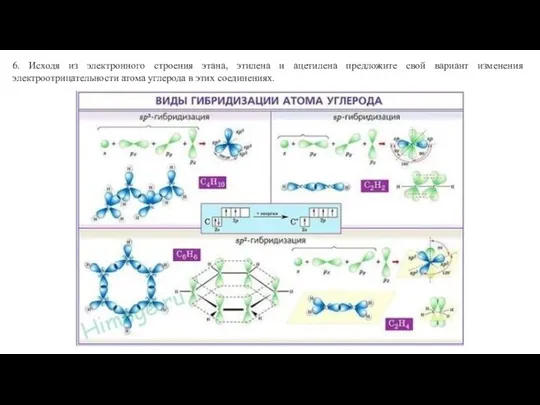 Виды гибридизации атома углерода
Виды гибридизации атома углерода Склероглюкан
Склероглюкан Презентация на тему Алюминий
Презентация на тему Алюминий  Практическая работа №1. Определение содержания нитратов в овощах и фруктах
Практическая работа №1. Определение содержания нитратов в овощах и фруктах Закон Авогадро
Закон Авогадро Презентация на тему Органическая химия. История развития
Презентация на тему Органическая химия. История развития  Влияние на скорость ферментативной реакции
Влияние на скорость ферментативной реакции Презентация на тему Атомы и молекулы
Презентация на тему Атомы и молекулы