Содержание
- 2. План урока 1) Классификация веществ; 2) Неорганические и органические кислоты, основания, амфотерные соединения: - определения -
- 3. Вопросы для повторения Какие бывают вещества? (неорганические и органические) Классификация неорганических веществ (простые и сложные) Определение
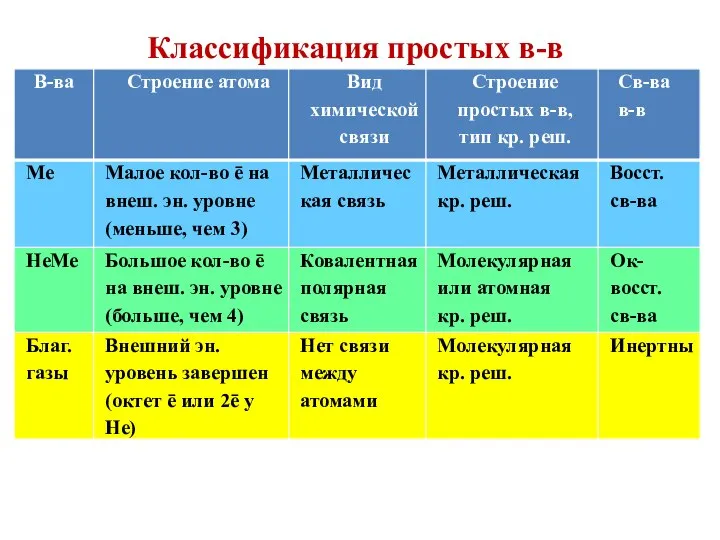
- 4. Классификация простых в-в
- 5. Классификация сложных веществ оксиды (несолеобразующие и солеобразующие: основные, кислотные и амфотерные) гидроксиды (кислоты, основания, амфотерные гидроксиды)
- 6. S8 AI(OH)3 H2SO3 NO BaO P2O5 HI табл. word Mg(OH)2 NaHSO3 (ZnOH)CI KNO3 KAI(SO4)2 Na3[AIF6] NH4Fe(SO4)2
- 7. Написать уравнения электролитической диссоциации NaHSO3→ (ZnOH)CI → KNO3 → KAI(SO4)2 → Na3[AIF6] → NH4Fe(SO4)2 →
- 8. Классификация органических веществ вид углеродной цепи (ациклические, циклические: карбоциклические, гетероциклические) наличие кратных связей табл. word
- 9. Неорганические и органические КИСЛОТЫ ОСНОВАНИЯ АМФОТЕРНЫЕ СОЕДИНЕНИЯ Определения: по структурной теории по электролитической теории по протолитической
- 10. Дайте характеристику по классификации и химическим свойствам след. веществ Сравните кислотные и основные свойства Н3РО4 H2SO4
- 11. Допишите уравнения реакций H2SO4 + КОН → CH3COOH + Mg(OH)2→ NH3 + HCI → CH3NH2 +
- 12. Вывод: Общими свойствами для неорганических и органических кислот и оснований является их взаимодействие друг с другом,
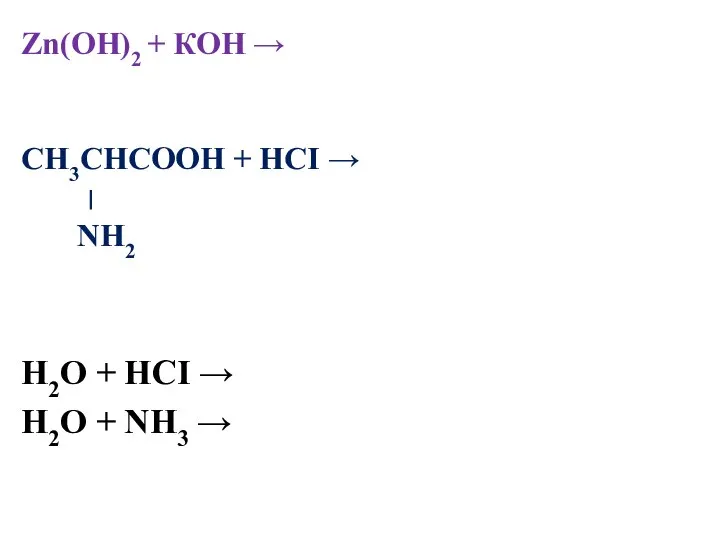
- 13. Zn(OH)2 + КОН → CH3CHCOOH + HCI → ׀ NH2 Н2О + НСI → Н2О +
- 14. Вывод: Амфотерные свойства проявляют оксиды и гидроксиды переходных Ме, а не типичных Ме и типичных НеМе.
- 15. Генетическая связь неорганических соединений Составьте генетический ряд для след. элементов Ва Сu S Si
- 16. Практическое осуществление ОВР ОВР между KMnO4 и Na2SO3 в различных средах (кислой, нейтральной и щелочной) Объясните
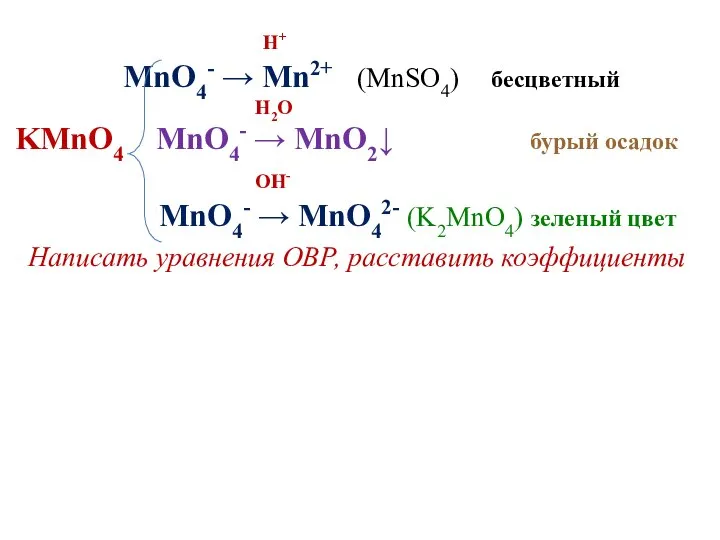
- 17. H+ MnO4- → Mn2+ (MnSO4) бесцветный H2O KMnO4 MnO4- → MnO2↓ бурый осадок OH- MnO4- →
- 18. KMnO4 + H2SO4 + Na2SO3 → K2SO4 + MnSO4 + Na2SO4 + H2O KMnO4 + H2O
- 20. Скачать презентацию




![Написать уравнения электролитической диссоциации NaHSO3→ (ZnOH)CI → KNO3 → KAI(SO4)2 → Na3[AIF6] → NH4Fe(SO4)2 →](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1024794/slide-6.jpg)








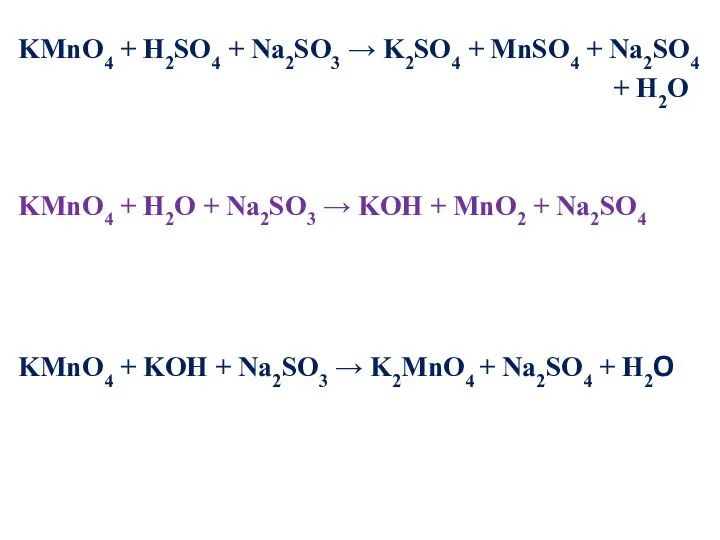
 Химические явления. Закон сохранения массы веществ
Химические явления. Закон сохранения массы веществ Непредельные углеводороды
Непредельные углеводороды Дисперсные системы
Дисперсные системы Фосфор в природе
Фосфор в природе Определение содержания солей в воде
Определение содержания солей в воде Решение задач на смеси, растворы и сплавы
Решение задач на смеси, растворы и сплавы Общая характеристика металлов
Общая характеристика металлов Презентация на тему Таблица Менделеева и строение атома
Презентация на тему Таблица Менделеева и строение атома  КВН по теме: Периодическая система химических элементов Д.И. Менделеева
КВН по теме: Периодическая система химических элементов Д.И. Менделеева Альдегиды. Номенклатура, изомерия. Получение альдегидов
Альдегиды. Номенклатура, изомерия. Получение альдегидов Нитраты в продуктах
Нитраты в продуктах Строение Алкенов
Строение Алкенов Способы получения металлов. Сплавы металлов
Способы получения металлов. Сплавы металлов Общие свойства металлов
Общие свойства металлов Дисперсные системы
Дисперсные системы Газообразные дисперсные системы (Аэрозоли)
Газообразные дисперсные системы (Аэрозоли) Химические средства защиты растений. Последствия применения пестицидов
Химические средства защиты растений. Последствия применения пестицидов Нефть. Способы переработки нефти
Нефть. Способы переработки нефти Стекло. Технология изготовления стекла
Стекло. Технология изготовления стекла Альфа- и бета- распад. Правило смещения
Альфа- и бета- распад. Правило смещения Кислородсодержащие органические вещества
Кислородсодержащие органические вещества Основные подходы к формированию и развитию социальных компетенций на уроках химии
Основные подходы к формированию и развитию социальных компетенций на уроках химии Дисперсные системы
Дисперсные системы Вебинар. Гидролиз солей
Вебинар. Гидролиз солей Основания, их классификация и свойства
Основания, их классификация и свойства Очистка хозяйственных и сточных вод от азота аммонийного с помощью нитрифицирующих бактерий
Очистка хозяйственных и сточных вод от азота аммонийного с помощью нитрифицирующих бактерий Химическая связь в молекулах. Экзаменационные вопросы
Химическая связь в молекулах. Экзаменационные вопросы Железо от начала времен до конца средних веков
Железо от начала времен до конца средних веков