Содержание
- 3. Сокращенное название «аммиак» которым мы всегда пользуемся, ввел в обиход в 1801 году русский ученый -
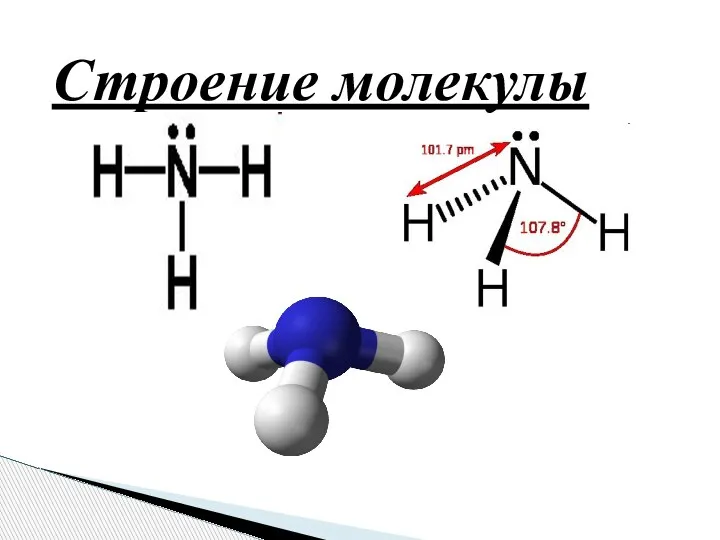
- 4. Строение молекулы
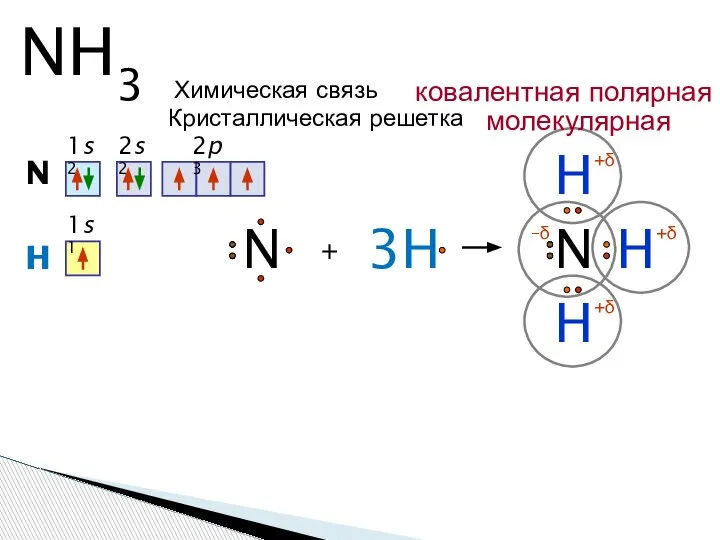
- 5. NH3 N 1s2 2s2 2p3 + H N H H 3H H N 1s1 +δ +δ
- 6. Физические свойства (при н.у. ) бесцветный газ с резким характерным запахом (запах нашатырного спирта) легче воздуха
- 7. Получение аммиака Для получения аммиака в лаборатории используют действие сильных щелочей на соли аммония: 2NH4Cl +
- 8. Промышленный способ получения аммиака основан на прямом взаимодействии водорода и азота: N2(г) + 3H2(г) ↔ 2NH3(г)
- 9. Химические свойства аммиака Для аммиака характерны реакции: 1) с изменением степени окисления атома азота (реакции окисления);
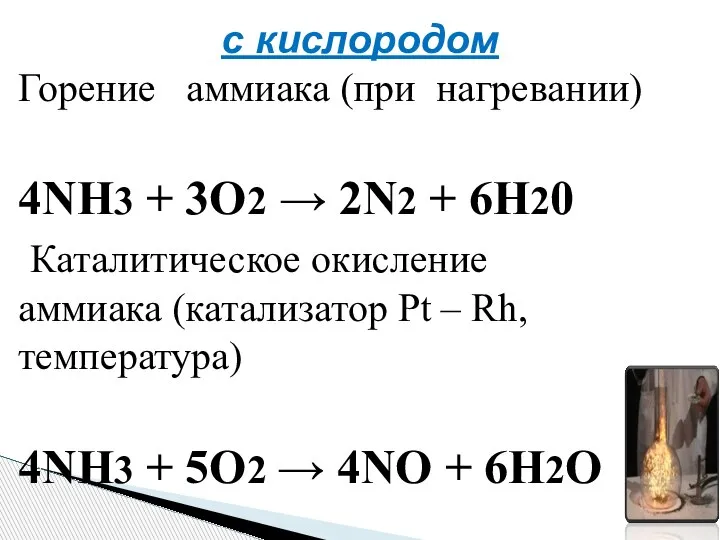
- 10. с кислородом Горение аммиака (при нагревании) 4NH3 + 3O2 → 2N2 + 6H20 Каталитическое окисление аммиака
- 11. с оксидами металлов 2NH3 +3CuO =3Cu + N2 +3H2O
- 12. с сильными окислителями 2NH3 + 3Cl2 = N2 + 6HCl (при нагревании)
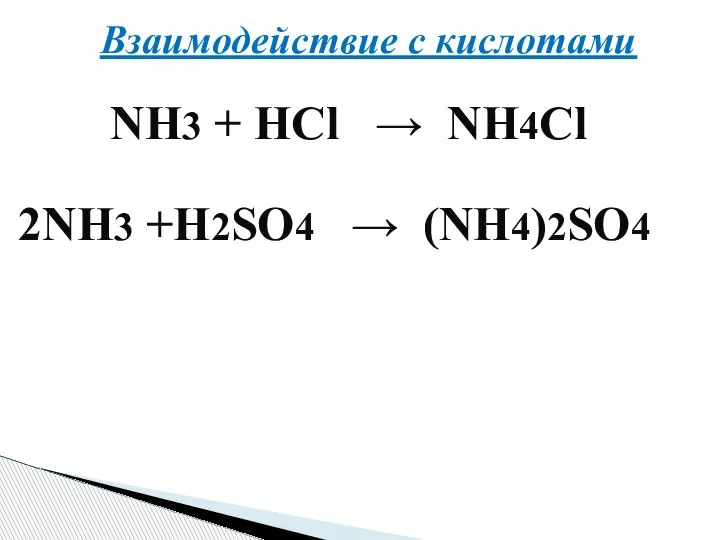
- 13. Взаимодействие с кислотами NH3 + HCl → NH4Cl 2NH3 +H2SO4 → (NH4)2SO4
- 14. Взаимодействие с водой NH3 + H2O = NH4OH При добавлении фенолфталеина‑ раствор становится малиновым, так как
- 15. Применение аммиака Производство пластмасс и волокон 2. В составе моющих средств
- 16. 3. Производство азотных удобрений 4. В сельском хозяйстве
- 17. 5. Производство азотной кислоты 6. Получение взрывчатых веществ
- 18. 7. В медицине
- 20. Скачать презентацию













 Индикаторная бумага
Индикаторная бумага Закон сохранения массы веществ
Закон сохранения массы веществ Полимеры. Виды полимеров
Полимеры. Виды полимеров Способы выражения концентраций растворов
Способы выражения концентраций растворов Отчет по ПП 03.01. Лаборант химического анализа
Отчет по ПП 03.01. Лаборант химического анализа Циклоалканы (полиметиленовые, циклопарафины, ациклические)
Циклоалканы (полиметиленовые, циклопарафины, ациклические) Алкилирование. Алкилирующие агенты
Алкилирование. Алкилирующие агенты Скорость химических реакций
Скорость химических реакций Амины. Аминокислоты. Белки
Амины. Аминокислоты. Белки Каустическая сода
Каустическая сода Модельные представления силикатных структур
Модельные представления силикатных структур О чем не узнаешь на уроке
О чем не узнаешь на уроке Количество теплоты, для получения углекислого газа. Химическое равновесие. Примеры. (Лекция 4)
Количество теплоты, для получения углекислого газа. Химическое равновесие. Примеры. (Лекция 4) Комментарии к выполненным заданиям по темам растворы и электролитическая диссоциация. 8 класс
Комментарии к выполненным заданиям по темам растворы и электролитическая диссоциация. 8 класс Техносферная безопасность. Химия как наука
Техносферная безопасность. Химия как наука Использование комплексно-ориентированных заданий на уроках
Использование комплексно-ориентированных заданий на уроках Электролиз (катод)
Электролиз (катод)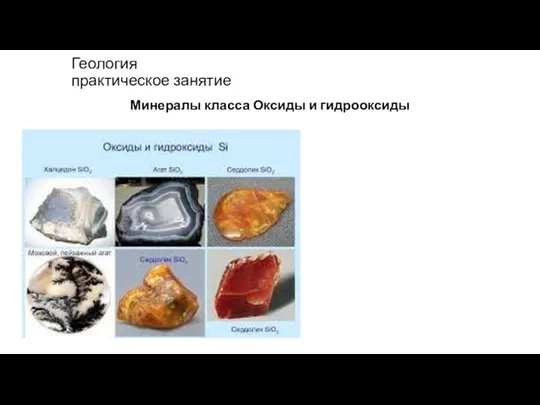 Оксиды и гидрооксиды
Оксиды и гидрооксиды Менделеевский период
Менделеевский период Коррозия металлов. Лекция №8
Коррозия металлов. Лекция №8 Биосенсоры. Основные принципы (лекция 2)
Биосенсоры. Основные принципы (лекция 2) 1_Лекція Комплексн
1_Лекція Комплексн Презентация на тему Кремний
Презентация на тему Кремний  Реакции неполного окисления в органике
Реакции неполного окисления в органике Путешествие по морю
Путешествие по морю Определение волокнистого состава хлопчатобумажных тканей. Практическая работа
Определение волокнистого состава хлопчатобумажных тканей. Практическая работа Сталь. Свойства стали
Сталь. Свойства стали Химические свойства карбоновых кислот
Химические свойства карбоновых кислот