Содержание
- 2. Железо-никелевые метеориты
- 3. Железо составляет большую часть земного ядра.
- 5. Fe
- 7. Железо — это простое вещество, металл, серебристо-белого цвета; его плотность 7,87 г/см3, температура плавления 1539 °C.
- 9. 26Fe 2e 8e 14e 2e – – – – –
- 10. Опты №1 3Fe + 2O2 = Fe3O4 + Q
- 11. При взаимодействии железа с галогенами (кроме йода) оно образует галогениды. 2Fe + 3Cl2 = 2FeCl3
- 12. При нагревании смеси железных опилок и порошка серы образуется сульфид железа (II). Fe + S =
- 13. Li, K, Ba, Ca, Na, Mg, Al, Mn, Zn, Cr, Fe, Co, Sn, Pb, H, Cu,
- 14. Железо восстанавливает из водных растворов солей металлы, расположенные правее в электрохимическом ряду напряжений. Если в реакцию
- 15. При восстановлении железом еще менее активных металлов, например, серебра из соли серебра, железо переходит в соединение,
- 16. Свойства оксидов Оксид железа(II) FeO обладает основными свойствами, ему отвечает основание Fe(OH)2. Оксид железа(III) Fe2O3 слабо
- 17. Свойства оксидов Гидроксид железа(III) Fe(OH)3 проявляет слабо амфотерные свойства, он способен реагировать только с концентрированными растворами
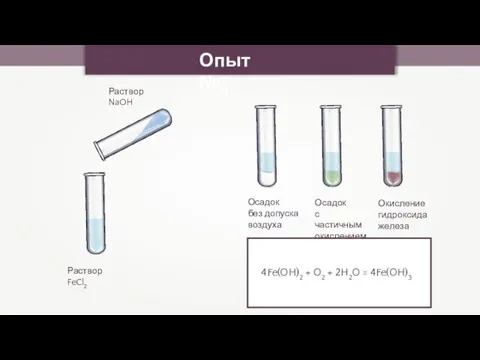
- 18. Раствор FeCl2 Раствор NaOH Осадок без допуска воздуха Опыт №2 Осадок с частичным окислением Окисление гидроксида
- 19. Железо Alchemist-hp
- 20. Железо в промышленности Красный железняк Красный железняк Norbert Kaiser
- 21. По запасу железных руд Россия занимает первое место в мире. Они залегают на Урале, в Курской
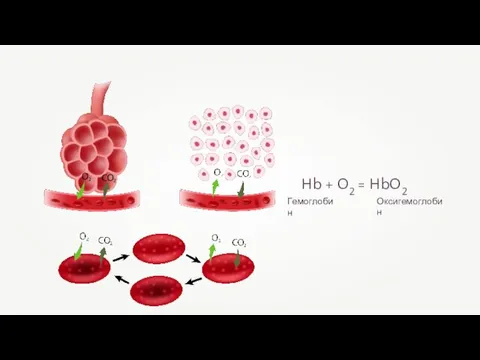
- 23. Hb + O2 = HbO2 Оксигемоглобин Гемоглобин
- 25. Железо
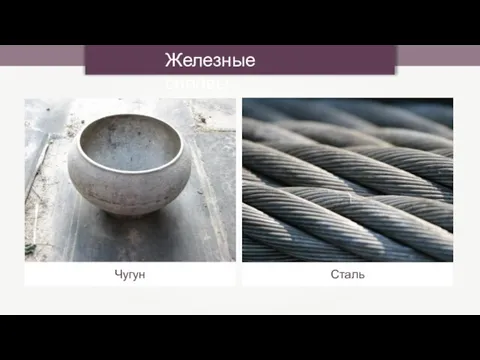
- 26. Железные сплавы Чугун Сталь
- 27. В чугуне содержится углерода больше, чем железо может удержать его при затвердевании в виде твердого раствора.
- 28. Особенность чугуна: при затвердевании он не сжимается, как большинство металлов, а расширяется. Поэтому чугун можно использовать
- 29. Решётка Летнего Сада
- 30. Сталь
- 31. Свойства стали в закаленном состоянии зависят от массовой доли в ней углерода: чем больше в стали
- 33. Легированная сталь
- 35. Быстрорежущая сталь
- 36. Нержавеющая сталь
- 37. Нержавеющие стали широко применяют в химической, машиностроительной, пищевой отраслях промышленности. В быт нержавеющая сталь вошла в
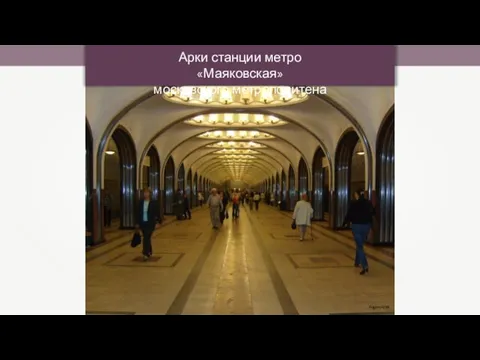
- 38. Арки станции метро «Маяковская» московского метрополитена Eugeny1988
- 39. Содержание железа у взрослого человека: 2–5 г. Содержание железа у взрослого человека: 300–400 мг.
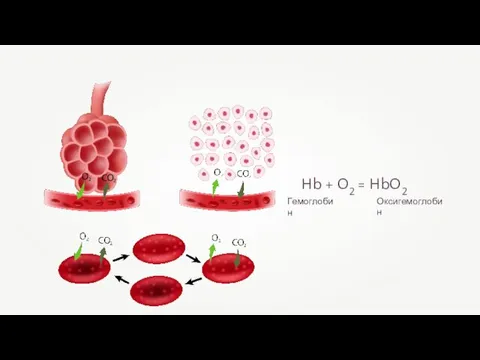
- 41. Hb + O2 = HbO2 Оксигемоглобин Гемоглобин
- 42. Железо выполняет множество важнейших функций, основная из которых — поддержание постоянного уровня гемоглобина в крови.
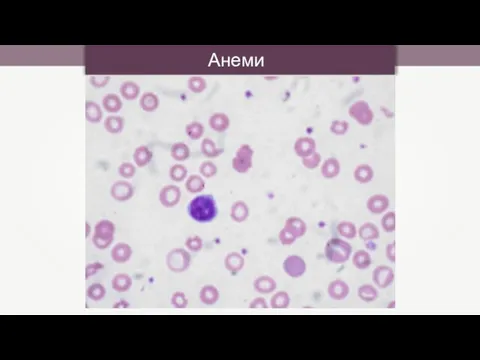
- 43. Анемия
- 47. Скачать презентацию



































 Химическое равновесие
Химическое равновесие Химия и география. Блиц-опрос. 7 класс
Химия и география. Блиц-опрос. 7 класс Амилаза. Строение амилазы
Амилаза. Строение амилазы Моющие и чистящие средства
Моющие и чистящие средства Основные химические законы
Основные химические законы Соли: получение
Соли: получение Синтетическое моторное масло. Маркировка моторных масел
Синтетическое моторное масло. Маркировка моторных масел Khim_8
Khim_8 Химические реакции
Химические реакции Систематизация знаний по периодической системе химических элементов
Систематизация знаний по периодической системе химических элементов химия
химия Nevarne snovi
Nevarne snovi Основания. Классификация
Основания. Классификация Стелс-материалы
Стелс-материалы Тип кристаллической решетки у белого фосфора…. Тест
Тип кристаллической решетки у белого фосфора…. Тест Классификация и свойства кислот
Классификация и свойства кислот Сeквенирование нуклеиновых кислот
Сeквенирование нуклеиновых кислот Набор для выращивания монокристалла. Защита проекта
Набор для выращивания монокристалла. Защита проекта Алканы. Строение, номенклатура, изомерия, физические свойства
Алканы. Строение, номенклатура, изомерия, физические свойства Реакции разложения и соединения
Реакции разложения и соединения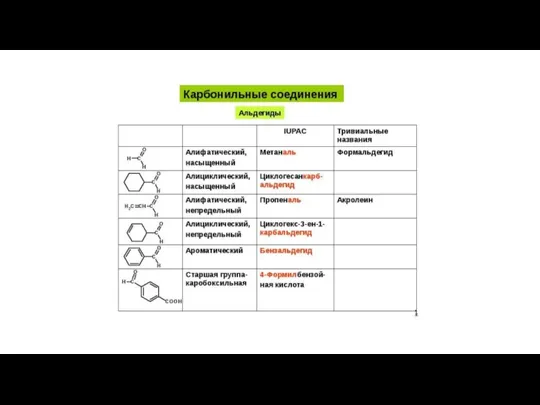 Карбонильные соединения (альдегиды)
Карбонильные соединения (альдегиды) карбоновые кислоты
карбоновые кислоты Вуглеводи. Групи
Вуглеводи. Групи Вычисление температур стеклования полимера при различных степенях отверждения смолы
Вычисление температур стеклования полимера при различных степенях отверждения смолы Сера
Сера Валенттілік. Атом-молекулалы ілім
Валенттілік. Атом-молекулалы ілім Классификация органических соединений
Классификация органических соединений Метанол. Краткая характеристика
Метанол. Краткая характеристика