Содержание
- 2. Актюбинский технико- технологический колледж Тема: Закон Гесса. Термохимические уравнения Преподователь: Жаржанова Г.К. Гр: 412. Дата 15.10.2020
- 3. 1. Основные понятия термохимии. 2. Закон Гесса и его следствия. 3. Примеры и расчеты по термохимическим
- 4. Термохимия - раздел физической химии изучающий тепловые эффекты, сопровождающие химические и физикохимические процессы (химические реакции, фазовые
- 5. Химическая реакция как термодинамический процесс, заключается в превращении одних веществ в другие, за счет изменения состава
- 6. Для физико-химических процессов действует закон сохранения массы, установленный М.В. Ломоносовым (m1 = m2). /МАССА / Химические
- 8. Теплота реакции - теплота, выделяемая или поглощаемая при химической реакции. Тепловой эффект химической реакции (ΔQ) –энергия,
- 9. Всякая система имеет некоторый запас энергии, определяемый имеющимися в ней веществами, их количеством, температурой и давлением.
- 10. H= U + pV Q= ΔH H – энтальпия U – внутренняя энергия р - давление
- 11. Δr H⁰ - стандартная теплота реакции – это теплота одного оборота реакции при стандартных условиях; она
- 12. Это уравнение химической реакции, в котором указан тепловой эффект реакции 2Н2 + О2 = 2Н2О +
- 13. Зная энергию химических связей, можно по разности узнать тепловой эффект реакции Для реакции H2 + Cl2
- 14. Теплота образования соединения (Qобр.) – это тепловой эффект реакции образования одного моль соединения из простых веществ,
- 15. Тепловой эффект химической реакции равен сумме теплот образования всех продуктов реакции минус сумма теплот образования исходных
- 17. В 1836 г. профессор Петербургского горного института Герман Иванович Гесс установил основной закон термохимии, который является
- 19. Закон Гесса позволяет обращаться с термохимическими уравнениями, как с алгебраическими, т.е. складывать, вычитать, умножать и делить
- 20. Пример: вычислить тепловой эффект реакции: Fe2O3 + 2Al = 2Fe + Al2O3, если известно, что Qобр
- 21. Решение Δ Q= Qобр (СО2) •3 - Qобр (Fe2O3) + Qобр(СО) •3= 394•3 – 820 +
- 22. Контрольные вопросы
- 23. Дайте определение: Контрольные вопросы Вычислите термохимические расчеты. /след сдайд/
- 24. Вычислить тепловой эффект реакции: Fe2O3 + 3CO = 2Fe + 3CO2 Если: Qобр (Fe2O3)= 820кдж/моль Qобр(СО2)
- 25. 1. Из нижеследующих химических реакций определите экзотермическую реакцию: А) Ca(OH)2 = CaO + H2O 67
- 27. Скачать презентацию
























 Выращивание кристаллов
Выращивание кристаллов Презентация на тему Химические синонимы
Презентация на тему Химические синонимы  5 группа элементов
5 группа элементов Horľaviny. Horľavá látka
Horľaviny. Horľavá látka Презентация на тему Роль йода в организме
Презентация на тему Роль йода в организме 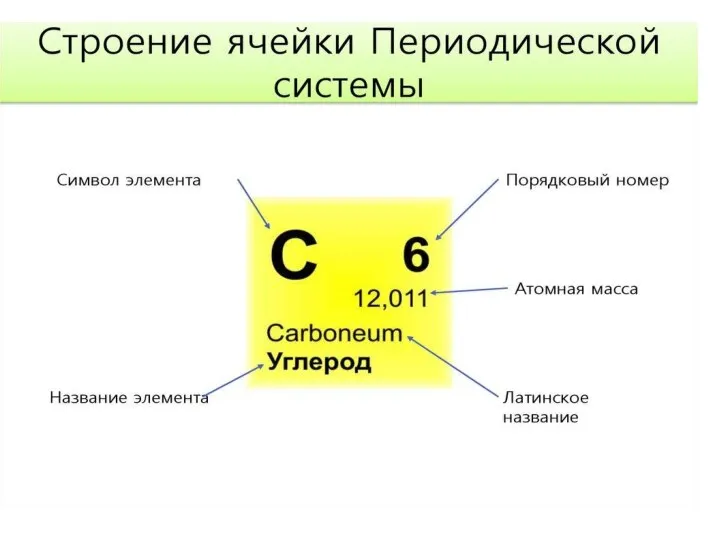 Строение ячейки периодической системы Менделеева
Строение ячейки периодической системы Менделеева Соли. Состав солей
Соли. Состав солей Разбор ДЗ. Титрование – общие моменты
Разбор ДЗ. Титрование – общие моменты Закон сохранения массы веществ. Уравнения химических реакций.
Закон сохранения массы веществ. Уравнения химических реакций. Комплексные соединения
Комплексные соединения Относительная атомная и молекулярная масса
Относительная атомная и молекулярная масса Алкены
Алкены Алюминий
Алюминий Теория электролитической диссоциации
Теория электролитической диссоциации Фотометрический анализ
Фотометрический анализ Углеродные материалы. Основные понятия и определения. Области их применения
Углеродные материалы. Основные понятия и определения. Области их применения Презентация на тему Строение атома и атомного ядра
Презентация на тему Строение атома и атомного ядра  Температурная зависимость скорости химической реакции
Температурная зависимость скорости химической реакции Драгоценные камни
Драгоценные камни Объёмный анализ
Объёмный анализ Непредельные углеводороды
Непредельные углеводороды Сера
Сера Оксиды. Классификация оксидов
Оксиды. Классификация оксидов Химия металлов. Влияние металлов на организм человека
Химия металлов. Влияние металлов на организм человека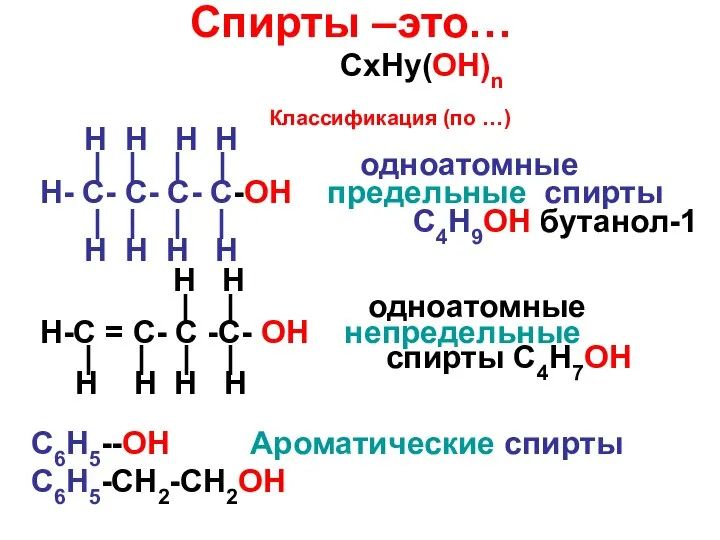 Спирты –это…
Спирты –это… Алюминийорганические соединения
Алюминийорганические соединения Презентация на тему Алмазы Индии
Презентация на тему Алмазы Индии  Химическая связь
Химическая связь