Содержание
- 2. Цели урока: познакомить учащихся с основными способами решения задач по химическим уравнениям: находить количество, массу и
- 3. Какое явление не является признаком химических превращений: а) появление осадка; б) выделение газа; в) изменение объема;
- 4. «Куча мала» 4Al + 3O2 = 2Al2O3 MgCO3= MgO + CO2 2HgO= 2Hg + O2 2Na
- 5. Алгоритм решения расчетных задач с использованием уравнений химических реакций. 1. Внимательно прочитайте текст задачи 2. Составьте
- 6. Задача 1. Вычислите массу кислорода, выделившегося в результате разложения порции воды массой 9 г. Дано: m(Н20)
- 7. Над формулой в уравнении реакции запишем найденное значение количества вещества, а под формулами веществ — стехиометрические
- 8. Следовательно, n(O2)=0,25 моль Найдем массу вещества, которую требуется вычислить m(O2)= n(O2)*M(O2) m(O2) = 0,25 моль •
- 9. Задача 2 Вычисление объема вещества по известной массе другого вещества, участвующего в реакции Вычислите объем кислорода
- 10. Запишем уравнение реакции. Расставим коэффициенты 2Н2О = 2Н2 + О2 Над формулой в уравнении реакции запишем
- 11. Вычислим количество вещества, массу которого требуется найти. Для этого составим пропорцию 0,5моль х моль 2 моль
- 12. Задачи для самостоятельного решения При восстановлении углем оксидов Fe2O3 и SnO2 получили по 20 г Fe
- 13. Решение задачи 1. Дано: Решение: m(Fe) = 20г n(Fe)= m/M, n(Fe) = 20г/56г/моль=0,36моль m(Fe2O3)=? хмоль 0,36моль
- 14. Решение задачи 2 Дано: Решение: m(Cu2O)=10г m (CuO)=10г 1. Cu2O + H2 = 2Cu + H2O
- 15. CuO + H2 = Cu + H2O n(CuO) = m/ M(CuO) n(CuO) = 10г/ 80г/моль =
- 16. Домашнее задание изучить материал учебника с. 45-47, решить задачу Какую массу оксида кальция и какой объём
- 18. Скачать презентацию















 Ko pēta ķīmija
Ko pēta ķīmija Аргентум, или серебро
Аргентум, или серебро Хлороводород и соляная кислота
Хлороводород и соляная кислота Исследование возможности создания порохов на основе 1,1диамино-2,2-динитроэтилена
Исследование возможности создания порохов на основе 1,1диамино-2,2-динитроэтилена Лавка возможностей
Лавка возможностей Водород – первый элемент в периодической таблице
Водород – первый элемент в периодической таблице Алкены
Алкены Как уберечь себя от опасности на уроках химии
Как уберечь себя от опасности на уроках химии Классификация силикатов
Классификация силикатов Синтетические каучуки
Синтетические каучуки 3 Серная кислота
3 Серная кислота Строение электронной оболочки атома часть 2
Строение электронной оболочки атома часть 2 Каучук негізіндегі материалдар
Каучук негізіндегі материалдар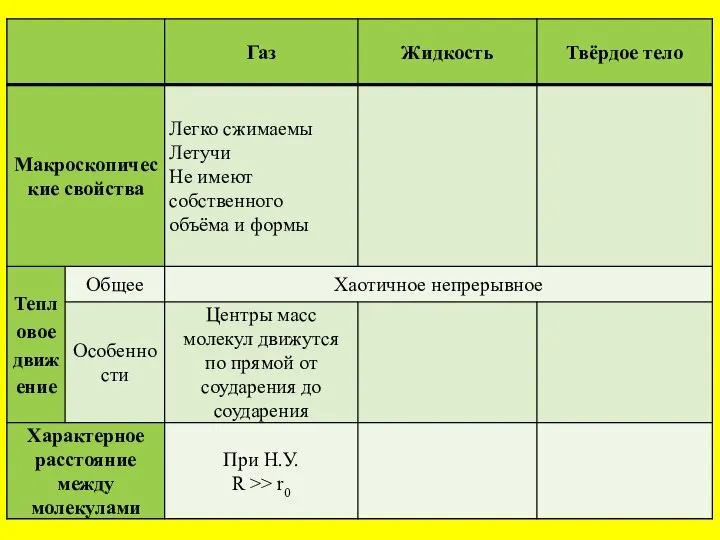 Макроскопические свойства
Макроскопические свойства Знакомство с химической посудой и лабораторным оборудованием. Правила техники безопасности
Знакомство с химической посудой и лабораторным оборудованием. Правила техники безопасности Проверочный тест. Номенклатура алканов
Проверочный тест. Номенклатура алканов Диеновые углеводороды. Алкадиены
Диеновые углеводороды. Алкадиены Аметист
Аметист Соли в свете теории электролитической диссоциации (ТЭД)
Соли в свете теории электролитической диссоциации (ТЭД) Составление ионных уравнений
Составление ионных уравнений Химическая термодинамика. Экзаменационные вопросы
Химическая термодинамика. Экзаменационные вопросы Классификация методов переработки пластмасс
Классификация методов переработки пластмасс Вещества простые и сложные
Вещества простые и сложные Подготовка выпускников к ГИА по химии: опыт, проблемы, перспективы
Подготовка выпускников к ГИА по химии: опыт, проблемы, перспективы Мифы и реальность о суперклее
Мифы и реальность о суперклее Презентация по Химии "Ароматические углеводороды в природе. Области их применения"
Презентация по Химии "Ароматические углеводороды в природе. Области их применения"  Карбоновые кислоты. Д.И. Менделеев
Карбоновые кислоты. Д.И. Менделеев Почему химия важна в профессии ювелира?
Почему химия важна в профессии ювелира?