Содержание
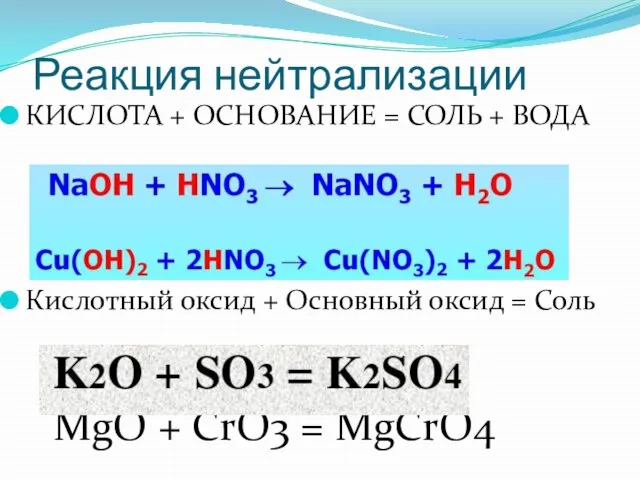
- 2. Реакция нейтрализации КИСЛОТА + ОСНОВАНИЕ = СОЛЬ + ВОДА Кислотный оксид + Основный оксид = Соль
- 3. Похимичим!
- 4. Реакции кислот с основными оксидами
- 5. Похимичим!
- 6. Кислоты. Сильная кислота + Соль слабой кислоты = Слабая кислота + соль сильной кислоты. H2SO4 +
- 8. Похимичим!
- 9. Реакции кислот с металлами
- 11. Похимичим!
- 13. Основания
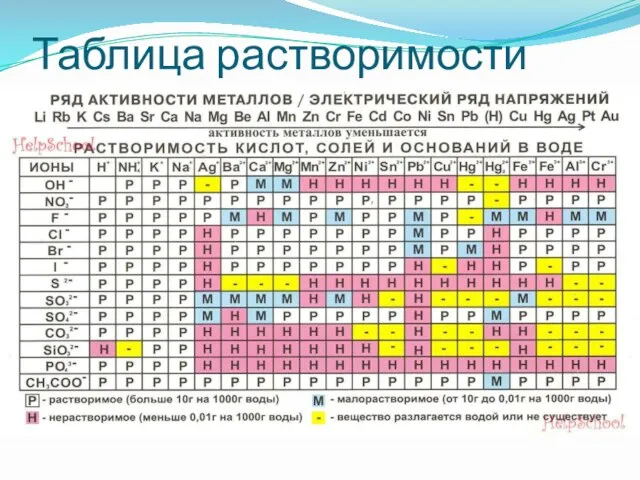
- 14. Таблица растворимости
- 15. Похимичим!
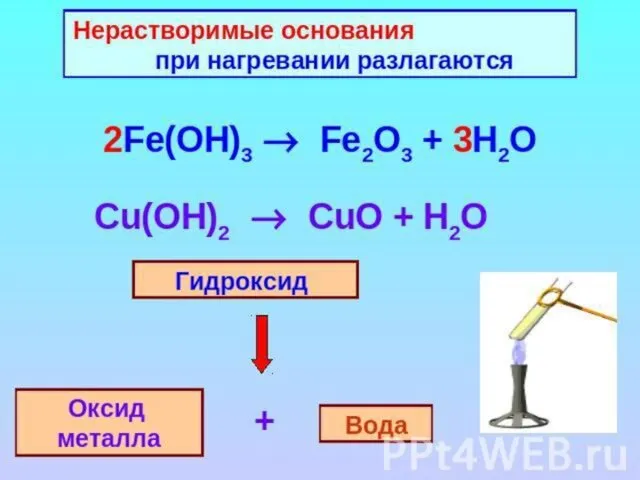
- 16. Разложение нерастворимых гидроксидов.
- 18. Скачать презентацию












 Обмен липидов
Обмен липидов Ковалентная связь между одинаковыми атомами неметаллов
Ковалентная связь между одинаковыми атомами неметаллов Классификация органических соединений
Классификация органических соединений Concise asymmetric total synthesis of lycopodine
Concise asymmetric total synthesis of lycopodine ЛКМ на основе кремнийорганических соединений
ЛКМ на основе кремнийорганических соединений Строение бензола
Строение бензола Строение электронных оболочек атомов. 8 класс
Строение электронных оболочек атомов. 8 класс Презентация на тему Типы химических реакций (8 класс)
Презентация на тему Типы химических реакций (8 класс)  Изомерия. Виды изомерии
Изомерия. Виды изомерии Реакции ионного обмена
Реакции ионного обмена Презентация по химии на тему _Высокомолекулярные Соединения_ (1)
Презентация по химии на тему _Высокомолекулярные Соединения_ (1) Пуриновые основания
Пуриновые основания Аналитическая химия. Введение
Аналитическая химия. Введение Презентация на тему Роль йода в организме
Презентация на тему Роль йода в организме  Хлор
Хлор Виготовлення водних розчинів з заданою масовою часткою розчиненої речовини
Виготовлення водних розчинів з заданою масовою часткою розчиненої речовини Агрегатные состояния веществ
Агрегатные состояния веществ Металлы 1 А - группы. Щелочные металлы
Металлы 1 А - группы. Щелочные металлы Ароматические углеводороды
Ароматические углеводороды Амфотерные гидроксиды
Амфотерные гидроксиды География. Уральские самоцветы
География. Уральские самоцветы Кислотность почв с.Берёзовка МОУ «СОШ с.Берёзовка» Колесников Иван, 9 класс Пряхина Виктория, 8 класс
Кислотность почв с.Берёзовка МОУ «СОШ с.Берёзовка» Колесников Иван, 9 класс Пряхина Виктория, 8 класс Карбонаты (3)
Карбонаты (3) Общая характеристика элементов главной подгруппы VI группы (подгруппы кислорода)
Общая характеристика элементов главной подгруппы VI группы (подгруппы кислорода) Команда Оптимисты
Команда Оптимисты Скорость химической реакции
Скорость химической реакции От простых правил к сложным структурам. Метод валентных связей. Принцип VSEPR
От простых правил к сложным структурам. Метод валентных связей. Принцип VSEPR