«атом» происходит от греческого слова, означающего «неделимый», поскольку греки думали, что, если делить некую вещь до тех пор, пока станет невозможным это делать, в результате последним останется атом. Сейчас, даже несмотря на то, что греки знали об этом, мы не можем доподлинно сказать, что именно они открыли атом. Прежде всего их вера в атом была ненаучной: она не исходила ни из какой-либо научной информации и не подтверждалась ею.
Атом, как мы знаем, был открыт на основе научных исследований и теорий. Приблизительно до начала XIX века идея, из чего состоит материя, или субстанция, рассматривалась только философами! Потом появился английский химик и математик Джон Дальтон, и в 1803 году он был первым, кто развил научную теорию атома.
Дальтон был старательным экспериментатором. Он взвешивал образцы многих газов и выявлял разницу в их массах. Он обнаружил, что газы так же, как и твердые и жидкие вещества, состоят из невероятно мелких частиц, которые он также назвал атомами. Он высчитал относительные массы для атомов известных ему элементов. Когда Дальтон установил, что атомы разных элементов имеют различные свойства и различные массы, он по-настоящему положил начало научному познанию атома.
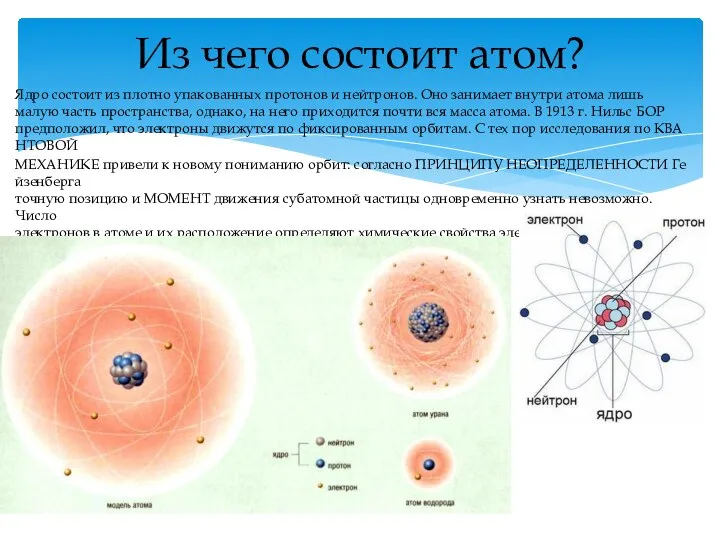
Кто открыл атом?





 Классификация и свойства кислот
Классификация и свойства кислот Фосфорные удобрения
Фосфорные удобрения Альдегиды. Свойства альдегидов
Альдегиды. Свойства альдегидов Типы химических реакций
Типы химических реакций Циклоалканы. Строение молекул
Циклоалканы. Строение молекул Оптические свойства ювелирных камней. Цвет плеохроизм. Часть 1
Оптические свойства ювелирных камней. Цвет плеохроизм. Часть 1 Метаморфизм
Метаморфизм Полиуретаны. Структура и строение
Полиуретаны. Структура и строение Основные классы неорганических соединений
Основные классы неорганических соединений Классификация неорганических веществ
Классификация неорганических веществ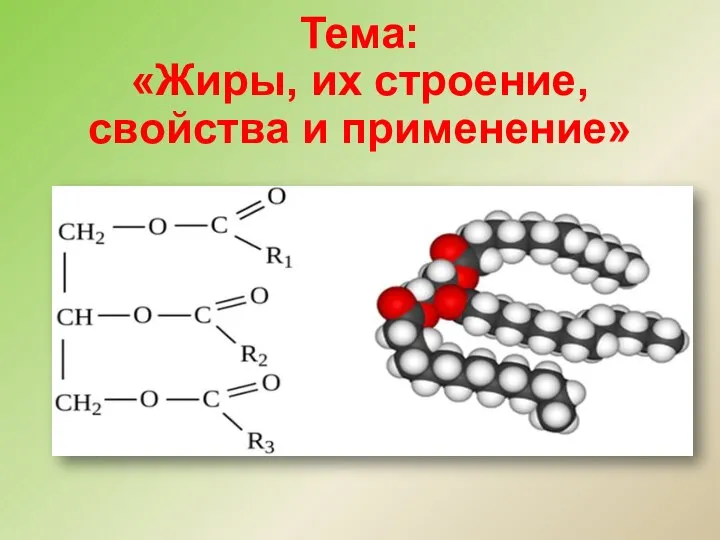 Жиры, их строение, свойства и применение
Жиры, их строение, свойства и применение Ковалентная полярная химическая связь
Ковалентная полярная химическая связь Типичные ошибки выпускников при решении задач ЕГЭ по органической химии
Типичные ошибки выпускников при решении задач ЕГЭ по органической химии Викторина Что это?
Викторина Что это? Концентрации растворов и эквиваленты веществ
Концентрации растворов и эквиваленты веществ Вода как растворитель. Растворы. Растворимость. 8 класс
Вода как растворитель. Растворы. Растворимость. 8 класс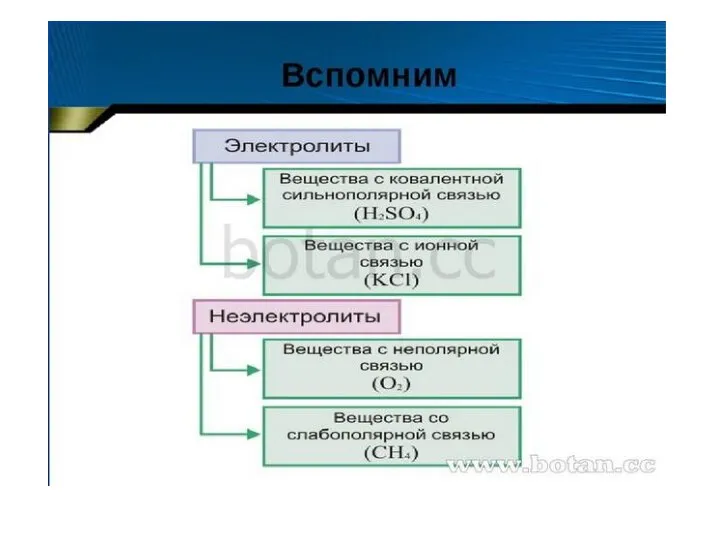 Диссоциация кислот, щелочей солей
Диссоциация кислот, щелочей солей Основной государственный экзамен. Химия 2022. Задание 2
Основной государственный экзамен. Химия 2022. Задание 2 Тренажер Химическая азбука для учащихся 8 класса
Тренажер Химическая азбука для учащихся 8 класса Графический диктант. Азот и Аммиак
Графический диктант. Азот и Аммиак Медь и её сплавы
Медь и её сплавы Молекулярно-кинетическая теория. Макро- и микропараметры
Молекулярно-кинетическая теория. Макро- и микропараметры Техника безопасности при работе в химическом кабинете
Техника безопасности при работе в химическом кабинете Применение алкинов
Применение алкинов Графит. Химические свойства
Графит. Химические свойства Презентация на тему Уравнение Менделеева-Клапейрона
Презентация на тему Уравнение Менделеева-Клапейрона  Характеристика углерода
Характеристика углерода Парфюмерные товары
Парфюмерные товары