Содержание
- 2. ОБРАТИМЫЕ И НЕОБРАТИМЫЕ ХИМИЧЕСКИЕ РЕАКЦИИ ОБРАТИМЫЕ РЕАКЦИИ : Обратимые реакции — химические реакции, протекающие одновременно в
- 3. ПРИМЕР ОБРАТИМОЙ РЕАКЦИИ
- 4. НЕОБРАТИМЫЕ ХИМИЧЕСКИЕ РЕАКЦИИ Необратимыми называют такие химические процессы, продукты которых не способны реагировать друг с другом
- 5. ПРИМЕР НЕОБРАТИМОЙ РЕАКЦИИ
- 7. Скачать презентацию
Слайд 2ОБРАТИМЫЕ И НЕОБРАТИМЫЕ ХИМИЧЕСКИЕ РЕАКЦИИ
ОБРАТИМЫЕ РЕАКЦИИ :
Обратимые реакции — химические реакции, протекающие одновременно в
ОБРАТИМЫЕ И НЕОБРАТИМЫЕ ХИМИЧЕСКИЕ РЕАКЦИИ
ОБРАТИМЫЕ РЕАКЦИИ :
Обратимые реакции — химические реакции, протекающие одновременно в

двух противоположных направлениях (прямом и обратном), например:
3H2 + N2 ⇆ 2NH3
Направление обратимых реакций зависит от концентраций веществ — участников реакции. По завершении обратимой реакции, т. е. при достижении химического равновесия, система содержит как исходные вещества, так и продукты реакции.
Простая (одностадийная) обратимая реакция состоит из двух происходящих одновременно элементарных реакций, которые отличаются одна от другой лишь направлением химического превращения. Направление доступной непосредственному наблюдению итоговой реакции определяется тем, какая из этих взаимно-обратных реакций имеет большую скорость. Например, простая реакция
N2O4 ⇆ 2NO2
складывается из элементарных реакций
N2O4 ⇆ 2NO2 и 2NO2 ⇆ N2O4
Для обратимости сложной (многостадийной) реакции, необходимо, чтобы были обратимы все составляющие её стадии.
Для обратимых реакций уравнение принято записывать следующим образом А + В АВ.
Две противоположно направленные стрелки указывают на то, что при одних и тех же условиях одновременно протекает как прямая, так и обратная реакция, например
СН3СООН + С2Н5ОН СН3СООС2Н5 + Н2О
3H2 + N2 ⇆ 2NH3
Направление обратимых реакций зависит от концентраций веществ — участников реакции. По завершении обратимой реакции, т. е. при достижении химического равновесия, система содержит как исходные вещества, так и продукты реакции.
Простая (одностадийная) обратимая реакция состоит из двух происходящих одновременно элементарных реакций, которые отличаются одна от другой лишь направлением химического превращения. Направление доступной непосредственному наблюдению итоговой реакции определяется тем, какая из этих взаимно-обратных реакций имеет большую скорость. Например, простая реакция
N2O4 ⇆ 2NO2
складывается из элементарных реакций
N2O4 ⇆ 2NO2 и 2NO2 ⇆ N2O4
Для обратимости сложной (многостадийной) реакции, необходимо, чтобы были обратимы все составляющие её стадии.
Для обратимых реакций уравнение принято записывать следующим образом А + В АВ.
Две противоположно направленные стрелки указывают на то, что при одних и тех же условиях одновременно протекает как прямая, так и обратная реакция, например
СН3СООН + С2Н5ОН СН3СООС2Н5 + Н2О
Слайд 3ПРИМЕР ОБРАТИМОЙ РЕАКЦИИ
ПРИМЕР ОБРАТИМОЙ РЕАКЦИИ

Слайд 4НЕОБРАТИМЫЕ ХИМИЧЕСКИЕ РЕАКЦИИ
Необратимыми называют такие химические процессы, продукты которых не способны реагировать друг
НЕОБРАТИМЫЕ ХИМИЧЕСКИЕ РЕАКЦИИ
Необратимыми называют такие химические процессы, продукты которых не способны реагировать друг

с другом с образованием исходных веществ. Примерами необратимых реакций может служить разложение бертолетовой соли при нагревании
2КСlО3 > 2КСl + ЗО2,
Необратимыми называются такие реакции, при протекании которых:
1) образующиеся продукты уходят из сферы реакции - выпадают в виде осадка, выделяются в виде газа, например
ВаСl2 + Н 2SО 4 = ВаSО4↓ + 2НСl
Na 2CO 3 + 2HCl = 2NaCl + CO2 ↓ + H2O
2) образуется малодиссоциированное соединение, например вода:
НСl + NаОН = Н2О + NаСl
3) реакция сопровождается большим выделением энергии, например горение магния
Mg + 1/2 О2 = МgО, ∆H = -602,5 кДж / моль
2КСlО3 > 2КСl + ЗО2,
Необратимыми называются такие реакции, при протекании которых:
1) образующиеся продукты уходят из сферы реакции - выпадают в виде осадка, выделяются в виде газа, например
ВаСl2 + Н 2SО 4 = ВаSО4↓ + 2НСl
Na 2CO 3 + 2HCl = 2NaCl + CO2 ↓ + H2O
2) образуется малодиссоциированное соединение, например вода:
НСl + NаОН = Н2О + NаСl
3) реакция сопровождается большим выделением энергии, например горение магния
Mg + 1/2 О2 = МgО, ∆H = -602,5 кДж / моль
Слайд 5ПРИМЕР НЕОБРАТИМОЙ РЕАКЦИИ
ПРИМЕР НЕОБРАТИМОЙ РЕАКЦИИ

Следующая -
Как нарисовать сани Деда Мороза Оңай балқитын флюстерді қолдана отырып хромкенді шекемтастар алу мүмкіндігін зерттеу
Оңай балқитын флюстерді қолдана отырып хромкенді шекемтастар алу мүмкіндігін зерттеу Массовая доля вещества в смеси. Таблица
Массовая доля вещества в смеси. Таблица Презентация на тему Полимеры и их получение
Презентация на тему Полимеры и их получение  Новые грани парфюмерии. Задача 5
Новые грани парфюмерии. Задача 5 Метод ТРИЗ (теория решения изобретательских задач) при обучении химии
Метод ТРИЗ (теория решения изобретательских задач) при обучении химии Презентация на тему Многообразие карбоновых кислот
Презентация на тему Многообразие карбоновых кислот  Кислородсодержащие органические соединения
Кислородсодержащие органические соединения Гидрокрекинг
Гидрокрекинг Силикатная промышленность
Силикатная промышленность Презентация на тему Почему протекают химические реакции
Презентация на тему Почему протекают химические реакции  Строение материалов. Дефекты кристаллической структуры
Строение материалов. Дефекты кристаллической структуры ТЭЦ, работающие на каменном угле более экологичны, чем на буром. Факт или вымысел?
ТЭЦ, работающие на каменном угле более экологичны, чем на буром. Факт или вымысел? История органической химии. Урок химии в 10 классе
История органической химии. Урок химии в 10 классе Масляная кислота
Масляная кислота 11 класс 15.09
11 класс 15.09 Белый фосфор
Белый фосфор Оксид цинка ZnO
Оксид цинка ZnO Подготовка газа к транспорту с применением процесса низкотемпературной сепарации
Подготовка газа к транспорту с применением процесса низкотемпературной сепарации Презентация на тему Коррозия
Презентация на тему Коррозия  Презентация на тему Метан и его свойства
Презентация на тему Метан и его свойства  Йод. Положение в периодической системе
Йод. Положение в периодической системе Стеариновая кислота
Стеариновая кислота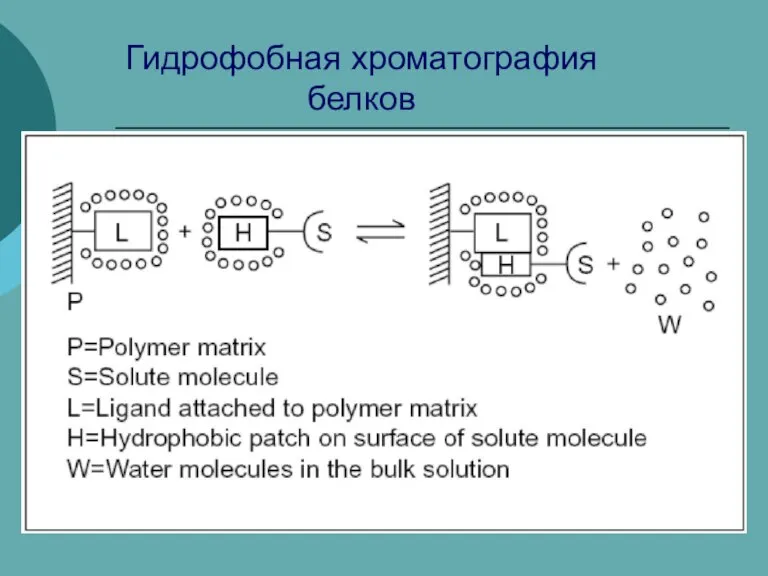 Гидрофобная хроматография белков
Гидрофобная хроматография белков Химическая промышленность. Аварии на химических предприятиях
Химическая промышленность. Аварии на химических предприятиях Цельное молоко: полезно или опасно для здоровья? (сравнительная характеристика качества восстановленного и цельного молока)
Цельное молоко: полезно или опасно для здоровья? (сравнительная характеристика качества восстановленного и цельного молока) Строение вещества. Химическая связь и кристаллическое строение. Урок 1: Ионная и ковалентная связи
Строение вещества. Химическая связь и кристаллическое строение. Урок 1: Ионная и ковалентная связи Химическое равновесие в гомогенных системах
Химическое равновесие в гомогенных системах Способы получения чистых веществ в лаборатории
Способы получения чистых веществ в лаборатории