Содержание
- 2. ВЗАИМОДЕЙСТВИЕ РАСТВОРА ХЛОРИДА ЖЕЛЕЗА (III) С ГИДРОКСИДОМ НАТРИЯ
- 3. 1) ЗАПИСАТЬ УРАВНЕНИЕ РЕАКЦИИИ В МОЛЕКУЛЯРНОЙ ФОРМЕ FeCI3 + 3NaOH = Fe(OH)3 + 3 NaCI 2)
- 4. ПРИЗНАКИ НЕОБРАТИМОСТИ РЕАКЦИЙ ИОННОГО ОБМЕНА ОБРАЗОВАНИЕ ОСАДКА Cu 2++ 2OH- = Cu(OH)2 ОБРАЗОВАНИЕ ГАЗООБРАЗНОГО ВЕЩЕСТВА CO32-
- 5. Получение гидроксида меди (II) I группа: CuCl2 + 2KOH = Cu(OH)2 + 2KCl 2 группа: CuBr2
- 6. Краткое ионное уравнение получения гидроксида меди (II) из растворов солей меди Cu 2++ 2OH- = Cu(OH)2
- 8. Скачать презентацию





 Типы химической связи
Типы химической связи Прикладная геохимия
Прикладная геохимия Чистые вещества и смеси
Чистые вещества и смеси Классификация сложных неорганических веществ. Оксиды
Классификация сложных неорганических веществ. Оксиды Минералы. Сокровища земли. Ко дню геолога
Минералы. Сокровища земли. Ко дню геолога Тест 1 задание
Тест 1 задание Химическое равновесие
Химическое равновесие Презентация на тему Виды химической связи и типы кристаллических решеток
Презентация на тему Виды химической связи и типы кристаллических решеток  Учебное задание Расчет теплоты сгорания
Учебное задание Расчет теплоты сгорания Презентация на тему Полезная химия во фруктах и овощах
Презентация на тему Полезная химия во фруктах и овощах  Донорно-акцепторный механизм образование связи
Донорно-акцепторный механизм образование связи Консультация по химии
Консультация по химии Нефть и продукты ее переработки. Лабораторная работа
Нефть и продукты ее переработки. Лабораторная работа Методы защиты металлов от электрохимической коррозии. Классификация методов защиты
Методы защиты металлов от электрохимической коррозии. Классификация методов защиты Кислотно-основные равновесия
Кислотно-основные равновесия Природный газ
Природный газ Сера
Сера Структура електронної оболонки атома. Енергетичні рівні та підрівні
Структура електронної оболонки атома. Енергетичні рівні та підрівні Генетическая связь между классами неорганических веществ
Генетическая связь между классами неорганических веществ Атомы. Нахождение в природе
Атомы. Нахождение в природе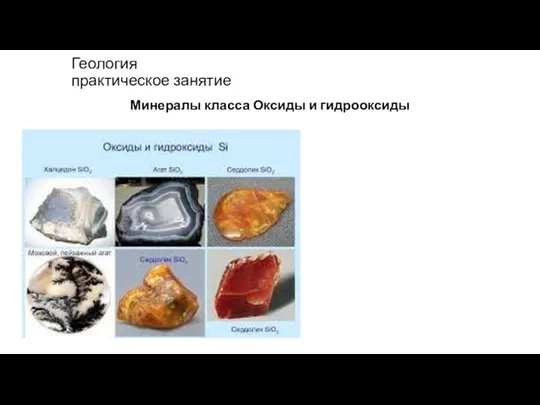 Оксиды и гидрооксиды
Оксиды и гидрооксиды 9-12 Гидролиз солей -
9-12 Гидролиз солей - Презентация на тему Неметаллы
Презентация на тему Неметаллы  Стекло
Стекло Карбоцепные полимеры
Карбоцепные полимеры Полиэтилен. Получение полиэтилена
Полиэтилен. Получение полиэтилена Группа веществ, требующих особых методов изолирования. Характеристика соединений. Токсикологическое значение
Группа веществ, требующих особых методов изолирования. Характеристика соединений. Токсикологическое значение Применение личностно-ориентированного подхода в обучении химии
Применение личностно-ориентированного подхода в обучении химии