Содержание
- 2. Вопросы Кислоты Оксиды Физические и химические свойства солей, применение и получение Основания Определение и классификацию солей
- 3. Соли – сложные вещества, образованные атомами металлов и кислотного остатка Что такое соли? Классификация солей Na3PO4
- 4. Свойства солей Физические свойства Соли - твердые вещества разного цвета. Растворимость их различна. Некоторые хорошо растворимы,
- 5. Химические свойства Соли реагируют с металлами ( исключения активные металлы: Li, Na, K, Ca, Ba -
- 6. Соли реагируют с некоторыми кислотными оксидами: CaCO3 + SiO2 = CaSiO3 + CO2 Соли реагируют с
- 7. Получение солей Взаимодействие металлов и неметаллов: 2Fe + 3Cl2 = 2FeCl3 Взаимодействие кислотных оксидов с основными
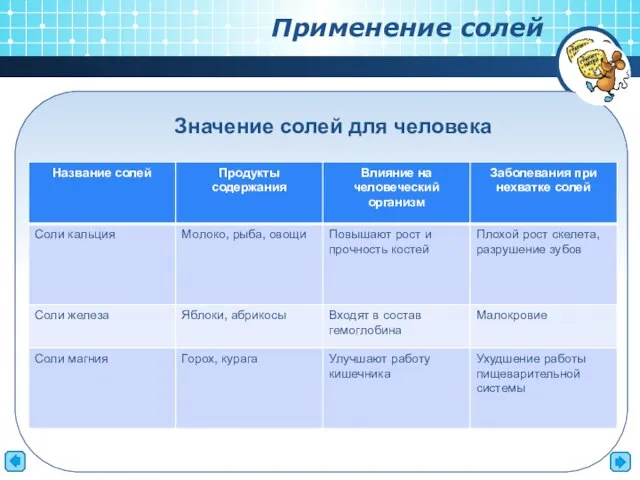
- 8. Применение солей Значение солей для человека
- 9. m =m = 18,8 гm = 18,8 г nm = 18,8 г n m = 18,8
- 10. Дано: Решение: n (CuO) = 0,1 моль CuO + 2HNO3 = Cu(NO3)2 + H2O HNO3 n
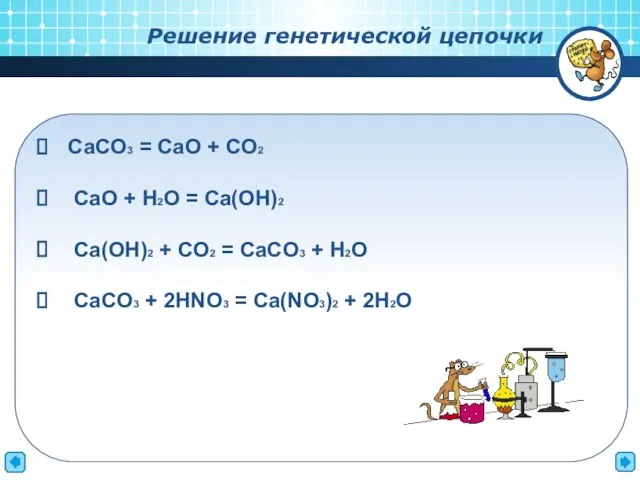
- 11. СaCO3 = CaO + CO2 CaO + H2O = Ca(OH)2 Ca(OH)2 + CO2 = CaCO3 +
- 13. Скачать презентацию







 Азотная кислота
Азотная кислота Окислительно-восстановительные реакции (ОВР)
Окислительно-восстановительные реакции (ОВР) Игра Что? Где? Когда?. Химия
Игра Что? Где? Когда?. Химия Обратимость химических реакций. Химическое равновесие
Обратимость химических реакций. Химическое равновесие Индиго-краситель
Индиго-краситель Растительные источники жиров и жирных масел
Растительные источники жиров и жирных масел Макро- и микромир
Макро- и микромир Коррозия металлов
Коррозия металлов Сказка о братьях карбонатах
Сказка о братьях карбонатах Взаимодействие атомов элементов-неметаллов между собой
Взаимодействие атомов элементов-неметаллов между собой Полиамиды (ПА)
Полиамиды (ПА) Фосфориты. Добыча фосфоритов
Фосфориты. Добыча фосфоритов Способы выражения концентраций растворов
Способы выражения концентраций растворов Кислородсодержащие органические соединения
Кислородсодержащие органические соединения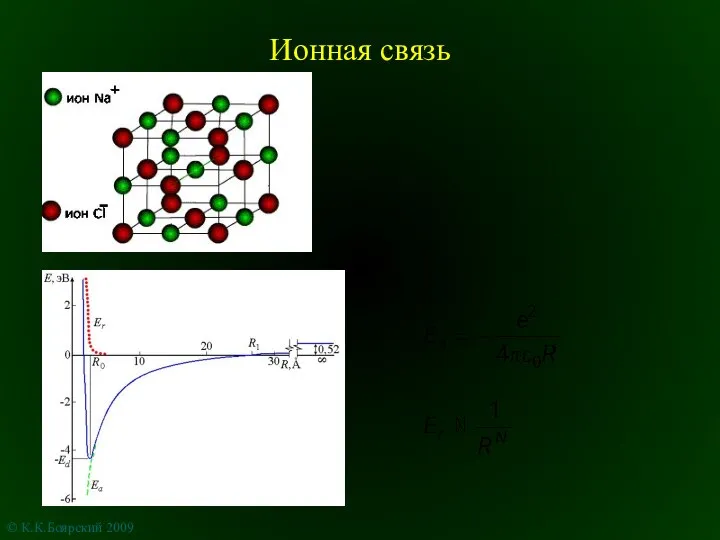 Ионная связь
Ионная связь Оңай балқитын флюстерді қолдана отырып хромкенді шекемтастар алу мүмкіндігін зерттеу
Оңай балқитын флюстерді қолдана отырып хромкенді шекемтастар алу мүмкіндігін зерттеу Карбоновые кислоты, их строение, номенклатура, получение и свойства
Карбоновые кислоты, их строение, номенклатура, получение и свойства Уравнение состояния идеального газа
Уравнение состояния идеального газа Шаблон для презентации по химии
Шаблон для презентации по химии Перициклические реакции
Перициклические реакции Оңай балқитын флюстерді қолдана отырып хромкенді шекемтастар алу мүмкіндігін зерттеу
Оңай балқитын флюстерді қолдана отырып хромкенді шекемтастар алу мүмкіндігін зерттеу Катализ в нефтепереработке
Катализ в нефтепереработке Органические галогениды. (Лекция 7)
Органические галогениды. (Лекция 7) Составление уравнений окислительно-восстановительных реакций
Составление уравнений окислительно-восстановительных реакций Жиры
Жиры Скорость химических реакций
Скорость химических реакций 1666603286718__4v20ts
1666603286718__4v20ts Основы МКТ
Основы МКТ