Содержание
- 2. Повторение Скажите, какие по составу вещества вы знаете? А чем они различаются? Чем различаются сложные вещества
- 3. ВАЛЕНТНОСТЬ Валентность - это свойство атомов химического элемента присоединять определённое число атомов других химических элементов. ВАЛЕНТНОСТЬ
- 4. Составление химических формул по валентности
- 5. 1. Запиши рядом знаки химических элементов, которые входят в состав вещества. Пример: Составить химическую формулу оксида
- 6. 2. Над знаками химических элементов поставь их валентность. Пример: Составить химическую формулу оксида бора. B O
- 7. 3. Определи Н.О.К. чисел выражающих валентность этих элементов. Запиши Н.О.К. в квадратике над формулой. Пример: Составить
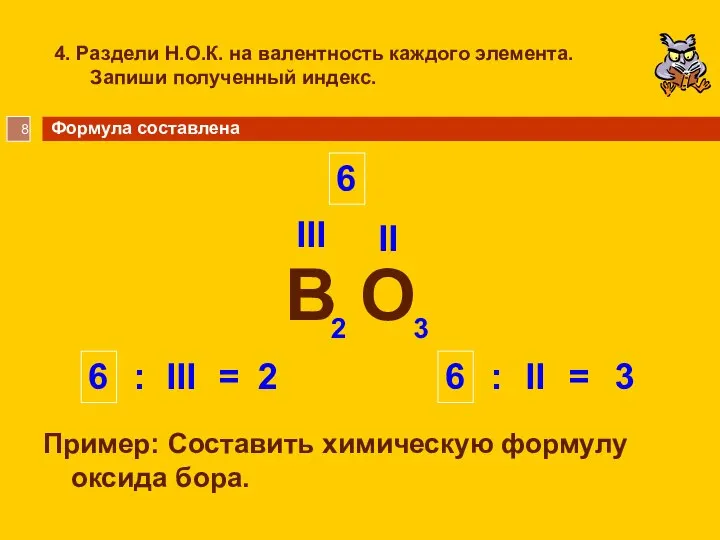
- 8. 4. Раздели Н.О.К. на валентность каждого элемента. Запиши полученный индекс. Пример: Составить химическую формулу оксида бора.
- 9. УПРАЖНЕНИЕ: Составьте химические формулы соединений А) Оксид лития (состоит из атомов лития и кислорода). Б) Оксид
- 10. ВАЛЕНТНОСТЬ Проверка д/з
- 11. ПОВТОРЕНИЕ Дайте определение: что такое валентность? Какие два типа валентности вы знаете? Назовите валентность химических элементов:
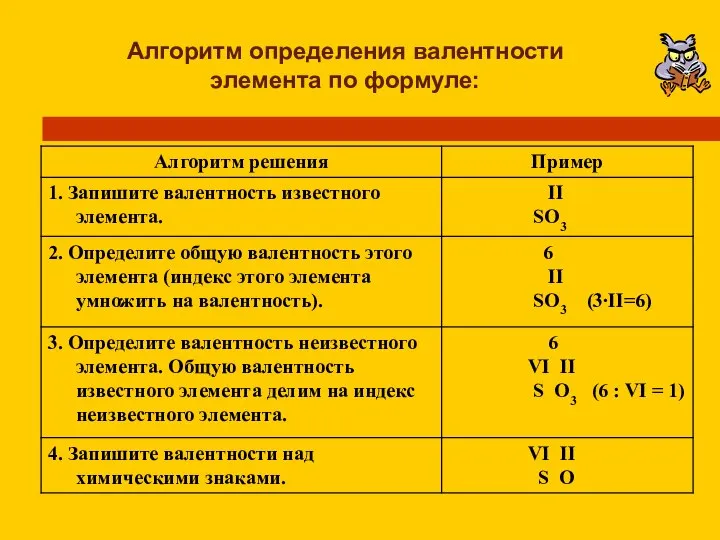
- 12. Алгоритм определения валентности элемента по формуле:
- 13. Al2O3 CaS NaCl AlCl3 P2O5 K2S ZnCl2 HCl Na2O Al2S3
- 14. Правила определения валентности элементов в соединениях 1. Валентность водорода принимают за I. 2. Кислород в своих
- 16. Скачать презентацию











 Вспомни… СаО, SО2, Fе2О3 , Nа2О, Сl2О7
Вспомни… СаО, SО2, Fе2О3 , Nа2О, Сl2О7 Электролиз
Электролиз Химический состав живых организмов. Метаболизм
Химический состав живых организмов. Метаболизм Презентация на тему Законы газового состояния вещества
Презентация на тему Законы газового состояния вещества  Презентация на тему Викторина "Узнай химический элемент"
Презентация на тему Викторина "Узнай химический элемент"  Качественное определение углерода, водорода и хлора в органических соединениях
Качественное определение углерода, водорода и хлора в органических соединениях Презентация на тему Соединения азота
Презентация на тему Соединения азота  Щелочноземельные металлы
Щелочноземельные металлы Презентация по Химии "Стиральные порошки и их экологическое воздействие на окружающую среду"
Презентация по Химии "Стиральные порошки и их экологическое воздействие на окружающую среду"  Органическая химия
Органическая химия Презентация на тему Химический состав клетки. Неорганические соединения
Презентация на тему Химический состав клетки. Неорганические соединения  Введение в химию. История химии
Введение в химию. История химии Предельные углеводороды (алканы)
Предельные углеводороды (алканы) СТЕПЕНЬ ОКИСЛЕНИЯ
СТЕПЕНЬ ОКИСЛЕНИЯ Номенклатура органических соединений. Упражнения
Номенклатура органических соединений. Упражнения Сложные эфиры и жиры
Сложные эфиры и жиры Минералы
Минералы Химические реакции в органической химии
Химические реакции в органической химии Сложные эфиры. Жиры. Мыла
Сложные эфиры. Жиры. Мыла 9-12 Гидролиз солей -
9-12 Гидролиз солей - Свойства растворителей
Свойства растворителей Идентификация Бензойной кислоты
Идентификация Бензойной кислоты Кислоты, их классификация и свойства
Кислоты, их классификация и свойства Предельные углеводороды (алканы)
Предельные углеводороды (алканы) 20140111_mineraly
20140111_mineraly Хімія у вирішенні промислової проблеми
Хімія у вирішенні промислової проблеми Небезпечні речовини
Небезпечні речовини Спирты. Классификация
Спирты. Классификация