Содержание
- 2. Цель урока: сформировать представления о валентности как свойстве атомов одного элемента присоединять, или замещать определённое число
- 3. Сравните качественный и количественный состав в молекулах: HCl, H2O, NH3, CH4. – Что общего в составе
- 4. Валентность - свойство атомов одного элемента присоединять к себе определенное число атомов другого элемента
- 5. – В начале XIX века Дж. Дальтоном был сформулирован закон кратных отношений, из которого следовало, что
- 6. Валентность обозначается римскими цифрами. I I I II III I IV I НCl H2O NH3 CH4
- 7. Переменная и постоянная валентность Есть элементы, которые имеют постоянную валентность: H, Li, Na, К, Rb, Cs,
- 8. Элементы с переменной валентностью Cu, Hg I,II Fe, Co, Ni II, III Sn, Pb, C II,
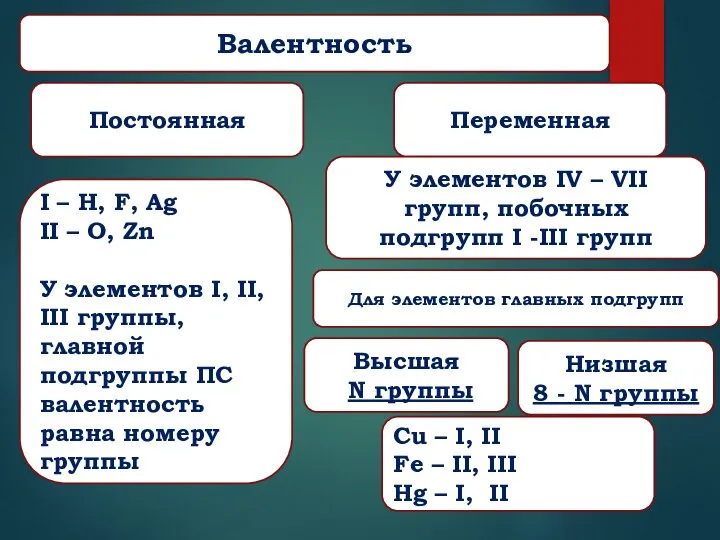
- 9. Валентность Постоянная Переменная I – H, F, Ag II – O, Zn У элементов I, II,
- 10. Алгоритм определения валентности элемента по формуле вещества: 1. над символами химических элементов с постоянной валентностью надписать
- 11. Определите валентность элементов в веществах SiH4, CrO3, H2S, CO2, CO, SO3, SO2, Fe2O3, FeO, HCl, HBr,
- 12. «Крестики-нолики» Выигрышный путь: одновалентные металлы. Выигрышный путь: трёхвалентные металлы.
- 13. Составление химических формул по валентности
- 14. 1 1. Запиши рядом знаки химических элементов, которые входят в состав вещества. Пример: Составить химическую формулу
- 15. 2. Над знаками химических элементов поставь их валентность. Пример: Составить химическую формулу оксида бора. B O
- 16. 3 3. Определи Н.О.К. чисел выражающих валентность этих элементов. Запиши Н.О.К. в квадратике над формулой. Пример:
- 17. 4 4. Раздели Н.О.К. на валентность каждого элемента. Запиши полученный индекс. Пример: Составить химическую формулу оксида
- 18. Выполнить одно из трёх заданий по выбору. Выбирайте только то задание, с которым вы справитесь. Репродуктивный
- 19. Классная работа: проработать презентацию, составить опорный конспект, выучить (слайд 7, 8, 9). Домашняя работа: выполнить письменное
- 21. Скачать презентацию

















 Щелочноземельные металлы
Щелочноземельные металлы Адамсит. Дигидрофенарсазинхлорид HN(C6H4)2AsCl
Адамсит. Дигидрофенарсазинхлорид HN(C6H4)2AsCl Основы материаловедения. Раздел 1
Основы материаловедения. Раздел 1 Природные смолы: канифоль, янтарь, сандарак (2)
Природные смолы: канифоль, янтарь, сандарак (2) Алгоритм названия органического соединения
Алгоритм названия органического соединения Сталь 12Х18Н10Т
Сталь 12Х18Н10Т Презентация на тему Подгруппа углерода и азота
Презентация на тему Подгруппа углерода и азота  3 Серная кислота
3 Серная кислота Калий. Общая информация
Калий. Общая информация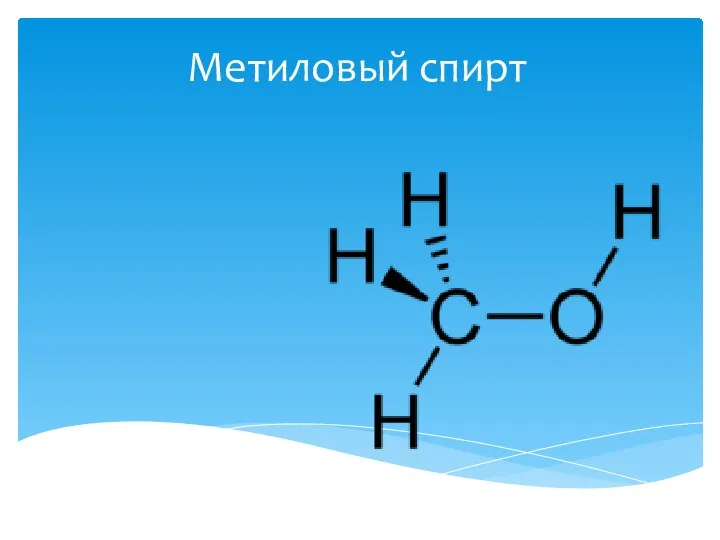 Метиловый спирт
Метиловый спирт Дисперсные системы
Дисперсные системы Свойства металлов. Лекция №8
Свойства металлов. Лекция №8 Использование ИКТ в преподавании химии
Использование ИКТ в преподавании химии Методы повышения надежности. Резервирование сложных ХТС
Методы повышения надежности. Резервирование сложных ХТС Disinfection without Chlorine and Chemistry
Disinfection without Chlorine and Chemistry Презентация на тему Медь
Презентация на тему Медь  Применение солей
Применение солей Презентация на тему Растворение. Растворы (8 класс)
Презентация на тему Растворение. Растворы (8 класс)  Презентация на тему Производство аммиака
Презентация на тему Производство аммиака  Положение металлов в периодической системе Д.И. Менделеева. Физические свойства металлов
Положение металлов в периодической системе Д.И. Менделеева. Физические свойства металлов Химические свойства амфотерных оксидов и гидроксидов
Химические свойства амфотерных оксидов и гидроксидов Презентация на тему Кислород (9 класс)
Презентация на тему Кислород (9 класс)  gidroliz_soley (1)
gidroliz_soley (1) Гидролиз. Виды гидролиза
Гидролиз. Виды гидролиза Изучаем химию с Агатой Кристи
Изучаем химию с Агатой Кристи Презентация на тему Альдегиды и их свойства
Презентация на тему Альдегиды и их свойства 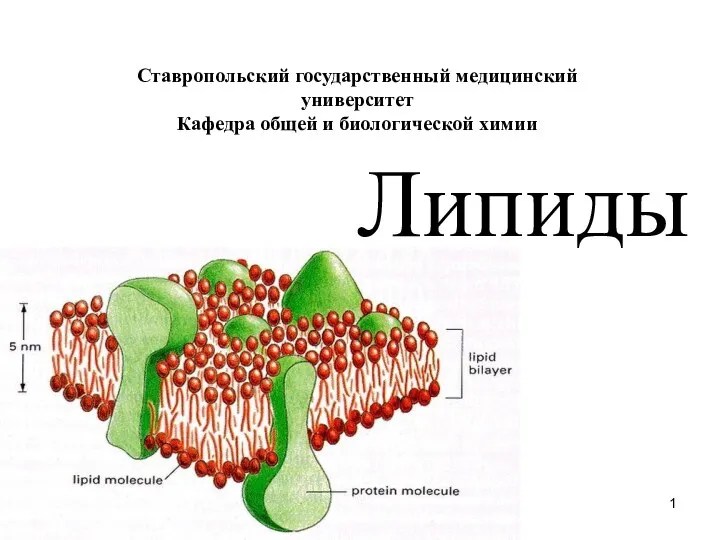 Липиды
Липиды Алюминий
Алюминий