Содержание
- 2. Зачем фармацевту информация об особенностях дженериков? Исключение претензий со стороны потребителей после приобретения ими в аптеке
- 3. Особенности национальной любви к дженерикам Недостаточная осведомленность населения в области фармакологии и фармакотерапии Низкий уровень разъяснительной
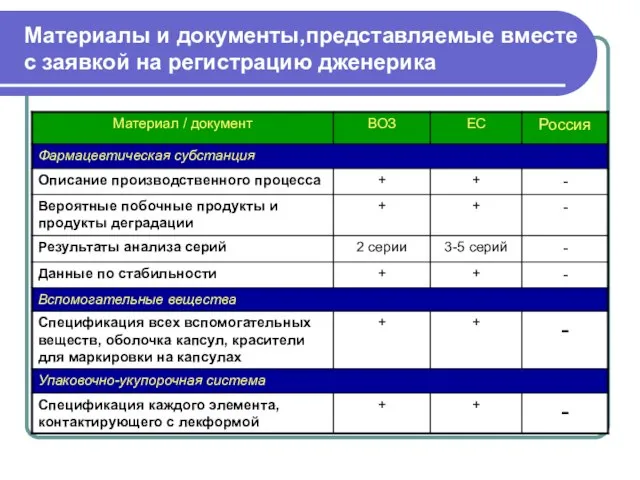
- 4. Материалы и документы,представляемые вместе с заявкой на регистрацию дженерика
- 5. «Засилие» дженериков В Российской Федерации зарегистрировано более 17 000 наименований лекарственных препаратов 78% из них являются
- 6. Примеры сравнения брэндов и дженериков Амлодипин и норваск Амиодарон и кордарон Ренитек и энам Козаар и
- 7. Оригинальный препарат Original (англ.) – первый, новый, истинный, прежде неизвестный, предшествующий, исходный… Новый препарат, произведенный на
- 8. Дженерик Generic (англ.) – общий, родовой, групповой Дже́нерик (иногда — генерик, женерик) —лекарственное средство, которое выпускается
- 9. Критерии сравнения Дженерик содержит то же активное лекарственное вещество (субстанцию), что и оригинальный (патентованный) препарат. Дженерик
- 10. Эквивалентность брэндов и дженериков (требования FDA) Фармацевтически эквивалентные лекарственные препараты содержат одинаковые активные ингредиенты в одинаковой
- 11. Фармацевтическая эквивалентность Фармацевтически эквивалентные лекарственные препараты содержат одинаковые активные ингредиенты в одинаковой лекарственной форме, предназначены для
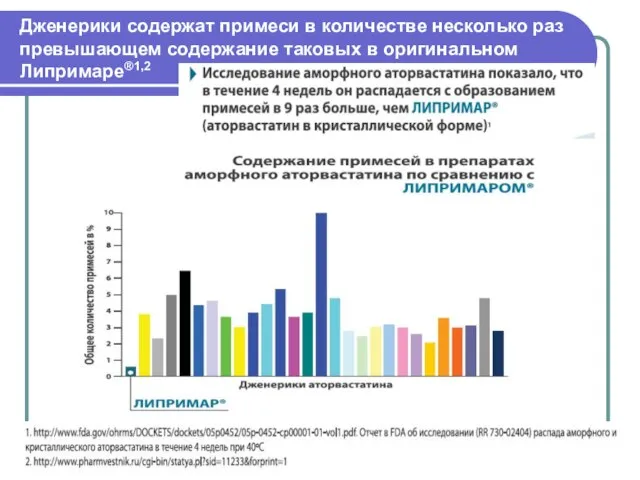
- 12. Дженерики содержат примеси в количестве несколько раз превышающем содержание таковых в оригинальном Липримаре®1,2
- 13. Electronic Orange Book – результаты поиска Периндаприл (Perindapril)– не зарегистрирован Аторвастатин – кодуэт, липитор (PFIZER) Квинаприл
- 14. Рекомендации ВОЗ в отношении биоэквивалентности Биоэквивалентность дженерика следует определять по отношению к оригинальному лекарственному препарату. Если
- 15. Терапевтическая эквивалентность Терапевтически эквивалентными лекарственные препараты могут считаться только в том случае, если они фармацевтически эквивалентны
- 16. Мнение специалиста Марцевич Сергей Юрьевич Профессор, доктор медицинских наук. Профессор кафедры доказательной медицины ФДПОП ММА им
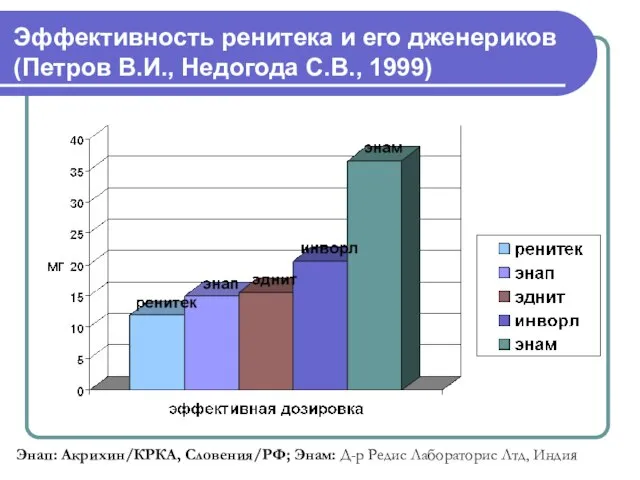
- 17. Эффективность ренитека и его дженериков (Петров В.И., Недогода С.В., 1999) Энап: Акрихин/КРКА, Словения/РФ; Энам: Д-р Редис
- 18. Дженерики: преимущества и недостатки Таблиц взаимозаменяемости дженерических препаратов в РФ не существует. В Интернете можно воспользоваться
- 19. Electronic Orange Book Approved Drug Products with Therapeutic Equivalence Evaluations Current through December 2008** ** In
- 20. Сравнение терапевтической эффективности липримара и его дженериков Эффективная дозировка – от 20 мг/сут Скорость наступления клинических
- 21. при принятии врачом решения о переводе пациента с оригинального препарата на генерический у 2/3 больных возникали
- 22. Мнение Association of American Physicians (основана в 1885 г.) Американская ассоциация врачей не рекомендует в качестве
- 23. Особенности отечественного амлодипина Компания «Pfizer» не передавала лицензию на производство и распространение «Норваска» Действие глобального патента
- 24. Особенности дженериков аторвастатина Компания «Pfizer» не передавала лицензию на производство и распространение «Липримара» Глобальный патент на
- 25. Что общего между ЛИПРИМАРОМ® и его дженериками? Что общего между алмазом и углем?
- 26. Почему все-таки Оригинальный препарат? Оригинальный препарат: Стабильность физико-химических свойств действующего вещества Высококачественные наполнители и оболочка Доказательства
- 27. Спасибо за внимание.
- 28. Е.М. Тареев «Для того, чтобы в наш век лечиться, нужно иметь хорошее здоровье!» Академик Академии медицинских
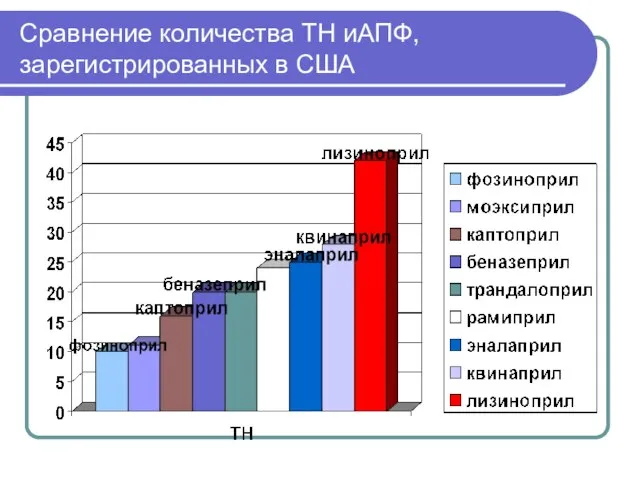
- 29. иАПФ, зарегистрированные в США (результаты поиска в Electronic Orange Book по “…pril” Беназеприл - 20 Каптоприл
- 30. Сравнение количества ТН иАПФ, зарегистрированных в США
- 32. Скачать презентацию

























 Болезни, связанные с нехваткой химических элементов
Болезни, связанные с нехваткой химических элементов Мемристорный протез функционального отдела спинного мозга. Исследовательский проект
Мемристорный протез функционального отдела спинного мозга. Исследовательский проект Квест – игра, посвящённая всемирному дню борьбы со спидом Предупреждён - вооружён
Квест – игра, посвящённая всемирному дню борьбы со спидом Предупреждён - вооружён Оценка эффективности применения шелка по сравнению с викрилом для закрытия срединных брюшных разрезов
Оценка эффективности применения шелка по сравнению с викрилом для закрытия срединных брюшных разрезов ІХС: Інфаркт міокарда
ІХС: Інфаркт міокарда Доврачебная помощь при клинической смерти
Доврачебная помощь при клинической смерти Medical concern of a shoulder pain
Medical concern of a shoulder pain Гнойный бурсит
Гнойный бурсит Школа здоровья для беременных. Что произошло в моём организме? Лекция 2
Школа здоровья для беременных. Что произошло в моём организме? Лекция 2 Известные дерматологические школы мира и их вклад в развитие дисциплины
Известные дерматологические школы мира и их вклад в развитие дисциплины Высокомощностная брахитерапия в комплексном лечении раннего рака молочной железы
Высокомощностная брахитерапия в комплексном лечении раннего рака молочной железы Хирургическая обработка гнойного очага при оказании специализированной помощи в условиях мирного времени
Хирургическая обработка гнойного очага при оказании специализированной помощи в условиях мирного времени Мифы о здоровом образе жизни
Мифы о здоровом образе жизни Язва желудка. Язва двенадцатиперстной кишки
Язва желудка. Язва двенадцатиперстной кишки Лучевые поражения животных
Лучевые поражения животных Аллергические заболевания и их профилактика
Аллергические заболевания и их профилактика Сахарный диабет
Сахарный диабет Корь. Эпидемиология
Корь. Эпидемиология Перемещение больного
Перемещение больного Хвороби кролів
Хвороби кролів Методы исследования восприятия
Методы исследования восприятия Профилактика коронавируса
Профилактика коронавируса Умей предупреждать болезни
Умей предупреждать болезни Стоматологический препарат Сафорайд. Занятие 2
Стоматологический препарат Сафорайд. Занятие 2 ЗОЖ. Проблема здоровья дошкольников
ЗОЖ. Проблема здоровья дошкольников Проект памяти врачей-героев, погибших от коронавируса
Проект памяти врачей-героев, погибших от коронавируса Анатомия и физиология сердца (лекция 4)
Анатомия и физиология сердца (лекция 4) Организация обучения курсу БЖД на время карантина
Организация обучения курсу БЖД на время карантина