Содержание
- 3. Проблемы по безопасности при применении лекарственных препаратов, когда пациенту может быть причинен вред: побочное действие; нежелательная
- 4. Нежелательная реакция - непреднамеренная неблагоприятная реакция организма, связанная с применением лекарственного препарата и предполагающая взаимосвязи с
- 5. Критические моменты проблемы по безопасности лекарственного препарата Информация, требующая срочного предоставления в регуляторный орган: Серьезные нежелательные
- 7. Проблемы по безопасности применения лекарственного препарата. Непредвиденная нежелательная реакция - нежелательная реакция, характер, степень тяжести или
- 8. Отсутствие терапевтической эффективности лекарственного препарата – отсутствие эффективности ЛП по показанию, заявленному в инструкции по медицинскому
- 9. Непредвиденные проблемы по безопасности: Микробная контаминация препарата Проблемы по безопасности применения лекарственного препарата.
- 10. Способ получения информации по безопасности препарата. Электронная почта: [email protected]; Телефон; Факс.
- 11. Информирование по безопасности Согласно внутренней НД: - СОП-РО-054 «Работа с рекламациями на готовую продукцию» - СОП-ФН-002
- 12. СОП-РО-054 «Работа с рекламациями на готовую продукцию»
- 13. СОП-ФН-002 «Мониторинг данных по фармаконадзору» 5.4 Действия инженера по качеству ООК Инженер по качеству ООК: 5.4.1
- 14. Информация по безопасности Требуемая информация для работы с претензией о проблеме по безопасности: Источник сообщения: электронная
- 15. Необходимость сбора данных по безопасности лекарственного препарата Статья 64. Фармаконадзор (61-ФЗ (ред. от 13.07.2020 г.) «Об
- 16. Необходимость сбора данных по безопасности лекарственного препарата Федеральный закон от 12.04.2010 № 61-ФЗ (ред. от 13.07.2020)
- 17. Необходимость сбора данных по безопасности лекарственного препарата КоАП Статья 19.7.8. Непредставление сведений или представление заведомо недостоверных
- 18. Уголовный кодекс РФ Статья 237. Сокрытие информации об обстоятельствах, создающих опасность для жизни или здоровья людей
- 19. Информирование регуляторного органа Росздравнадзор оповещается через заполнение извещения о нежелательной реакции или отсутствия терапевтической эффективности
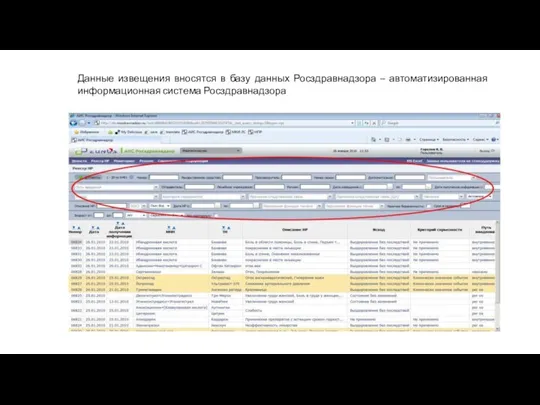
- 20. Данные извещения вносятся в базу данных Росздравнадзора – автоматизированная информационная система Росздравнадзора
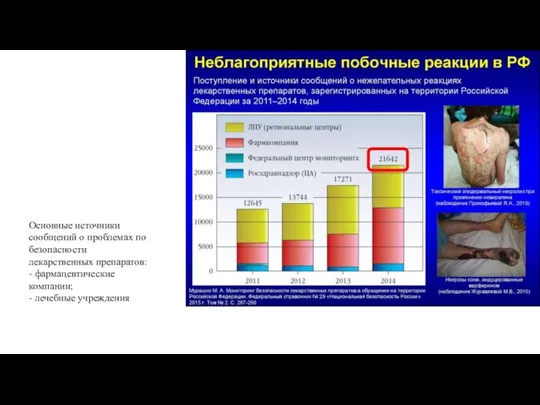
- 21. Основные источники сообщений о проблемах по безопасности лекарственных препаратов: - фармацевтические компании; - лечебные учреждения
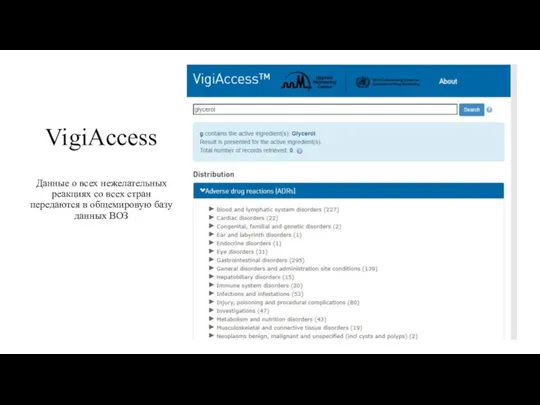
- 22. VigiАccess Данные о всех нежелательных реакциях со всех стран передаются в общемировую базу данных ВОЗ
- 24. Скачать презентацию

















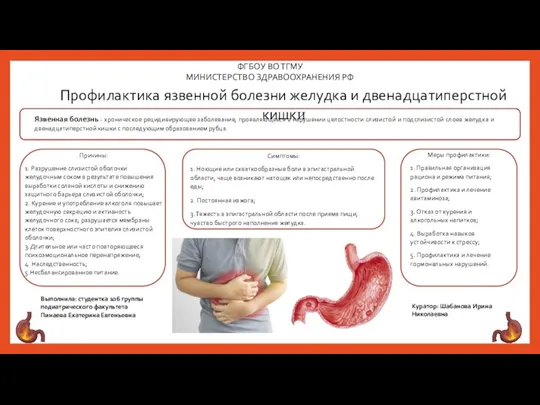 Профилактика язвенной болезни желудка и двенадцатиперстной кишки
Профилактика язвенной болезни желудка и двенадцатиперстной кишки Аортальный стеноз
Аортальный стеноз Европейские рекомендации 2017 (1)
Европейские рекомендации 2017 (1) Спиральды мүше. Жарғақты лабиринттің вестибулярлы бөлігі
Спиральды мүше. Жарғақты лабиринттің вестибулярлы бөлігі Предмет и задачи фармакологии
Предмет и задачи фармакологии Анатомия и физиология гортани. Острые и хронические ларингиты. Новообразования гортани
Анатомия и физиология гортани. Острые и хронические ларингиты. Новообразования гортани Стоматолгиялық науқастарды функционалды зерттеу әдістері
Стоматолгиялық науқастарды функционалды зерттеу әдістері Үймереттердің ішкі канализация жүйес.і Ішкі канализация жүйесінің негізгі элементтері
Үймереттердің ішкі канализация жүйес.і Ішкі канализация жүйесінің негізгі элементтері Узлы в хирургии. Виды швов
Узлы в хирургии. Виды швов Решение для измерения температуры тела от Dahua
Решение для измерения температуры тела от Dahua Алкоголизм и его влияние на развитие здоровой личности
Алкоголизм и его влияние на развитие здоровой личности Йодирование соли
Йодирование соли Методы закаливания
Методы закаливания Ультразвуковая диагностика заболеваний молочной железы
Ультразвуковая диагностика заболеваний молочной железы Микробиология, вирусология және иммунология
Микробиология, вирусология және иммунология Врождённый сифилис
Врождённый сифилис Systane Family New Look. Семейство Систейн
Systane Family New Look. Семейство Систейн Выбор оптимального НПВП при сильной боли. Клинический разбор
Выбор оптимального НПВП при сильной боли. Клинический разбор Основы лечебной физкультуры, особенности применения у больных стоматологического профиля
Основы лечебной физкультуры, особенности применения у больных стоматологического профиля Пневмония
Пневмония Лейкотомия (лоботомия)
Лейкотомия (лоботомия) Туберкулез органов грудной клетки на фоне ВИЧ-инфекции Рентгеносемиотика туберкулеза ОГК
Туберкулез органов грудной клетки на фоне ВИЧ-инфекции Рентгеносемиотика туберкулеза ОГК Выписка рецептов на очки
Выписка рецептов на очки Ветряная оспа
Ветряная оспа Исследование ассортимента и потребительских предпочтений лекарственных препаратов на основе амброксола
Исследование ассортимента и потребительских предпочтений лекарственных препаратов на основе амброксола Периодическая аккредитация для специалистов со средним медицинскими фармацевтическим образованием 2021 года
Периодическая аккредитация для специалистов со средним медицинскими фармацевтическим образованием 2021 года Бронхиальная астма
Бронхиальная астма Порядок морфологического исследования простаты
Порядок морфологического исследования простаты