и содержащий перечень показателей качества и (или) методов контроля качества конкретной лекарственной формы, лекарственного растительного сырья, описания биологических, биохимических, микробиологических, физико-химических, физических, химических и других методов анализа лекарственного средства, а также требования к используемым в целях проведения данного анализа реактивам, титрованным растворам, индикаторам
Фармакопейная статья - документ, утвержденный уполномоченным федеральным органом исполнительной власти и содержащий перечень показателей качества и методов контроля качества лекарственного средства






 Приемы массажа
Приемы массажа хрящевая ткань
хрящевая ткань Сестринский уход за пациентами с термическими ожогами у взрослых
Сестринский уход за пациентами с термическими ожогами у взрослых Волчанка. Системная красная волчанка
Волчанка. Системная красная волчанка Зарядка для глаз
Зарядка для глаз Детский аутизм. Причины и механизмы раннего детского возраста
Детский аутизм. Причины и механизмы раннего детского возраста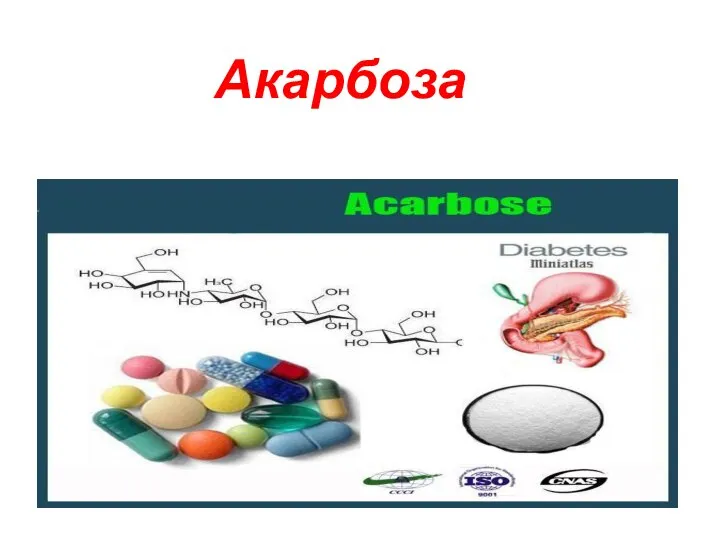 Акарбоза (торговое название Глюкобай)
Акарбоза (торговое название Глюкобай) гем. лихорадки
гем. лихорадки Афазии
Афазии Профессиональные заболевания и их профилактика в профессии парикмахер
Профессиональные заболевания и их профилактика в профессии парикмахер Тонометрия. Внутриглазное давление
Тонометрия. Внутриглазное давление Строение счётной камеры Горяева
Строение счётной камеры Горяева Тархины цочмог харвалт
Тархины цочмог харвалт Теория о роли грибка кандиды в возникновении злокачественных опухолей
Теория о роли грибка кандиды в возникновении злокачественных опухолей Дыхание. Рак лёгких
Дыхание. Рак лёгких Технологии логопедического воздействия при дислалии
Технологии логопедического воздействия при дислалии Органы кроветворения
Органы кроветворения Герпесвирус
Герпесвирус Коррекция и развитие детей с нарушениями опорно-двигательного аппарата
Коррекция и развитие детей с нарушениями опорно-двигательного аппарата Щитовидная железа
Щитовидная железа Хейлопластикаға көрсеткіш,реабилитация, диспансеризация
Хейлопластикаға көрсеткіш,реабилитация, диспансеризация Анафилактический шок
Анафилактический шок Антиадренергические средства
Антиадренергические средства Паралич мягкого нёба
Паралич мягкого нёба «Нормоген» – противоопухолевый препарат будущего
«Нормоген» – противоопухолевый препарат будущего Гебоидная шизофрения
Гебоидная шизофрения Onconetix. Таргетная панель для подбора эффективной терапии с учетом генетических особенностей опухоли
Onconetix. Таргетная панель для подбора эффективной терапии с учетом генетических особенностей опухоли Лечебно-диагностический процесс и сестринская деятельность при хроническом гепатите и циррозе печени
Лечебно-диагностический процесс и сестринская деятельность при хроническом гепатите и циррозе печени