Слайд 2Цель занятия:
выявление полового хроматина
*в ядрах соматических клеток человека:
- слизистой буккального

эпителия;
- нейтрофилов крови;
*решение генетических задач;
*скрининг-тесты для генных наследственных обменных болезней человека.
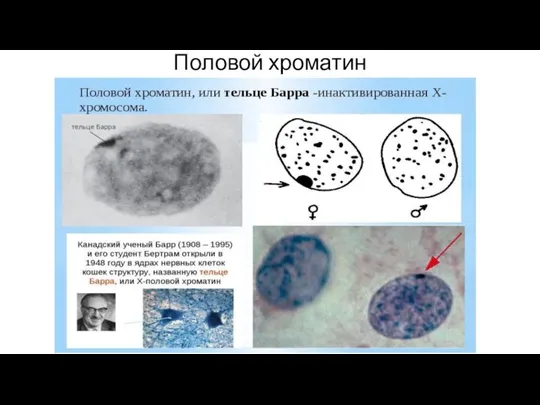
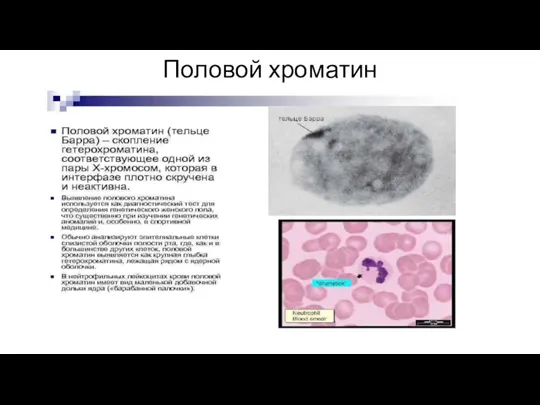
Слайд 3Половой хроматин (тельце Барра) — материал генетически инактивированной X-хромосомы,
в норме выявляемый

только в соматических (диплоидных) клетках женщин с кариотипом 46ХХ.
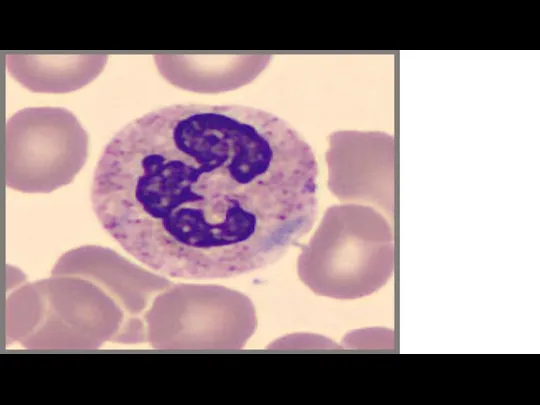
В гранулоцитах половой хроматин выглядит как «барабанная палочка».
Число Х-хромосом у индивида равно числу телец полового хроматина плюс один.
Слайд 4В клетках различных тканей (в различных популяциях) половой хроматин выявляется с неодинаковой

частотой: 80—90 % нервных клеток содержат половой хроматин,
тогда как в клетках буккального эпителия половой хроматин обнаруживается со средней частотой 20—40 %.
Слайд 5Половой хроматин локализуется в ядре, чаще всего прилегая к ядерной оболочке, с

которой он связан тонкими нитями.
Реже он располагается около ядрышка или в середине ядра.
Если половой хроматин прилегает изнутри к ядерной оболочке, он имеет форму треугольника, с вершиной, направленной в сторону центра ядра, или имеет полусферическую форму.
Слайд 6Все организмы, в кариотипе которых
имеются две Х-хромосомы,
содержат одно тельце полового

хроматина.
При трисомии по Х-хромосоме в ядрах клеток содержится по два тельца полового хроматина.
Существует обратная зависимость между пролиферативной активностью клеточной популяции и частотой встречаемости телец полового хроматина.
Слайд 7Объекты исследования Х-хроматина — клетки буккального эпителия, эпителиальные клетки мочевого осадка, нейтрофилы

крови и др.
В онтогенезе половой хроматин появляется рано, до того, как у эмбриона закладываются гонады.
Слайд 8Изучение полового хроматина используется для верификации хромосомного пола (1),
диагностики хромосомных аберраций

по половым хромосомам (2),
для ориентировочного прогноза
пролиферативной активности опухолей (3).
Слайд 9На 5—6-й день эмбрионального развития сначала в клетках трофоэктодермы, затем — в

других частях зародыша осуществляется инактивация одной из каждых двух гомологичных хромосом,
включая и одну из двух Х-хромосом у зародышей женского пола.
Слайд 10Механизм этого явления связан с метилированием ДНК инактивируемой хромосомы.
Специальный участок Xq27.3

на Х-хромосоме («островок CpG») содержит множественные цитозин-гуаниновые повторы, которые в геноме эукариот могут метилироваться.
Так, они полностью метилированы в тельце Барра и не метилированы (активны) в единственной мужской Х-хромосоме, как и в активной женской.
Слайд 11
У человека развитие мужского пола предопределено наличием Y-хромосомы.
В присутствии любого количества

Х-хромосом одной Y-хромосомы достаточно для формирования организма по мужскому типу.
Слайд 12Ген SRY, находящийся в Y-хромосоме, срабатывает на 6—7-й неделе эмбриогенеза,
запуская в

действие ряд генов, локализованных в других хромосомах и обеспечивающих программу синтеза тестостерона.
Фетальный тестостерон направляет развитие зародыша по мужскому типу.
Слайд 13
Продукция тестостерона и антимюллерова ингибирующего пептида в гонадах плода
предопределяет
(2—3-й месяц

эмбриогенеза) формирование внутренних половых органов по мужскому типу.
Слайд 14 Метаболит андрогенов
(5-альфа-дигидротестостерон),
не конвертируемый в эстрогены,
контролирует маскулинный тип формирования

наружных гениталий на 3—4-м месяце фетогенеза (соматический пол).
Часть тестостерона плода метаболизирует в эстрогены.
Слайд 15При наличии Y-хромосомы и высокой продукции тестостерона
обеспечивается высокое содержание метаболитов эстрогенов,

подавляющих формирование обратной связи между продукцией лютеинизирующего гормона (ЛГ) и эстрогенов в развивающемся мозге.
Слайд 16Это ведет к установлению мужского нециклического типа гипоталамо-гипофизарной регуляции половых функций
и

обеспечивает на 4—6-м месяце фетогенеза
мужской тип дифференцировки головного мозга,
что лежит в основе нейропсихической маскулинизации в последующей жизни.
Слайд 17Созревание центров секреции гонадотропинов идет под контролем эстрогенов, полученных из тестостерона,
а

центров, определяющих половое влечение, — под совместным контролем андрогенов и их ароматических эстрогенных производных.
Центры, ответственные за поддержание поведения,
соответствующего избранной половой роли,
у мужчин организуются под влиянием
только андрогенов.
Слайд 18При отсутствии гена SRY, даже если кариотип 46ХХ, а не 45X0 (синдром

Шерешевского — Тернера),
описанные события не происходят,
и
формируется
соматический и психический
женский тип.
Слайд 19Под наследственными понимают заболевания с
первичными техническими дефектами в программном аппарате клеток,

передаваемые
по наследству через гаметы.
Слайд 20Моногенные наследственные заболевания контролируются одним геном и поэтому наследуются в соответствии с

законами Менделя (например, гемофилия А).
Полигенные наследственные болезни контролируются суммарным эффектом нескольких генов, расположенных в разных частях генома и имеющих неодинаковые свойства.
Слайд 21Полигенные наследственные болезни наследуются по
аддитиво-полигенному типу, как правило, с пороговым эффектом

по воздействию того или иного лимитирующего фактора внешней среды (например, сахарный диабет).
Слайд 22Важно помнить, что мутации, хотя и лежат в основе патогенеза наследственных болезней,

но не тождественны самому понятию «наследственная болезнь».
Для возникновения наследственных болезней -как и для возникновения других заболеваний - необходимо действие причинных факторов и существенно влияние условий и реактивности организма.
Слайд 23Работа 1.
Определение полового хроматина в соскобе
со слизистой полости рта

Слайд 24Перед взятием соскоба со слизистой щеки несколько раз зубами сжать слизистую, затем

проглотить слюну и шпателем сделать соскоб с данного места слизистой щеки.
Полученный материал перенести на предметное стекло и размазать по стеклу.
Слайд 25Не давая материалу подсохнуть, наносят на мазок 1—2 капли 1 % уксуснокислого

орсеина.
При отсутствии орсеина окраску можно производить 0,2—0,5 % раствором толуидиновой
(или метиленовой) синьки или азура 1, имеющими рН 4,5—4,7.
Слайд 26Через 1—2 мин на мазок накладывается покровное стекло, а поверх него —

кусочек фильтровальной бумаги, сложенной в 4 раза. Большим пальцем прижимают фильтровальную бумагу и покровное стекло к предметному стеклу.
Таким образом достигается равномерное распределения клеток эпителия в один слой.
Слайд 28Слева: клетки буккального эпителия. Красная стрелка указывает на глыбку полового хроматина (тельце
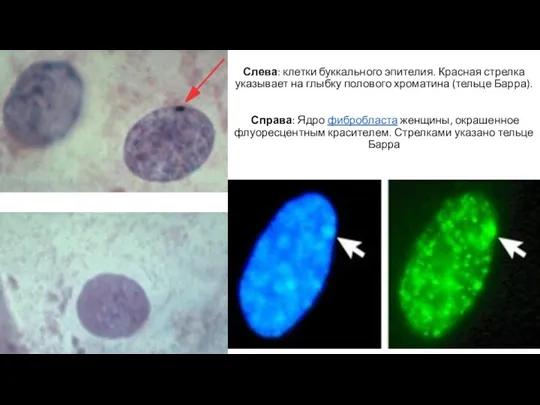
Барра).
Справа: Ядро фибробласта женщины, окрашенное флуоресцентным красителем. Стрелками указано тельце Барра
Слайд 29Работа 2. Нахождение Х-хроматина в нейтрофилах крови человека
Окрашенный мазок крови просматривают под

иммерсионным увеличением, внимательно изучают сегментоядерные нейтрофилы и отыскивают 100 нейтрофилов, отмечая количество клеток, содержащих Х-хроматин — «барабанные палочки».
В протоколе:
а) нарисовать нейтрофилы, содержащие Х-хроматин («барабанные палочки»);
б) подсчитать частоту встречаемости нейтрофилов,
содержащих «барабанные палочки».
Слайд 32
Ход анализа полового хроматина:
1. Получение клеточного материала.
Источник – разнообразные ткани, но

предпочтительны те, что не нужно культивировать in vitro.
Для определения Х-хроматина у взрослого человека используют чаще всего мазки со слизистой оболочки щеки, реже слизистой оболочки влагалища, а также клетки волосяных фолликулов.
Перинатальная диагностика проходит с использованием амниотических клеток.
Для определения численности У-хроматина используется перечисленные ткани, а также сперматозоиды и культивируемые лимфоциты.
В целом для анализа Х-хроматина и У-хроматина идеально подходят однослойные культуры клеток, обычно фибробластов.
Слайд 332. Фиксация препаратов раствором метанола или смесью этанола и уксусной кислоты (3:1)

или исключительно этанолом.
3. Дегидратация путем переноса (ТОЛЬКО для анализа телец Барра) препарата из одного раствора в другой с выдержкой в каждом в течение 5 минут: в спирте 70°, в спирте 50°, в дистиллированной воде I, в дистиллированной воде II.
4. Гидролиз (ТОЛЬКО для анализа телец Барра) в НСl (необязательно).
Слайд 345. Окрашивание полового хроматина.
Методы окраски X- и Y-хроматина различны. Х -

хроматин окрашивается препаратами на основе нефлюоресцирующих красителей: основной фуксин, тионин, ацетоорсеин, толуидиновый синий и др. У – хроматин окрашивается флюорохромами — производными акридинового оранжевого: акрихином, акрихин-ипритом, акрихин-пропилом.
Препараты выдерживаются в краситиле от 30 минут до 12 часов.
Препараты Х-хроматина высушивают и изучают с масляной иммерсией в проходящем свете.
Препараты У-хроматина заключают в специальный буферный р-р и изучают в ультрафиолетовом свете с помощью люминесцентного микроскопа.
Анализ проводят на разъединенных, распластанных клетках.
Срезы тканей для определения полового хроматина используют лишь тогда, когда невозможно получить мазки или препараты-отпечатки среза органа.
Слайд 35Работа 3. Скрининг-тесты наследственных обменных болезней человека
А. Определение фенилаланина в моче человека

(проба И. А. Феллинга)
К пробе мочи (2 мл) добавить 6 капель 10 % раствора хлорного железа.
Появление сине-зеленого окрашивания мочи указывает на положительный результат пробы (реакция положительна при содержании фенилаланина в моче более 15 мг %).
Слайд 36Фенилкетонурия (ФКУ) – это нарушение метаболизма аминокислот, приводящее к возникновению клинического синдрома умственной

отсталости с когнитивными и поведенческими расстройствами, вызванными повышенным уровнем фенилаланина.
Наследуется аутосомно-рецессивно.
Слайд 38 фенилаланин – незаменимая аминокислота, строительный блок белков.
При фенилкетонурии (наследстевнная ферментопатия, дефект

гена РАН (12q23.2; ген фенилаланингидроксилазы)
нарушено нормальное превращение фенилаланина в тирозин как результат недостатка фенилаланингидроксилазы
(A.Folling,1934, 98%),
фенилаланин накапливается в крови и превращается в фенилпировиноградную кислоту = нейротропный яд.
➤ судорожный синдром, олигофрения (фенилпировиноградная олигофрения).
Слайд 39При своевременной диагностике можно полностью избежать патологических изменений, если с рождения и

до полового созревания ограничить поступление в организм фенилаланина с пищей.
Позднее начало лечения хотя и даёт определённый эффект, но не устраняет развившихся ранее необратимых изменений ткани мозга.
Слайд 40При рождении ребёнка в роддомах
на 3—4 сутки берут анализ крови и проводят неонатальный скрининг для

обнаружения врождённых заболеваний обмена веществ.
На этом этапе возможно обнаружение фенилкетонурии и
возможно раннее начало лечения для предотвращения необратимых последствий.
Слайд 41В. Определение гомогентизиновой кислоты в моче человека (проба А. Гаррода)
К 0,5 мл

мочи больного алкаптонурией добавить
5 мл 5 % раствора азотнокислого серебра и несколько капель 10 % раствора аммиака. Появление черного окрашивания указывает на положительный результат пробы
(наличие в моче гомогентизиновой кислоты).
Слайд 42Алкапто́нури́я — наследственное заболевание, обусловленное выпадением функций оксидазы гомогентизиновой кислоты и характеризующееся расстройством обмена тирозина и экскрецией с

мочой большого количества гомогентизиновой кислоты.
На примере алкаптонурии сэр Арчибальд Эдвард Гаррод в 1909 году разработал концепцию метаболического блока.
Слайд 43Концепция метаболического блока de facto основана на принципе
«один ген - один

фермент - один признак (симптом)»
(принцип Бидла - Тейтама).
Слайд 44Согласно концепции метаболического блока, при наследственном заболевании имеется дефицит белка-фермента.
Это ведет

к нарушению определенной биохимической реакции.
Создается избыток вовлеченного в эту реакцию субстрата.
Часть его может выделяться из организма или откладываться в тканях
(«болезни накопления» или тезаурисмозы ).
Слайд 45
Избыток субстрата может вовлекаться в альтернативные превращения, давая такие продукты, которые отсутствуют

или имеются лишь в виде следов в норме.
Помимо избытка субстрата и действия альтернативных продуктов ( которые могут быть токсическими), часть симптомов наследственных болезней порождается нехваткой конечных продуктов блокированной реакции и подавлением реакций, следующих в цепи превращений за блокированным этапом.
Слайд 46Помимо избытка субстрата и действия альтернативных продуктов
( которые могут быть токсическими),

часть симптомов наследственных болезней порождается
нехваткой конечных продуктов блокированной реакции и подавлением реакций, следующих в цепи превращений за блокированным этапом.
Слайд 47Современная трактовка принципа Бидла-Тейтама и положений Гарода о метаболическом блоке сильно изменилась

по сравнению с оригинальной, поскольку появилось много новых данных, не укладывающихся в классическую схему:
1. Не все гены кодируют белки. Некоторые из них кодируют транспортные и рибосомальные РНК.
Слайд 482. Не все белки, кодируемые генами - ферменты.
Множество наследственных болезней не

связано с дефектом какого бы то ни было фермента, так как при них поражаются гены, кодирующие неэнзиматические белки.
Слайд 493. Один белок кодируется чаще всего не одним геном, а несколькими, причем

каждый ответственен за структуру одного полипептида в составе белка.
4. Гены в генотипах взаимодействуют, и, в силу этого, существует явление плейотропии - множественного действия гена.
Слайд 50Алкаптонурия возникает вследствие мутации гена, кодирующего синтез оксидазы гомогентезиновой кислоты.
Данная патология характеризуется
аутосомно-рецессивным
типом

наследования.
Алкаптонурией чаще болеют мужчины.
Ген оксидазы гомогетинзиновой кислоты человека (HGD) локализован на длинном плече
3 хромосомы человека (3q 21-23).
Слайд 51В нормальных условиях гомогентизиновая кислота — промежуточный продукт распада тирозина и фенилаланина

— переводится в малеилацетоуксусную кислоту,
из которой в конечном счёте образуются фумаровая и ацетоуксусная кислоты, вступающие в другие биохимические циклы.
Слайд 52Из-за дефекта фермента этот процесс тормозится, и остающаяся в избытке гомогентизиновая кислота

превращается полифенолоксидазой в хиноновый полифенол (алкаптон или бензохинонацетат), который и выводится почками.
Слайд 53Алкаптон - если он не полностью экскретируется с мочой - откладывается в

хрящевой и другой соединительной ткани,
обусловливая их потемнение и повышенную хрупкость.
Чаще всего первой появляется пигментация склер и ушных хрящей.
Радикального лечения нет, используется симптоматическая терапия и большие дозы аскорбиновой кислоты.
Слайд 54Г. Определение меди в моче человека
Пробу мочи больного гепатоцеребральной дистрофией (болезнь Вильсона

— Коновалова) нанносят на фильтровальную бумагу и высушивают.
На высушенную пробу мочи наносят каплю реактива (непосредственно перед постановкой реакции
растворить в 5 мл ацетона 0,1 г ортотолуидина и 0,5 г роданистого аммония).
Появление в течение 30 сек синего окрашивания указывает на положительный результат
(экскреция меди повышена).
Слайд 55Болезнь Вильсона — Коновалова (Гепатоцеребральная дистрофия, гепатолентикулярная дегенерация, болезнь Вестфаля — Вильсона) —
наследственное

нарушение метаболизма меди, приводящее к тяжелейшим поражениям центральной нервной системы и внутренних органов.
Слайд 56Диагностируется у 5-10 % больных циррозом печени дошкольного и школьного возраста. Заболевание

передаётся аутосомно-рецессивно.
Ген ATP7B, мутации которого вызывают заболевание, расположен на 13-й хромосоме (участок 13q14-q21)
Ген кодирует P-тип АТФазы, которая транспортирует медь в желчь и включает её в церулоплазмин.
Слайд 57Аутосомно-рецессивный тип наследования болезни Вильсона.
25 % вероятность рождения больного у родителей-гетерозигот

Слайд 58Английский невролог Сэмюель Вильсон
( S. Wilson, (1878 - 1937) в 1912 году
описал у больных:
* типичные изменения

в головном мозге,
*клинику нового заболевания,
*установил постоянное наличие цирроза печени
* и назвал патологию
прогрессивной лентикулярной дегенерацией
(лат. lenticularis чечевицеобразный).
Слайд 59Было предположено, что ген PRNP
(кодирует прионный белок, активен в головном мозге

и других тканях)
участвует в транспорте меди.
А вариации в гене PRNP могут изменить течение болезни, увеличивая возраст появления заболевания и влияя на тип симптомов, которые развиваются.
Слайд 60Медь в организме выполняет множество функций.
В основном она является кофактором для

таких ферментов, как
церулоплазмин, цитохром -С-оксидаза,
дофамин бета гидроксилаза, супероксиддисмутаза и тирозиназа.
Медь всасывается из ЖКТ в тонкой кишке: транспортный белок на CMT1 ( Copper Membrane Transporter 1) перемещает медь внутрь клеток.
Слайд 61Часть меди связывается с металлотионеином, а другая — перемещается в аппарат Гольджи с помощью транспортного белка

ATOX1.
В аппарате Гольджи в ответ на повышение концентрации меди
фермент ATP7A ( Copper-transporting ATPase 1)
высвобождает этот элемент через воротную вену в печень.
Слайд 62
В гепатоцитах белок ATP7B
1) связывает медь с церулоплазмином и высвобождает его в

кровь,
2) удаляет избыток меди с выделяющейся жёлчью.
При болезни Вильсона обе функции ATP7B нарушены.
Медь накапливается в ткани печени; церулоплазмин продолжает выделяться, но с недостатком меди (апоцерулоплазмин)
и быстро разрушается в кровотоке.
Слайд 63Когда меди в печени становится больше,
чем белков её связывающих,
происходит их

окислительное повреждение .
Это приводит к гепатиту, фиброзу
и в итоге к циррозу.
Также из печени в кровоток выделяется медь, которая не связана с церулоплазмином.
Эта свободная медь оседает по всему организму, особенно в почках, глазах и головном мозге.
Слайд 64Основную роль в патогенезе играет накопление меди в нервной ткани
(особенно поражены базальные

ганглии),
почках, печени и роговице и токсическое повреждение медью данных органов.
Нарушение метаболизма выражается в нарушении синтеза и снижении в крови концентрации церулоплазмина.
Слайд 65Церулоплазмин участвует в процессе выведения меди из организма.
В печени формируется крупноузловой

или смешанный цирроз.
В почках в первую очередь страдают проксимальные канальцы.
В головном мозге помимо особенно сильного поражения базальных ганглиев, поражаются зубчатое ядро мозжечка и черная субстанция.
Отложение меди в десцеметовой мембране глаза приводит к формированию кольца Кайзера-Флейшера.
Слайд 66Кольца Кайзера-Флейшера:
желтовато-зелёная или зеленовато-коричневая пигментация по периферии роговицы на десцеметовой мембране (задняя пограничная мембрана).
Кольца - отложения меди на

границе роговицы и склеры внутри от лимба роговицы, в первую очередь появляются в форме полулуния на верхнем крае роговицы.
Слайд 67Лечение
Патогенетическое лечение направлено на выведение меди из организма. Для этого применяются комплексообразующие соединения: тиолы, пеницилламин.

Лечение пеницилламином сопровождается заметным улучшением состояния больных или даже приводит к полной ликвидации симптомов.
Диета № 5 — с ограничением меди до 1 мг в сутки — исключение шоколада, орехов, сухофруктов, раков, печени, цельной пшеницы.
Препаратом выбора является купренил (пеницилламин), который эффективен в 90 % случаев. Д-пеницилламин или унитиол.
































































 Гимнастические упражнения как основной способ профилактики заболеваний у детей школьного возраста (11-13 лет)
Гимнастические упражнения как основной способ профилактики заболеваний у детей школьного возраста (11-13 лет) Санитария и гигиена на кухне
Санитария и гигиена на кухне Хламидиоз. Инфекционные болезни
Хламидиоз. Инфекционные болезни Инфекции передающиеся контактно-бытовым путём
Инфекции передающиеся контактно-бытовым путём Тіс қандай бөлімдерден тұрады?
Тіс қандай бөлімдерден тұрады? Современные вопросы ведения черепно-мозговой травмы
Современные вопросы ведения черепно-мозговой травмы Вирус Зика
Вирус Зика Медики всегда в строю…
Медики всегда в строю… Паллиативная помощь в Бразилии
Паллиативная помощь в Бразилии Анализ статистических данных влияния потребления кофе и энергетических напитков в состоянии стресса у студентов в академии
Анализ статистических данных влияния потребления кофе и энергетических напитков в состоянии стресса у студентов в академии Аутизм, РАС-биокоррекция при аутизме и РАС. Интенсив для родителей. Занятие 1
Аутизм, РАС-биокоррекция при аутизме и РАС. Интенсив для родителей. Занятие 1 ВИЧ и СПИД: профилактика
ВИЧ и СПИД: профилактика Меню с умом. Основы рационального питания, нутрициологии
Меню с умом. Основы рационального питания, нутрициологии Диетические столы, применяемые для больных в педиатрическом отделении
Диетические столы, применяемые для больных в педиатрическом отделении Физиология печени
Физиология печени Носовое кровотечение
Носовое кровотечение Оценка аллергологического статуса
Оценка аллергологического статуса Обучение взрослых медицинских работников
Обучение взрослых медицинских работников Расстройства пищевого поведения
Расстройства пищевого поведения Тақырып:микротолқынды спектроскопия
Тақырып:микротолқынды спектроскопия Свертывание крови. Группы крови
Свертывание крови. Группы крови Проба на индивидуальную совместимость по резус-фактору
Проба на индивидуальную совместимость по резус-фактору Врожденные пороки сердца
Врожденные пороки сердца Школа здоровья для беременных. Занятие 3. Как себя вести: вопросы и ответы
Школа здоровья для беременных. Занятие 3. Как себя вести: вопросы и ответы Острая ревматическая лихорадка (ОРЛ)
Острая ревматическая лихорадка (ОРЛ) Топографическая анатомия области шеи, топография сосудисто-нервных пучков шеи. Главный сосудисто-нервный пучок шеи
Топографическая анатомия области шеи, топография сосудисто-нервных пучков шеи. Главный сосудисто-нервный пучок шеи Синдром Брилла – Симмерса
Синдром Брилла – Симмерса Фармакотерпаия болевого синдрома
Фармакотерпаия болевого синдрома