Правила выбраковки поступающего в лабораторию клинического материала. Алгоритм и методы его обеззараживания
Содержание
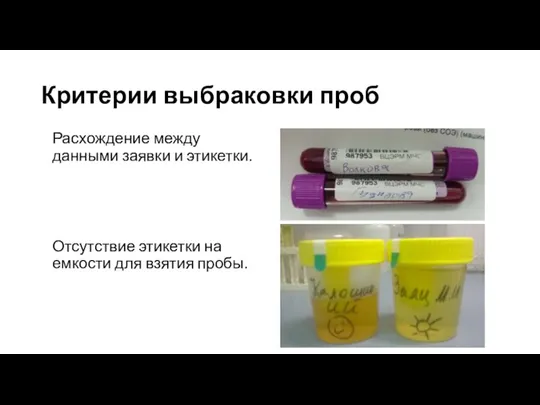
- 2. Критерии выбраковки проб Расхождение между данными заявки и этикетки. Отсутствие этикетки на емкости для взятия пробы.
- 3. Критерии выбраковки проб Взятый материал находится в несоответствующей емкости. Гемолиз (за исключением исследований, на которые наличие
- 4. Критерии выбраковки проб Невозможность прочесть на заявке и/или этикетке паспортные данные пациента. Отсутствие названия отделения, номера
- 5. Остатки материала, инфицированного (подозрительного на инфицирование) микроорганизмами I-IV групп патогенности, использованную посуду, после дезинфекции регламентируемыми дезинфицирующими
- 6. Обработка исследуемого материала, инфицированного м/о I—II групп патогенности мертиолят натрия концентрация 1 : 10 000 (0,01
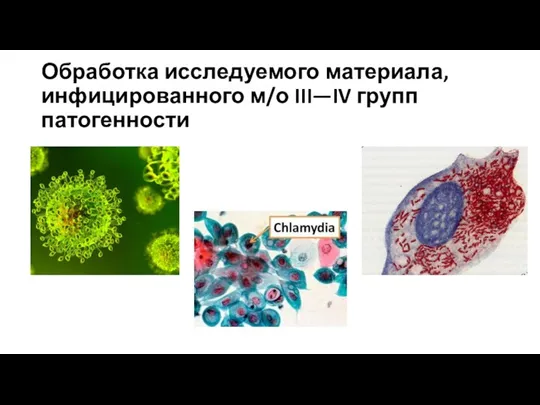
- 7. Обработка исследуемого материала, инфицированного м/о III—IV групп патогенности
- 8. Обработка исследуемого материала, инфицированного м/о III—IV групп патогенности Способ 1. Прогревание исследуемого образца при 100 °С
- 9. Обработка исследуемого материала, инфицированного бактериями II—IV групп патогенности, образующими споры исследуемый материал 100 мкл 0,9 мл
- 10. Обработка исследуемого материала, инфицированного вирусами I—II групп патогенности, содержащего инфекционную РНК, исследуемый материал 100 мкл 500
- 11. Обработка исследуемого материала, инфицированного вирусом натуральной оспы исследуемый материал 100 мкл 400 мкл лизирующего буферного раствора
- 12. Обработка исследуемого материала, инфицированного вирусами I—II групп патогенности, содержащих неинфекционную РНК или ДНК исследуемый материал 100
- 13. Обработка исследуемого материала, подозрительного на инфицирование высокопатогенным неизвестным возбудителем проводится в соответствии с действиями при обработке
- 15. Скачать презентацию










 Количественные нарушения со стороны лейкоцитов
Количественные нарушения со стороны лейкоцитов Тема 2.2: Двигательная активность и закаливание организма
Тема 2.2: Двигательная активность и закаливание организма Ботулизм
Ботулизм Холиномиметики. Классификация холиномиметиков. Препараты
Холиномиметики. Классификация холиномиметиков. Препараты Понятие о здоровье
Понятие о здоровье Спазмофилия
Спазмофилия Плоскостопие, причины и профилактика
Плоскостопие, причины и профилактика Лидер 21 века. Интеллектуальная игра
Лидер 21 века. Интеллектуальная игра Омыртқа жотасы мен жұлынның зақымдануы мен аурулары
Омыртқа жотасы мен жұлынның зақымдануы мен аурулары Аномалии родовой деятельности
Аномалии родовой деятельности Болезнь Паркинсона
Болезнь Паркинсона Острый коронарный синдром и острые заболевания пищевода и желудка
Острый коронарный синдром и острые заболевания пищевода и желудка Гиперчувствительность и её типы. Аллергия. Аллергические методы диагностики. Лекция № 19
Гиперчувствительность и её типы. Аллергия. Аллергические методы диагностики. Лекция № 19 Phylogenetic. Disorders of Human
Phylogenetic. Disorders of Human Витамины
Витамины Анализ смертности населения Калининградской области
Анализ смертности населения Калининградской области Веноздық жүйе
Веноздық жүйе Аборт опасный и безопасный. Лекция 29
Аборт опасный и безопасный. Лекция 29 Формовочные, отбеливающие, абразивные, полировочные материалы, используемые в зуботехнической лаборатории
Формовочные, отбеливающие, абразивные, полировочные материалы, используемые в зуботехнической лаборатории Паралич Белла
Паралич Белла Методы кастрации жеребцов
Методы кастрации жеребцов Польза секса для здоровья
Польза секса для здоровья Снотворные средства (гипнотики)
Снотворные средства (гипнотики) Ересек және балалардағы синкопальды жағдайлар
Ересек және балалардағы синкопальды жағдайлар Повреждения глаза и его придаточного аппарата, клиника, неотложная помощь, профилактика, диспансеризация
Повреждения глаза и его придаточного аппарата, клиника, неотложная помощь, профилактика, диспансеризация Афазия как речевое расстройство
Афазия как речевое расстройство Санитарно-гигиеническая обработка больных
Санитарно-гигиеническая обработка больных Заболеваемость антропонозными бактериальными инфекциями в РФ. Вопросы по ОКИ
Заболеваемость антропонозными бактериальными инфекциями в РФ. Вопросы по ОКИ