Слайд 2МКБ-10
Другие системные поражения соединительной ткани (M35)
M35.1 Другие перекрестные синдромы
Смешанное заболевание соединительной ткани

Слайд 3Определение
Синдром Шарпа – аутоиммунное заболевание соединительной ткани, включающее симптоматику по крайней мере

2 СЗСТ из числа следующих: системная красная волчанка, склеродермия, дерматомиозит, полимиозит, ревматоидный артрит.
Сопровождается наличием характерных аутоантител к U1-RNP (ранее известные как антитела к ENA).
Слайд 4February 1972
Mixed connective tissue disease-an apparently distinct rheumatic disease syndrome associated with

a specific antibody to an extractable nuclear antigen (ENA)
Gordon C. Sharp
Слайд 5Эпидемиология
Точная частота неизвестна.
Исследование, проведенное в округе Олмстед, штат Миннесота.
Заболеваемость 1,9 на 100

000 взрослых в год.
Средний возраст на момент постановки диагноза - 48 лет, 84% женщины.
“Норвежское” исследование.
2,1 на миллион взрослых в год.
Ж/М – 3.1/1
Средний возраст на момент постановки диагноза – 37,9 лет.
Слайд 6Этиология
Точная этиология – неизвестна.

Слайд 7Патофизиология
Сплайсосома – состоит из 5 мяРНК (snRNA) + белковых факторов, вместе составляющих
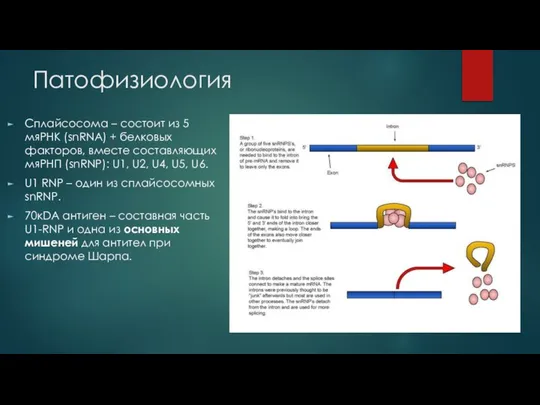
мяРНП (snRNP): U1, U2, U4, U5, U6.
U1 RNP – один из сплайсосомных snRNP.
70кDA антиген – составная часть U1-RNP и одна из основных мишеней для антител при синдроме Шарпа.
Слайд 8Патофизиология
Два механизма превращения мяРНП в аутоантигены:
Апоптотическая модификация
Молекулярная микикрия

Слайд 9Апоптотическая модификация
Во время апоптоза белки подвергаются посттрансляционной модификации из-за активизации различных ферментных

систем.
Эти модифицированные белки концентрируются в поверхностных пузырьках апоптотических клеток и становятся доступными для иммунной системы.
Антиген-презентирующими клетки представляют антигены Т-клеткам, которые выделяют цитокины, которые, в свою очередь, стимулируют В-клетки к выработке антител.
Анти-U1-RNP-антитело, анти-U1 70 кДа-антитело и анти-U1 70 кДа реактивные Т-лимфоциты, циркулирующие в периферической крови, являются отличительной чертой MCTD.
Слайд 10Молекулярная мимикрия
Экзогенные агенты (инфекции, лекарства, токсины, химические вещества) – аминокислотная последовательность несобственных

белков может имитировать эпитоп в организме хозяина и индуцировать выработку антител.
HERVы – неактивные последовательности ретровирусов человека, следы оригинальных вирусов, которые были интегрированы в геном человека миллионы лет назад.
Слайд 11HERVs
У 90,9% пациентов со смешанной болезнью соединительной ткани (MCTD) (n = 22)

было выявлено присутствие консервативной последовательности pol вируса иммунодефицита человека типа 1 (ВИЧ-1) в ДНК, выделенной из сыворотки.
У 100% пациентов с SSc (n = 9), положительных на анти-U1-рибонуклеопротеин (RNP), присутствовала ВИЧ-1-консервативная последовательность pol.
Identification of retroviral conserved pol sequences in serum of mixed connective tissue disease and systemic sclerosis patients, 2004.
Слайд 13HERVs
“The close homology with an already incorporated HERV-K virus suggests that the

HIV-1 vatches may belong to this and other retroviral or viral species, or to previously nonpathogenic ancestors already resident in the human genome. For whatever reason, HIV-1 viral proteins closely resemble fragments of a large sample of the human proteome”.
Extensive viral mimicry of 22 AIDS-related autoantigens by HIV-1 proteins and pathway analysis of 561 viral/human homologues suggest an initial treatable autoimmune component of AIDS Chris J. Carter, 2011
Слайд 14Классификационные критерии (Sharp,1987)

Слайд 18Классификационные критерии (Alarcon-Segovia G., 1995)
Для постановки диагноза необходим один серологический и три

клинических критерия (обязательно синовит или миозит).
Слайд 19Классификационные критерии (Kasukawa)

Слайд 26Лечение
Рандомизированных контролируемых исследований по лечению смешанных заболеваний соединительной ткани еще не проводилось.

Целью терапии является контроль клинических проявлений заболевания и предотвращение вовлечения внутренних органов.
Слайд 27Лечение
Феномен Рейно
Симптоматическое лечение включает в себя отказ от кофеина, курения, переохлаждения конечностей.
БМКК:

например, нифедипин.
Внутривенные простагландины и нитроглицерины.
Существуют случаи, когда феномен Рейно реагировал на ритуксимаб.
Слайд 28Лечение
Артриты и артралгии
Обычно хороший ответ на НПВП и гидроксихлорохин.
При наличии рефрактерного синовита

можно использовать кортикостероиды и метотрексат.
Слайд 29Лечение
Плеврит, перикардит, миозит, миокардит и асептический менингит
Ответ на стероидную терапию.
Метотрексат, циклоспорин, азатиоприн

и микофенолата мофетил – препараты второй линии.
Стероид-резистентный миозит может отвечать на внутривенный иммуноглобулин.
Слайд 30Лечение
Легочная гипертензия
Иммуносупрессия стероидами в сочетании с циклофосфамидом/микофенолатом может давать эффект.
БМКК.
Эффективность применения варфарина

– неизвестна.
Применение простагландинов (эпопростенол), антагонистов эндотелиновых рецепторов (бозентан, амбризентан), ингибиторов ФДЭ-5 (силденафил, варденафил) – четких рекомендаций нет, из терапевтических соображений эффект может быть.
Слайд 31Лечение
Аутоиммунная гемолитическая анемия и тромбоцитопения
Инициальное лечение – кортикостероиды.
При резистентности – рассмотреть возможность

применения ритуксимаба.
Слайд 32Прогноз
Исследование 280 пациентов: вероятность 5-летней выживаемости – 98%, 10-летней – 96%, 15-летней

– 88%. Умерли 22 из 280 пациентов.
“Норвежское” исследование – 12 из 147 пациентов умерли в течение 5,6 лет наблюдения.
ЛАГ: 3 пациента – из-за недостаточности правого желудочка, возникшнего на фоне ЛАГ.
Интерстициальное поражение легких – 2 пациента.
Злокачественные новообразования – 4 пациента.
Ишемическая болезнь сердца – 2 пациента.
1 пациент – причина смерти неизвестна.
Обнаружение aCL, anti-b2-GPI и AECA – более высокий риск смерти.






























 Причины и механизмы отклонений результатов клинических лабораторных исследований
Причины и механизмы отклонений результатов клинических лабораторных исследований Основы трансторакальной эхокардиографии
Основы трансторакальной эхокардиографии Болезнь Тея - Сакса
Болезнь Тея - Сакса Антисептики
Антисептики Лучевые исследования при заболеваниях печени, желчевыводящих путей, поджелудочной железы
Лучевые исследования при заболеваниях печени, желчевыводящих путей, поджелудочной железы Повязка та її види
Повязка та її види Опорно-двигательный аппарат, кожные покровы, суставы
Опорно-двигательный аппарат, кожные покровы, суставы Первая медицинская помощь при травмах опорно-двигательного аппарата
Первая медицинская помощь при травмах опорно-двигательного аппарата Нановакцины и нанолекарства
Нановакцины и нанолекарства Bronchitis
Bronchitis Глаза – окно в мир. Строение глаза
Глаза – окно в мир. Строение глаза Рецепты здоровья
Рецепты здоровья Противоаритмические лекарственные препараты
Противоаритмические лекарственные препараты Висцероптоз (спланхноптоз)
Висцероптоз (спланхноптоз) Питание при нехватке витамина В12
Питание при нехватке витамина В12 Пастереллез кроликов
Пастереллез кроликов Болезнь Альцгеймера
Болезнь Альцгеймера Метоика кормения тяжелобольного пациента
Метоика кормения тяжелобольного пациента Внутрибольничный колиэнтерит
Внутрибольничный колиэнтерит Сестринский уход за пациентами с анаэробной инфекцией
Сестринский уход за пациентами с анаэробной инфекцией Условия для образования органа зрения
Условия для образования органа зрения Классификация лекарственных препаратов
Классификация лекарственных препаратов Анафилактический шок
Анафилактический шок Ангиоотек. Классификации – по клинической характеристике
Ангиоотек. Классификации – по клинической характеристике Искусственное прерывание беременности. Имеет ли будущий папа права на принуждение будущей мамы к сохранению беременности
Искусственное прерывание беременности. Имеет ли будущий папа права на принуждение будущей мамы к сохранению беременности Основи зоогігієни і ветеринарії
Основи зоогігієни і ветеринарії Дистиллированная вода. Методы получения для использования в фармакологии и медицине
Дистиллированная вода. Методы получения для использования в фармакологии и медицине Осовные направления сестринского ухода за пациентом с язвенной болезнью желудка
Осовные направления сестринского ухода за пациентом с язвенной болезнью желудка