Содержание
- 2. Никто из нас не совершенен. Всё больше генетических тестов становится доступно, и каждый из нас, в
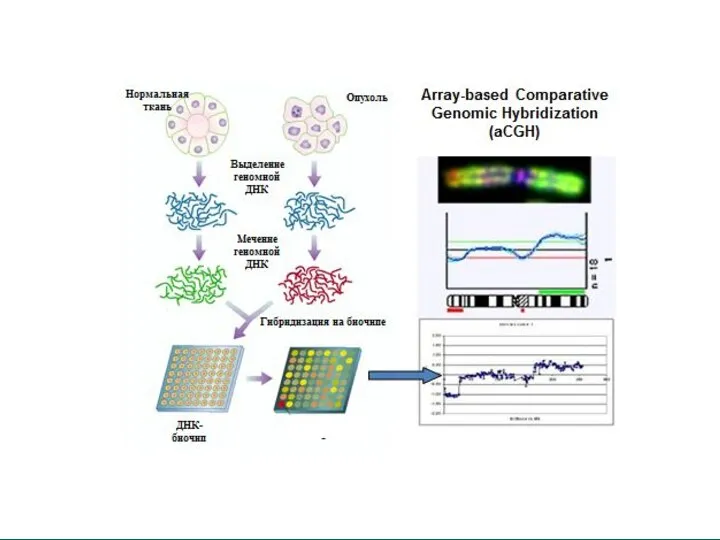
- 3. CNV Copy Number Variations Фрагмент ДНК, размером более 1 т.п.н., по числу копий отличающийся от референсного
- 6. Локус-специфичная частота CNV варьирует от 0,0001 до 0,00001. Патогенные дупликации встречаются реже, чем делеции, т.к. их
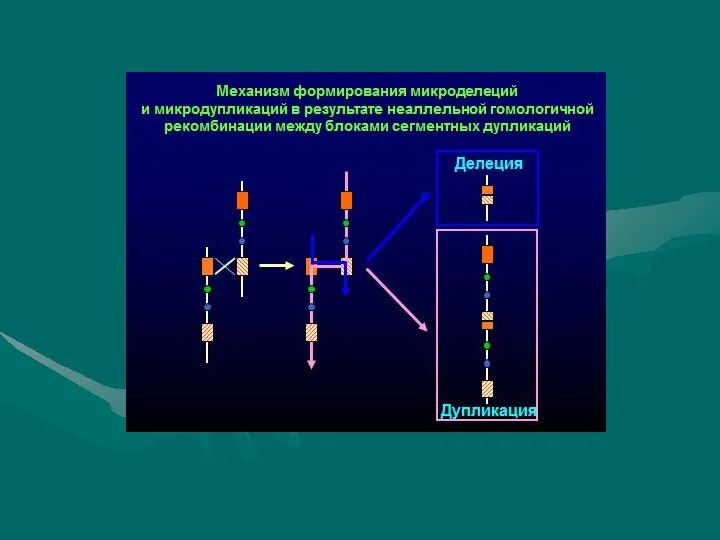
- 7. Патогенетические механизмы развития заболеваний: изменение дозы генов эффект положения разрыв кодирующей последовательности гена образование химерного гена
- 8. Клиническое значение Точки разрыва аберрации могут нарушать кодирующую последовательность гена или приводить к возникновению нового гибридного
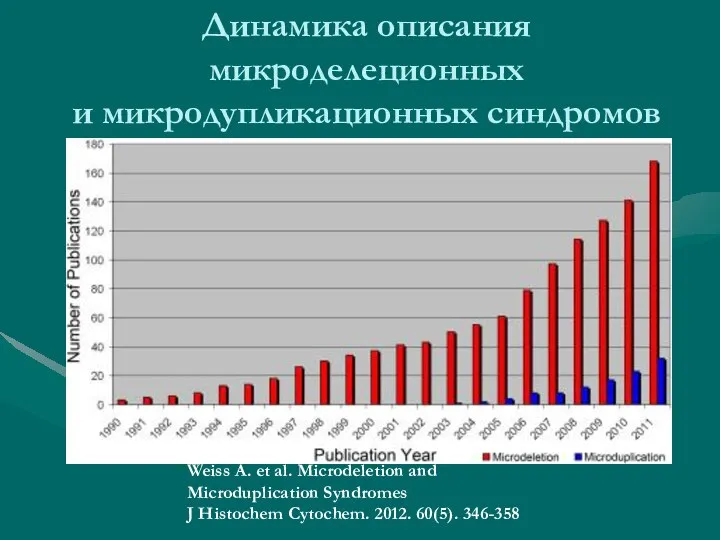
- 9. Динамика описания микроделеционных и микродупликационных синдромов Weiss A. et al. Microdeletion and Microduplication Syndromes J Histochem
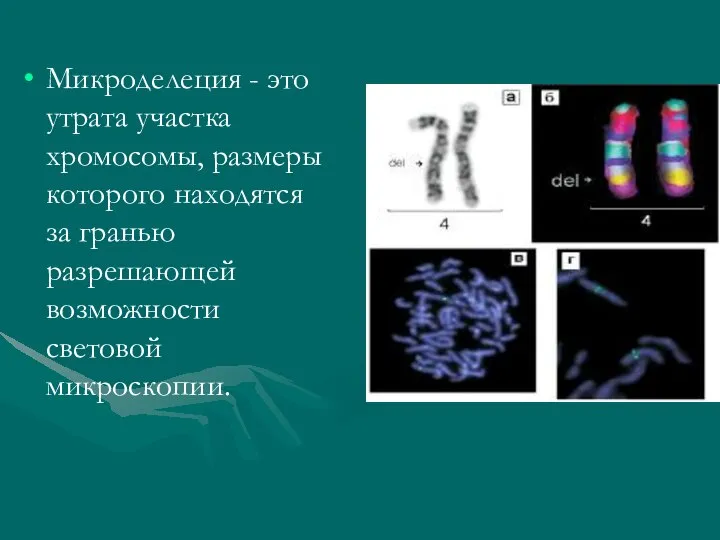
- 10. Микроделеция - это утрата участка хромосомы, размеры которого находятся за гранью разрешающей возможности световой микроскопии.
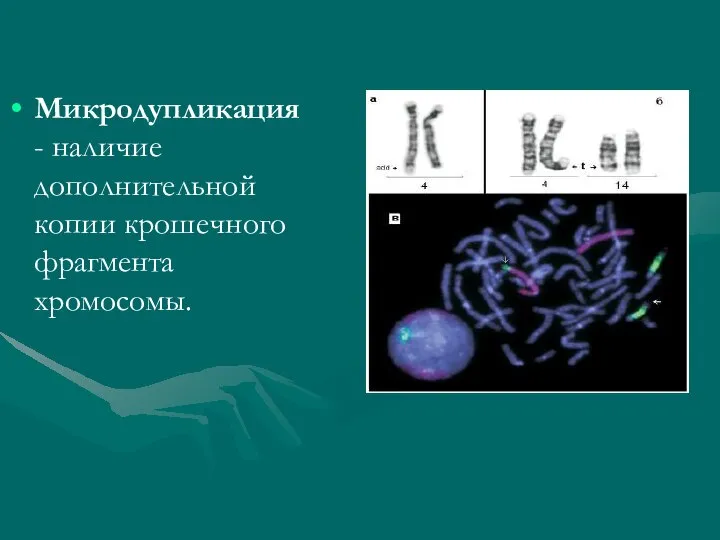
- 11. Микродупликация - наличие дополнительной копии крошечного фрагмента хромосомы.
- 13. Nevado et al. New microdeletion and microduplication syndromes: A comprehensive review Genet Mol Biol. 2014. V.
- 14. СИНДРОМЫ МИКРОДЕЛЕЦИЙ СИНДРОМ ВИЛЬЯМСА (7q11.23) Синдром «лица эльфов» - заболевание, вызванное делецией размером 1,5 – 1,8
- 15. СИНДРОМ ВИЛЬЯМСА (7q11.23) Клинические признаки: Необычное лицо, низкий рост, короткий нос, полные щеки, маленькая нижняя челюсть,
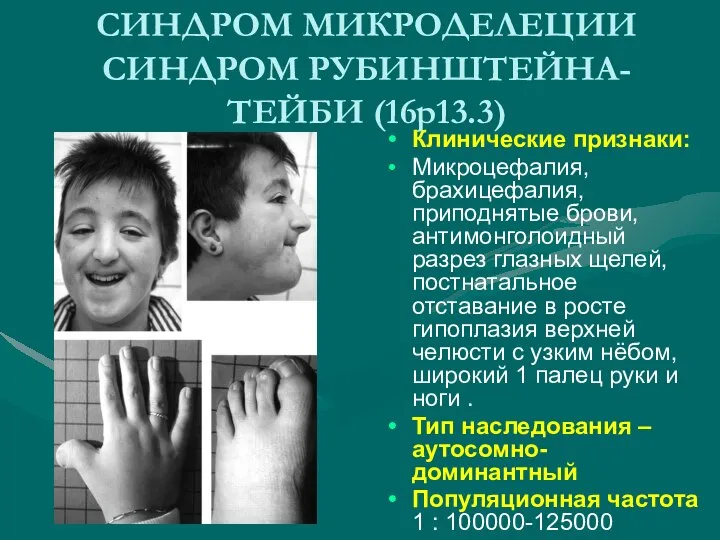
- 16. СИНДРОМ МИКРОДЕЛЕЦИИ СИНДРОМ РУБИНШТЕЙНА-ТЕЙБИ (16p13.3) Заболевание, вызванное делецией или мутациями в генах CREBBP (локус16р13.3 ) или
- 17. СИНДРОМ МИКРОДЕЛЕЦИИ СИНДРОМ РУБИНШТЕЙНА-ТЕЙБИ (16p13.3) Клинические признаки: Микроцефалия, брахицефалия, приподнятые брови,антимонголоидный разрез глазных щелей, постнатальное отставание
- 18. СИНДРОМ МИКРОДЕЛЕЦИИ СИНДРОМ СМИТ-МАГЕНИС (17р11.2) Заболевание, вызванное делецией 3,7 миллионов нуклеотидных пар или мутациями в гене
- 19. СИНДРОМ СМИТ МАГЕНИС Клинические признаки: Черпно-лицевые аномалии: брахицефалия, выпуклый лоб гипоплазия средней части лица, брахидактилия, пороки
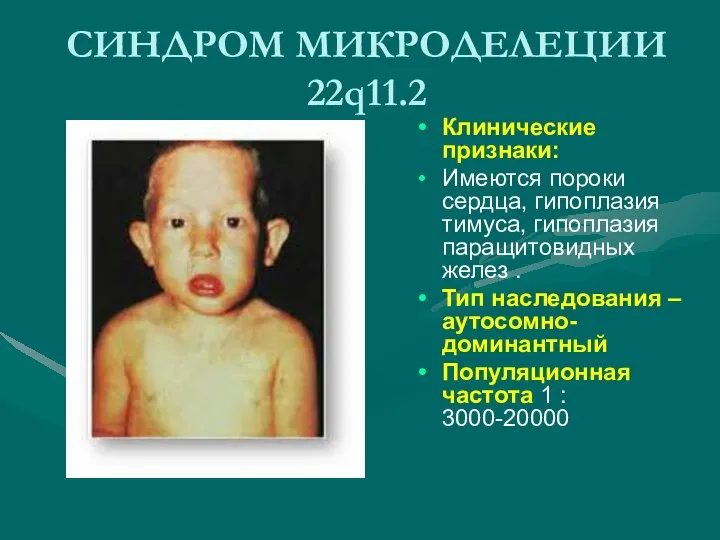
- 20. СИНДРОМ МИКРОДУПЛИКАЦИИ 22q11.2 Синдром Ди Джорджи, велокардиофациальный синдром, делеция центрального участка длинного плеча хромосомы в 1,5
- 21. СИНДРОМ МИКРОДЕЛЕЦИИ 22q11.2 Клинические признаки: Имеются пороки сердца, гипоплазия тимуса, гипоплазия паращитовидных желез . Тип наследования
- 22. СИНДРОМЫ ХРОМОСОМНОЙ НЕСТАБИЛЬНОСТИ Синдромы хромосомный нестабильности, также известные как синдромы хромосомной поломки - это группа генетических
- 23. Анемия Фанкони 13 генов, мутации в которых вызывают развитие анемии Фанкони: FANCA, FANCB, FANCC, FANCD1, FANCD2,
- 24. Анемия Фанкони Клинические признаки: Недостаточность костного мозга, небольшой рост, различные повреждения кожи, рук, головы, глаз, почек,
- 25. Ниймеген синдром (8q21) Ген NBN, мутации в котором приводят к развитию синдрома, состоит из 50 тыс.п.н.
- 26. Ниймеген синдром Клинические признаки: Микроцефалия, задержка умственного развития, отсталость физ. Развития, комбинированный иммунодефицит, «птичье лицо» .
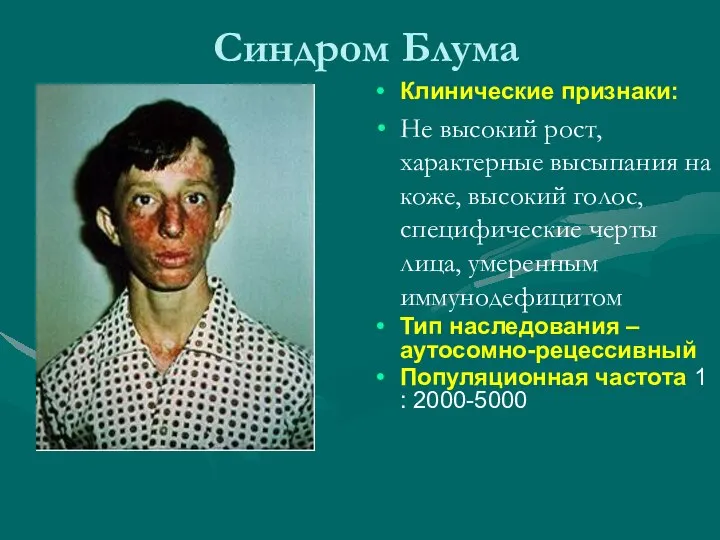
- 27. Синдром Блума (15q26.1) Причиной заболевания служит мутация в гене BLM (RECQL3), который имеет 22 экзона. Кодирует
- 28. Синдром Блума Клинические признаки: Не высокий рост, характерные высыпания на коже, высокий голос, специфические черты лица,
- 29. Атаксия телеангиэктазия (синдром Луи-Бара) 11q22-23 Белковый продукт гена ATM относится к семейству фосфатидилинозитолкиназ, контролирует клеточный цикл,
- 30. Атаксия телеангиэктазия Клинические признаки: Мозжечковая атаксия, интенционный тремор, нарушения движений глазного яблока, косоглазие, нистагм, отставание в
- 31. Пигментная ксеродерма Пигментная ксеродерма – генетически разнородное, панэтническое, аутосомно-рецессивное заболевание репарации ДНК. Вызвана мутациями, влияющими на
- 32. Пигментная ксеродерма Клинические признаки: фотофобия, повышенная чувствительность к УФЛ, развитие рака и атрофии кожи, гиперпигментация типа
- 34. Скачать презентацию






















 Первая помощь при неотложных состояниях у детей
Первая помощь при неотложных состояниях у детей О мерах по обеспечению безопасности несовершеннолетних в связи с угрозой распространения коронавирусной инфекции
О мерах по обеспечению безопасности несовершеннолетних в связи с угрозой распространения коронавирусной инфекции Объективный структурированный клинический экзамен – ОСКЭ
Объективный структурированный клинический экзамен – ОСКЭ Принципы анестезиологии и интенсивной терапии в условиях ограниченных ресурсов
Принципы анестезиологии и интенсивной терапии в условиях ограниченных ресурсов Практика по выполнению заданий блока С
Практика по выполнению заданий блока С Врожденные пороки сердца
Врожденные пороки сердца Антиманиакальные средства. Препараты лития. Возможные механизмы действия. Применение. Побочные эффекты
Антиманиакальные средства. Препараты лития. Возможные механизмы действия. Применение. Побочные эффекты Гериатриялық фармакология
Гериатриялық фармакология здоровье и питание
здоровье и питание тәрбие процессі факты мақсаты Ару Б
тәрбие процессі факты мақсаты Ару Б Вакцинация и иммунопрофилактика
Вакцинация и иммунопрофилактика Туберкулёз и его профилактика
Туберкулёз и его профилактика Реакция агглютинации и её варианты
Реакция агглютинации и её варианты Профилактика психосоматических заболеваний обучающихся
Профилактика психосоматических заболеваний обучающихся Бычий цепень
Бычий цепень Первая помощь при острой сердечной недостаточности и инсульте
Первая помощь при острой сердечной недостаточности и инсульте Созылмалы бүйрек ауруларының үдеу механизмі
Созылмалы бүйрек ауруларының үдеу механизмі Хирургические заболевания щитовидной железы
Хирургические заболевания щитовидной железы Какой шоколад полезнее?
Какой шоколад полезнее? Мышечная дистрофия Дюшенна
Мышечная дистрофия Дюшенна Газ алмасу механизмінің бұзылуына байланысты
Газ алмасу механизмінің бұзылуына байланысты Полисомнография. Сущность метода. Показания к проведению исследования
Полисомнография. Сущность метода. Показания к проведению исследования Топографическая анатомия малого таза и промежности
Топографическая анатомия малого таза и промежности Холерный вибрион. Микробиология
Холерный вибрион. Микробиология Взрослым о подростковой наркомании
Взрослым о подростковой наркомании Щитовидная железа
Щитовидная железа Экспресс-методы в лабораторной диагностике
Экспресс-методы в лабораторной диагностике Вред картошки фри
Вред картошки фри