1. Расчет фазовых превращений в металлах и сплавах В работе предложены аналитические выражения для расчета критических темпер
- Главная
- Разное
- 1. Расчет фазовых превращений в металлах и сплавах В работе предложены аналитические выражения для расчета критических темпер

Содержание
- 2. Энергия образования кристаллического вещества равна : Уравнения (3,4) позволяют рассчитать также координационные числа атомов в жидких
- 3. • Выражения (1-6) применимы и для расчета фазовых превращений в сплавах. В этом случае энергии связи
- 4. 2. Расчет фазовых равновесий в трехкомпонентных металлических системах Существующие методы термодинамического расчета фазовых равновесий и построения
- 5. Расчет процесса кристаллизации многокомпонентных твердых растворов, где число компонентов n>3 Для многокомпонентных систем в случае двухфазных
- 6. 4 Расчет неравновесной кристаллизации твердых растворов При разработке метода расчета весь процесс неравновесной кристаллизации сплава рассматривается
- 7. Выводы: Для расчета общего количества твердой фазы m-αn и ее относительной доли Sn после n-й стадий
- 9. Скачать презентацию
Слайд 2Энергия образования кристаллического вещества равна :
Уравнения (3,4) позволяют рассчитать также координационные
Энергия образования кристаллического вещества равна :
Уравнения (3,4) позволяют рассчитать также координационные

в жидких и твердых фазах, образующиеся при нагреве или охлаждении металла,
а также их изменения при фазовых переходах.
При температурах фазовых переходов, когда устанавливается критическое расстояние между соседними ионами, должно выполнятся следующее условие :
:
Расчет температур фазовых переходов в чистых металлах :
где:
где: - температуры испарения, плавления и полиморфного превращения.
Слайд 3
• Выражения (1-6) применимы и для расчета фазовых превращений в сплавах.
• Выражения (1-6) применимы и для расчета фазовых превращений в сплавах.
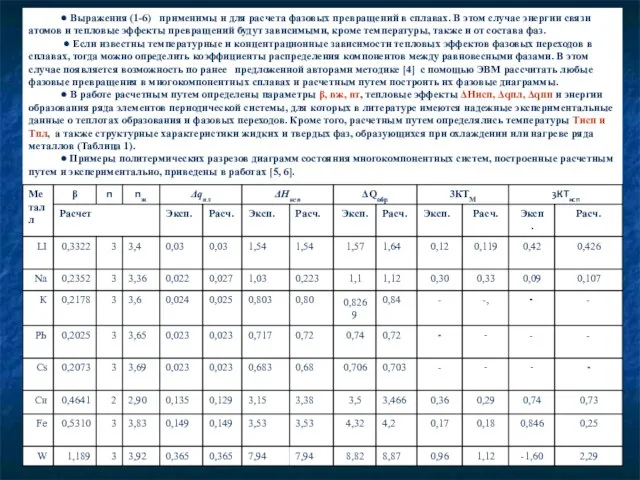
• Если известны температурные и концентрационные зависимости тепловых эффектов фазовых переходов в сплавах, тогда можно определить коэффициенты распределения компонентов между равновесными фазами. В этом случае появляется возможность по ранее предложенной авторами методике [4] с помощью ЭВМ рассчитать любые фазовые превращения в многокомпонентных сплавах и расчетным путем построить их фазовые диаграммы.
• В работе расчетным путем определены параметры β, nж, nт, тепловые эффекты ΔНисп, Δqпл, Δqпп и энергии образования ряда элементов периодической системы, для которых в литературе имеются надежные экспериментальные данные о теплотах образования и фазовых переходов. Кроме того, расчетным путем определялись температуры Тисп и Тпл, а также структурные характеристики жидких и твердых фаз, образующихся при охлаждении или нагреве ряда металлов (Таблица 1).
• Примеры политермических разрезов диаграмм состояния многокомпонентных систем, построенные расчетным путем и экспериментально, приведены в работах [5, 6].
Слайд 4
2. Расчет фазовых равновесий в трехкомпонентных
металлических системах
Существующие методы термодинамического расчета фазовых равновесий
2. Расчет фазовых равновесий в трехкомпонентных
металлических системах
Существующие методы термодинамического расчета фазовых равновесий

В работе получены аналитические зависимости между составами исходных сплавов, составами и относительными количествами равновесных фаз и коэффициентами распределения компонентов, позволяющие рассчитать составы и относительные количества фаз в зависимости от температуры и состава исходного сплава (число компонентов сплава n= 2,3, …N) .
• Состав жидкой фазы Хn (n=А,В,С индексы компонентов) рассчитывается:
• Состав твердой фазы, находящейся в равновесии с жидкой при заданной температуре, определяется, как:
где:
- грамм-атомные доли компонентов А, В и С в твердой (α) и жидкой (Ж) фазах,
- грамм-атомные доли компонентов А, В и С в исходном сплаве.
• Относительные количества твердой
и жидкой (1-
)
фаз
можно определить из уравнении:
• Например, при кристаллизации тройных твердых растворов
температуры ликвидуса и солидуса определяются из условий:
где:
Слайд 5
Расчет процесса кристаллизации многокомпонентных твердых растворов,
где число компонентов n>3
Расчет процесса кристаллизации многокомпонентных твердых растворов,
где число компонентов n>3

Для многокомпонентных систем в случае двухфазных равновесий α+ж
зависимости между составами исходного сплава
, жидкой
и твердой
фазами, а также коэффициентами распределения компонентов также имеют вид:
где: i – индекс компонента сплава (i=1÷n):
αT - относительное количество твердой фазы при заданной температуре Т0К.
Для определения относительной доли твердой фазы αТ:
Определяя концентрационные и температурные зависимости коэффициентов распределенияв многокомпонентных сплавах независимыми способами, из уравнений () можно найти долю равновесных твердой (αТ) и жидкой (1-αТ) фаз при любой температуре, рассчитать их составы и определить положения конод.
Температуры ликвидуса и солидуса многокомпонентных сплавов также могут быть определены из условий:
Слайд 64 Расчет неравновесной кристаллизации твердых растворов
При разработке метода расчета
4 Расчет неравновесной кристаллизации твердых растворов
При разработке метода расчета
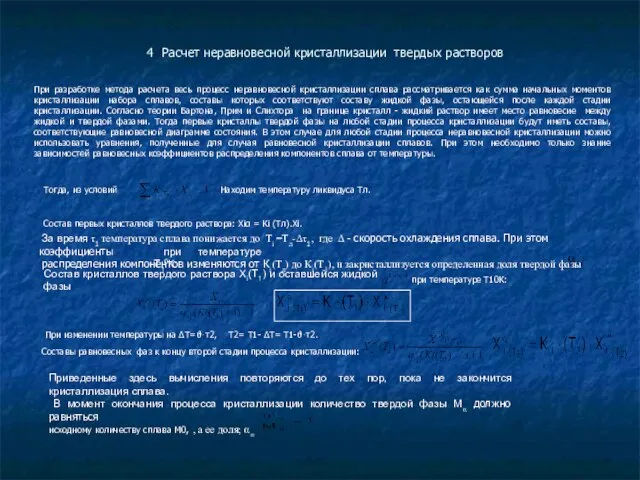
Тогда, из условий
Находим температуру ликвидуса Тл.
Состав первых кристаллов твердого раствора: Хiα = Кi (Тл).Хi.
За время τ1 температура сплава понижается до Тi =Тл-Δτ1, где Δ - скорость охлаждения сплава. При этом коэффициенты
распределения компонентов изменяются от Кi(Тл) до Кi(Т1), и закристаллизуется определенная доля твердой фазы
.
Состав кристаллов твердого раствора Хi(Т1) и оставшейся жидкой фазы
при температуре Т10К:
при температуре Т10К:
При изменении температуры на ΔТ=ϑ⋅τ2, Т2= Т1- ΔТ= Т1-ϑ⋅τ2.
Составы равновесных фаз к концу второй стадии процесса кристаллизации:
Приведенные здесь вычисления повторяются до тех пор, пока не закончится кристаллизация сплава.
В момент окончания процесса кристаллизации количество твердой фазы Мα должно равняться
исходному количеству сплава М0, , а ее доля; α=
.
Слайд 7 Выводы:
Для расчета общего количества твердой фазы m-αn и ее относительной
Выводы:
Для расчета общего количества твердой фазы m-αn и ее относительной

m-αn= m-α1+ m-α2+…+ m-αn ,
Sn= α1+(1- α1)α2+(1- α1) (1- α2) α3+…+(1- α1) (1- α2)… (1- αn-1) αn .
Температуру при которой Sn становится равной единице, примем за температуру неравновесного солидуса. Общее время кристаллизации сплава (τ0) при заданной скорости охлаждения ϑ равно: τ0=(Тлик-Тсолид) ϑ.
1.Предложен метод расчета фазовых равновесий в многокомпонентных металлических системах и построения их диаграмм состояния, основанный на впервые сформулированных условиях определения критических точек фазовых превращений с использованием температурных и концентрационных зависимостей коэффициентов распределения компонентов. Установлены аналитические зависимости между коэффициентами распределения компонентов, средним химическим составом сплавов, составом и относительными количествами равновесных фаз. Предложенный метод позволяет количественно описать процесс формирования фазового состава и структуры сплавов при равновесных и неравновесных условиях охлаждения.
2. Предложены математические модели изменения избыточных химических потенциалов компонентов при фазовых переходах и произведения растворимостей компонентов при выделении кристаллов химических соединений в сплавах систем на основе алюминия и меди. Разработаны программы расчета фазовых превращений в равновесных и неравновесных условиях охлаждения.
3. Расчетным методом, а также методами микроскопического, дифференциально-термического и микрорентгеноспектрального анализов исследованы фазовые равновесия в сплавах систем Al-Cu-Si, Al-Ni-Si, Al-Si-Cu-Ni. Показано хорошее соответствие между расчетными и опытными данными.Впервые установлено, что в сплавах изученных систем имеет место ряд безвариантных эвтектических и перитектических превращений. Уточнены положения критических точек.
 Билл Виола. Видеоарт
Билл Виола. Видеоарт Bulienko_Siemion_Pavlovich
Bulienko_Siemion_Pavlovich Adani Vidya Mandir, Ahmedabad
Adani Vidya Mandir, Ahmedabad Роль і завдання комерційної роботи торгового підприємства на сучасному етапі
Роль і завдання комерційної роботи торгового підприємства на сучасному етапі Блокада Ленинграда
Блокада Ленинграда Задержка роста плода
Задержка роста плода Элементы квалификации руководителей и служащих предприятий
Элементы квалификации руководителей и служащих предприятий Упражнения для тренировки глаз по методу Шичко-Бейтса
Упражнения для тренировки глаз по методу Шичко-Бейтса КЛУБ_UTL_01 сенября 2022 (1)
КЛУБ_UTL_01 сенября 2022 (1) Ванная и спальня
Ванная и спальня Волейбол
Волейбол С днем медика (открытки)
С днем медика (открытки) Понятие статьи. Веб-райтер
Понятие статьи. Веб-райтер Спрос, предложение и рыночное равновесие
Спрос, предложение и рыночное равновесие  1
1 Холодное оружие
Холодное оружие Соединения элементов
Соединения элементов Атомная энергетика, как альтернативный источник энергии
Атомная энергетика, как альтернативный источник энергии Командный менеджмент
Командный менеджмент Презентация на тему Украшение пасхального яйца
Презентация на тему Украшение пасхального яйца Business meeting in USA
Business meeting in USA Медальерное искусство
Медальерное искусство B1
B1 Россия и ООН
Россия и ООН Презентация на тему Биотические факторы
Презентация на тему Биотические факторы Клад. Законодательное понятие. Самые крупные найденные клады
Клад. Законодательное понятие. Самые крупные найденные клады Фотомарафон ВГСХА - 2019
Фотомарафон ВГСХА - 2019 Загрязнение гидросферы
Загрязнение гидросферы