Слайд 2Контрольные вопросы
Какие из приведенных соединений относятся к органическим?
Ответ 1 : все

приведенные соединения
Ответ 2 : б, в, г, д
Ответ 3 : б, в, д, е, ж
Ответ 4 : все, кроме "е" и "з"
Слайд 3Что является критерием деления веществ на органические и неорганические?
Ответ 1 :

происхождение вещества
Ответ 2 : элементный состав соединения
Ответ 3 : способ получения
Ответ 4 : способность к горению
Ответ 5 : способность к диссоциации
Ответ 6 : молекулярная масса
Ответ 7 : температуры кипения и плавления
Слайд 4Одной из причин многообразия органических веществ является
Ответ 1 : способность атомов углерода

образовывать углерод- углеродные связи
Ответ 2 : аллотропия углерода
Ответ 3 : большое число элементов, из которых образованы органические вещества
Ответ 4 : многообразие реакций, протекающих в живой природе
Слайд 5Исторический экскурс
1.Какие открытия нанесли удар по учению
о «жизненной силе»?
( работы Ф. Вёлера,

А Кольбе,
А.М. Бутлерова, М. Бертло)
2. Кто ввел понятие «органическая химия»?
3. Перечислите особенности органических веществ.
Слайд 8Образование ковалентной связи

Слайд 10Теория гибридизации
Лайнус Карл Полинг
выдвинул постулат о
гибридизации
близких по энергии АО
и

образование
гибридных облаков.
Гибридизацией орбиталей называется процесс их выравнивания по форме и энергии.
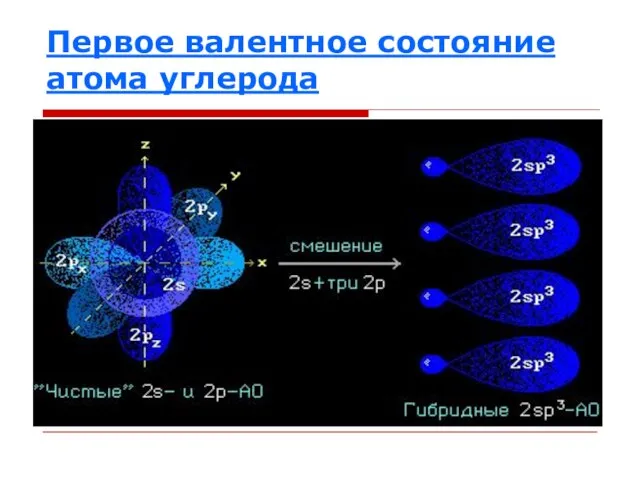
Слайд 11Первое валентное состояние атома углерода
Слайд 12Характеристика молекулы метана
Форма молекулы:
Валентный угол:
Длина связи:
L (c-c) = 0,154 нм
Активность молекулы:
Энергия связи:
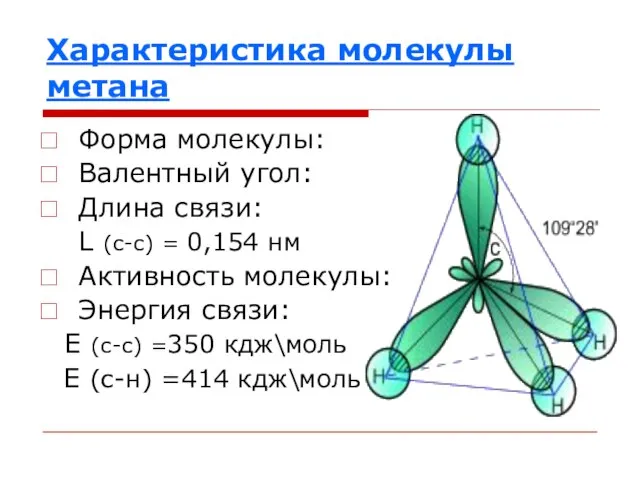
Е (с-с) =350 кдж\моль
Е (с-н) =414 кдж\моль
Слайд 13Пространственная модель молекулы метана

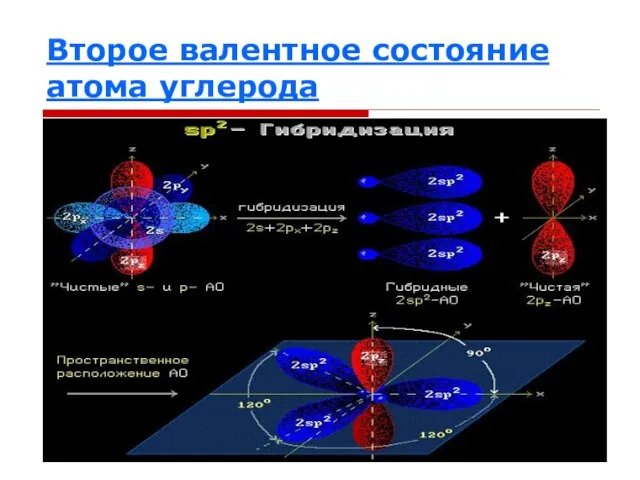
Слайд 16Второе валентное состояние атома углерода
Слайд 20Характеристика молекулы этилена
Форма молекулы:
Валентный угол:
Длина связи:
L (c=c) = 0,134 нм
Активность молекулы:
Энергия связи:
Е

(Σ) =350 кдж\моль
Е (Π) =270 кдж\моль
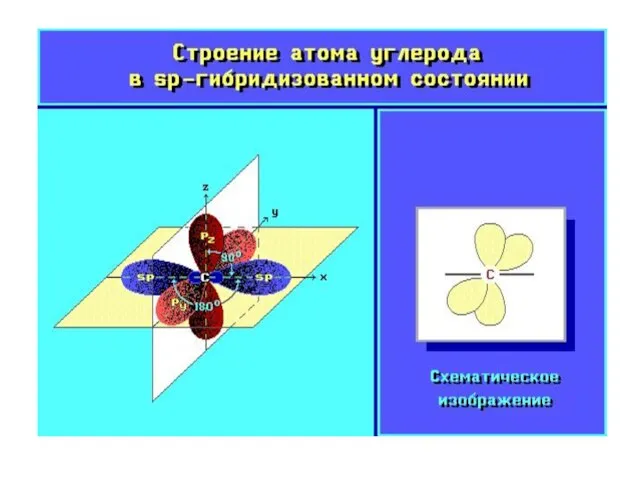
Слайд 22Третье валентное состояние атома углерода

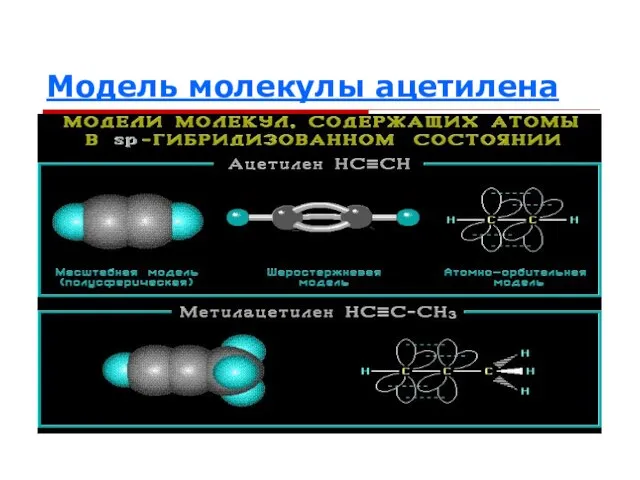
Слайд 26Пространственная модель молекулы ацетилена

Слайд 27Характеристика молекулы ацетилена
Форма молекулы:
Валентный угол:
Длина связи:
L (c=c) = 0,120 нм
Активность молекулы:
Энергия связи:
Е

(Σ) =350 кдж\моль
Е (Π) =270 кдж\моль
Слайд 29
Типы гибридизации атомов углерода в соединениях
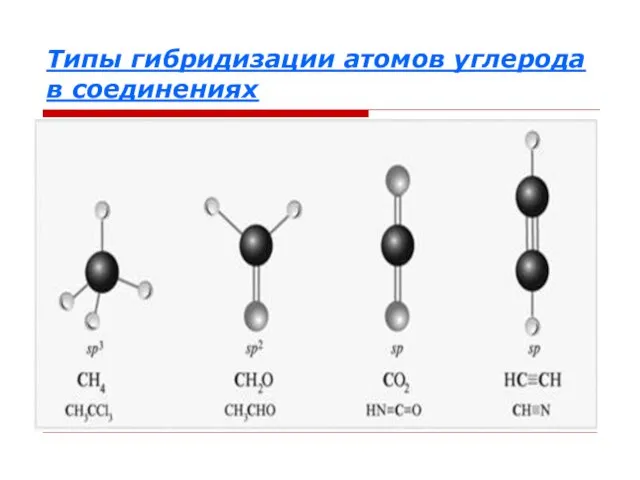
Слайд 30Определите в каком валентном состоянии находится атом углерода?













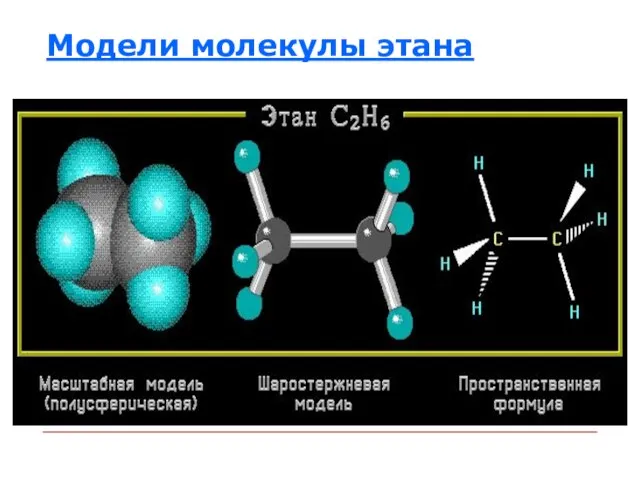
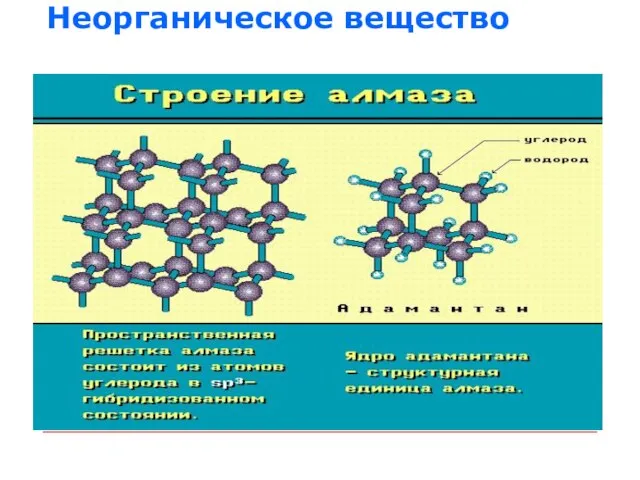

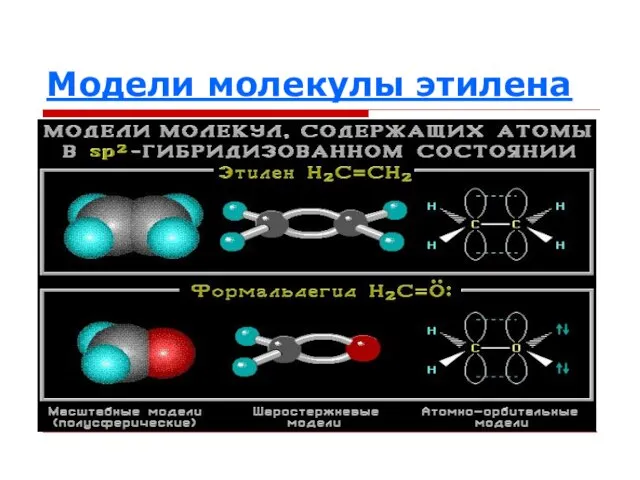



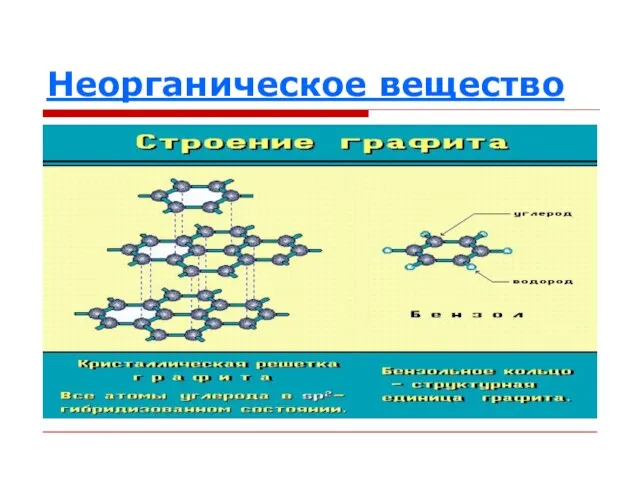






 coffee
coffee Спектакли на этой неделе
Спектакли на этой неделе Виды земляных сооружений
Виды земляных сооружений Типи декларацій
Типи декларацій Сайт бесплатных объявлений Купи.ру
Сайт бесплатных объявлений Купи.ру СПИД -болезнь номер один
СПИД -болезнь номер один В мире басен
В мире басен Применение теоремы Пифагора
Применение теоремы Пифагора Национальный состав России
Национальный состав России Проект Тотальная читка
Проект Тотальная читка Всё успевать
Всё успевать Как решать типичные проблемы стартапов?
Как решать типичные проблемы стартапов? Важность реакции на негатив в социальных медиа
Важность реакции на негатив в социальных медиа Презентация на тему Невидимые друзья и враги: вирусы
Презентация на тему Невидимые друзья и враги: вирусы  Технология составления рабочих программ по учебным предметам и курсам внеурочной деятельности
Технология составления рабочих программ по учебным предметам и курсам внеурочной деятельности Резьба по кости. История появления резьбы по кости
Резьба по кости. История появления резьбы по кости Нефть и нефтепродукты
Нефть и нефтепродукты Предпринимательская деятельность. Факторы производства
Предпринимательская деятельность. Факторы производства Презентация на тему Здоровячок - морячок
Презентация на тему Здоровячок - морячок 4 класс Урок русского языка (программа «Гармония»)
4 класс Урок русского языка (программа «Гармония») Great Patriotic War
Great Patriotic War Смысл жизни
Смысл жизни Поддержка систем дистанционного обучения
Поддержка систем дистанционного обучения Are you as green as grass?
Are you as green as grass? Зона степей
Зона степей Страховая защита и безопасность на транспорте. Перспективы развития законодательства в сфере страхования на транспорте, обязател
Страховая защита и безопасность на транспорте. Перспективы развития законодательства в сфере страхования на транспорте, обязател Периодизация психического развития детей. Возрастные кризы. Типы воспитания
Периодизация психического развития детей. Возрастные кризы. Типы воспитания Количество кружков и секций в БГТЭПТК.
Количество кружков и секций в БГТЭПТК.