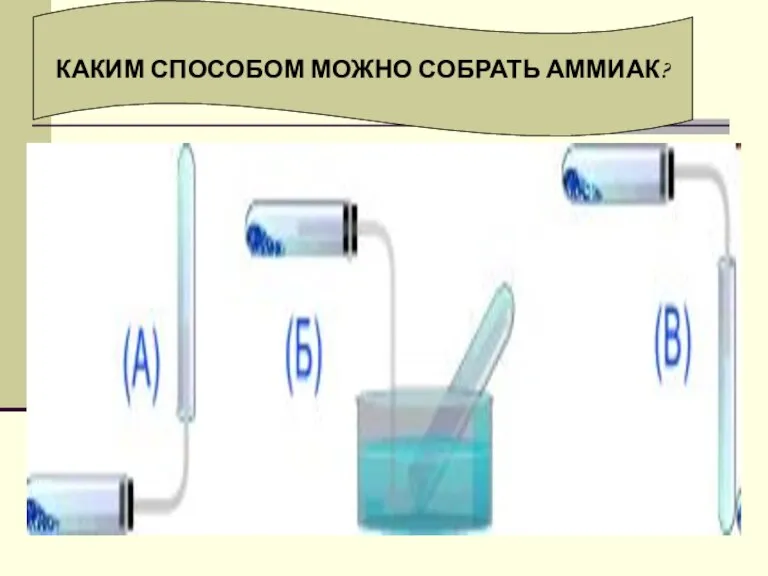
высокую теплоту испарения, он легко сжимается. Хорошо растворим в воде: в 1V Н2O растворяется 750V NH3 (при t°=20°C и p=1 атм)В хорошей растворимости аммиака можно убедиться на следующем опыте. Сухую колбу наполняют аммиаком и закрывают пробкой, в которую вставлена трубка с оттянутым концом. Конец трубки опускают в воду и колбу немного подогревают. Объем газа увеличивается, и немного аммиака выйдет из трубки. Затем нагревание прекращают и, вследствие сжатия газа некоторое количество воды войдет через трубку в колбу. В первых же каплях воды аммиак растворится, в колбе создастся вакуум и вода, под влиянием атмосферного давления будет подниматься в колбу, - начнет "бить фонтан".
Благодаря водородным связям, аммиак имеет сравнительно высокие t°кип. и t°пл., а также высокую теплоту испарения, он легко сжимается. Хорошо растворим в воде: в 1V Н2O растворяется 750V NH3 (при t°=20°C и p=1 атм)В хорошей растворимости аммиака можно убедиться на следующем опыте. Сухую колбу наполняют аммиаком и закрывают пробкой, в которую вставлена трубка с оттянутым концом. Конец трубки опускают в воду и колбу немного подогревают. Объем газа увеличивается, и немного аммиака выйдет из трубки. Затем нагревание прекращают и, вследствие сжатия газа некоторое количество воды войдет через трубку в колбу. В первых же каплях воды аммиак растворится, в колбе создастся вакуум и вода, под влиянием атмосферного давления будет подниматься в колбу, - начнет "бить фонтан".
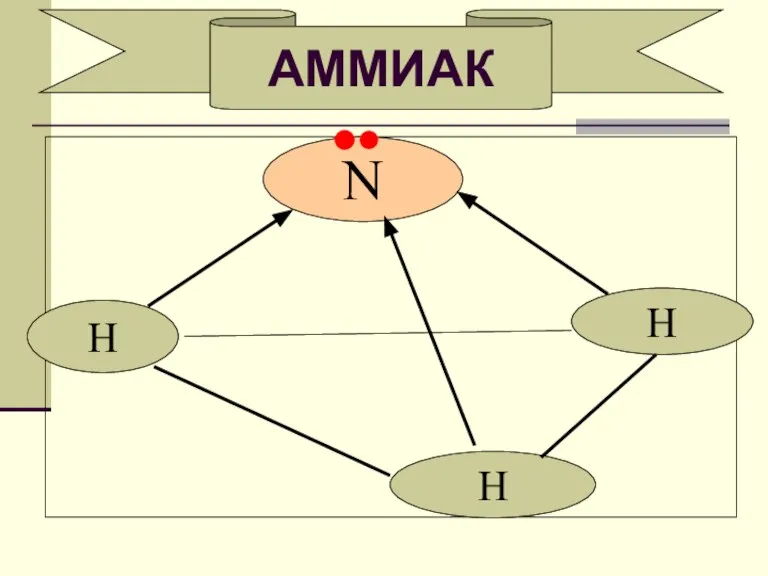
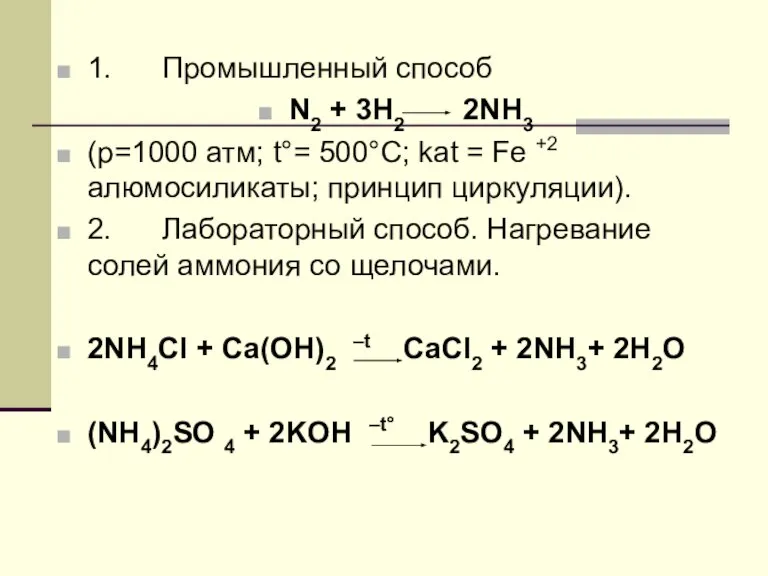
ПОЛУЧЕНИЕ
АММИАКА












 Презентация КС (2)
Презентация КС (2) Подвижные игры с элементы баскетбола на уроках в начальной школе
Подвижные игры с элементы баскетбола на уроках в начальной школе Плавный пуск электродвигателей
Плавный пуск электродвигателей Правонарушения и юридическая ответственность педагога. Лекция 17
Правонарушения и юридическая ответственность педагога. Лекция 17 Неделя истории
Неделя истории Коммуникационная политика в международном маркетинге
Коммуникационная политика в международном маркетинге Презентация на тему Презентация Венгрия
Презентация на тему Презентация Венгрия Алимова Е.Л. МОУ Оленинская СОШ
Алимова Е.Л. МОУ Оленинская СОШ Викторина по физике 7 класс «Первоначальные сведения о строении вещества»
Викторина по физике 7 класс «Первоначальные сведения о строении вещества» Права ребенка
Права ребенка Ценностные основания государственной политики в сфере образования
Ценностные основания государственной политики в сфере образования Лесопарк «Новокосино»
Лесопарк «Новокосино» Организация оценки и анализа рисков на современных предприятиях
Организация оценки и анализа рисков на современных предприятиях Презентация:
Презентация: Психологическое кино
Психологическое кино Решение уравнений, приводимых к квадратным
Решение уравнений, приводимых к квадратным Профилактика наркомании в воспитательном процессе школы
Профилактика наркомании в воспитательном процессе школы Приглашение к участию в тендере ГК «АвтоСпецЦентр»
Приглашение к участию в тендере ГК «АвтоСпецЦентр» Системы линейных алгебраических уравнений. Лекция 2
Системы линейных алгебраических уравнений. Лекция 2 Презентация Microsoft PowerPoint — копия
Презентация Microsoft PowerPoint — копия Rave cosmology (часть 3.6)
Rave cosmology (часть 3.6) Становление российской государственности в XV - XVI в
Становление российской государственности в XV - XVI в Правила видеомонтажа
Правила видеомонтажа Иллюстрация к любимому литературному произведению
Иллюстрация к любимому литературному произведению Композиция Новогодняя
Композиция Новогодняя Презентация на тему Транспорт веществ в растительном организме
Презентация на тему Транспорт веществ в растительном организме  Профессиональное образование
Профессиональное образование Презентация на тему Разноспрягаемые глаголы (6 класс)
Презентация на тему Разноспрягаемые глаголы (6 класс)