Содержание
- 2. Границы между исследованием и обычным лечением Медицинская практика – это воздействие, единственной целью которого является улучшение
- 3. Клинические исследования должны проводиться в соответствии с этическими принципами, базирующимися на Хельсинской Декларации, и соответствовать GCP
- 4. Этический комитет Ethics Committee Независимый орган (на уровне данного учреждения, региональном, национальном или наднациональном уровне), состоящий
- 5. Принципы деятельности комитетов по этике Независимость. Компетентность. Открытость. Плюрализм. Объективность Конфиденциальность
- 6. Функции комитетов по этике Осуществляют функции экспертизы, консультирования, рекомендаций, побуждения, оценки, ориентирования в моральных и правовых
- 7. Обязанности ЭК защищать права, безопасность и здоровье испытуемых. Особое внимание должно быть уделено тем исследованиям, в
- 8. ЭК должны осуществлять свои функции согласно письменным рабочим процедурам и должны хранить всю письменную документацию о
- 9. Процедуры ЭК Определение состава (указываются имена и квалификация членов и официальный орган, учредивший данный комитет). Составление
- 10. Состав ЭК Должен состоять из рационального количества участников (членов), и коллективно обладать квалификацией и опытом, достаточными
- 11. Документы для предоставления в ЭК для осуществления им своих функций: Протоколы исследований, поправки к протоколу, Письменные
- 12. По каждому документу, поступившему в ЭК должен быть вынесен вердикт: положительное заключение; для получения положительного заключения
- 13. У субъектов исследований должно быть достаточно информации, на основании которой они могут принять решение об участии
- 14. Информированное согласие Информированное согласие - процесс добровольного подтверждения пациентом его согласия участвовать в том или ином
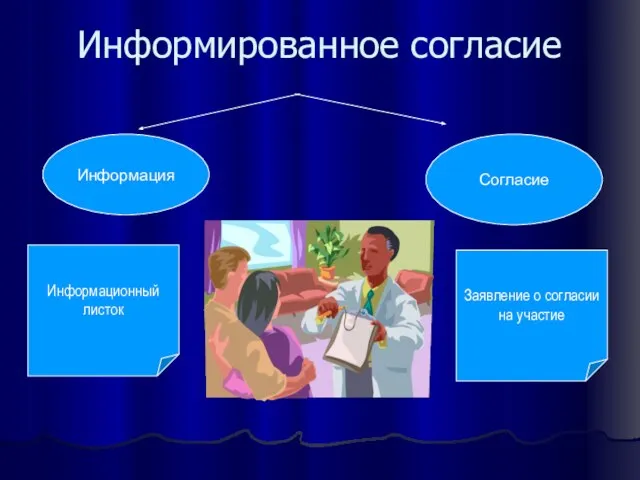
- 15. Информированное согласие Информация Согласие Информационный листок Заявление о согласии на участие
- 16. Основные принципы информированного согласия Испытуемый информирован o целях исследования о методах исследования о лекарственных средствах и
- 17. Информация для испытуемых Информация о цели исследования и его дизайне. Описания предполагаемых риска и неудобств для
- 18. ОСНОВНЫЕ ПРИНЦИПЫ ICH GCP 4.8.11 Испытуемый или его официальный представитель должны получить подписанный и датированный экземпляр
- 19. ИС должно быть получено до любых манипуляции, проводимых для целей исследования! ИС может быть получено только
- 20. Изменения в ИС: Изменения протокола Изменение дозы препарата Изменение количества и вида процедур Новая информация по
- 21. Принятие решения об участии в КИ Пациент должен иметь возможность задать исследователю все интересующие его вопросы,
- 22. Участвуя в клиническом исследовании. Вы, вероятно, сможете: получить доступ к новым видам лечения, которые не доступны
- 23. Клинические исследования имеют следующие неудобства (риски): могут быть побочные эффекты при применении лекарственных средств, лечение может
- 24. Что такое плацебо? Плацебо - это неактивное вещество (таблетка, жидкость, порошок), которое не имеет лечебного эффекта.
- 25. Типичные ошибки, допускаемые при оформлении информированного согласия Отсутствие даты подписания. Не указано время подписания в случае
- 26. Уязвимые категории населения Дети Беременные Люди с психическими отклонениями Экономически или образовательно несостоятельные личности Заключенные Военнослужащие
- 27. FDA Information Sheets. A Guide To Informed Consent. Illiterate English-Speaking Subjects An impartial third party should
- 28. Планирование медицинских исследований с участием детей Не разрешенные к применению, но находящиеся на рассмотрении в установленном
- 29. Исследования на детях Consent form Assent form 6 – 12 13 – 18
- 30. Этические аспекты проведения исследований на женщинах репродуктивного возраста Клинические исследования с участием женщин, которые на момент
- 31. Исследования на людях с нарушением психики В качестве основного правила предполагается, что все взрослые люди, вне
- 32. Бюллетень ВАК министерства образования РФ, М, №3, 2002.-С.73-76. При принятии к рассмотрению и защите диссертаций, тематика
- 34. Скачать презентацию






























 Становление герба Самарской губернии
Становление герба Самарской губернии Франкл: логотерапия. Логотерапия, как терапия смыслом
Франкл: логотерапия. Логотерапия, как терапия смыслом Alla stazione. In carrozza, si parte
Alla stazione. In carrozza, si parte Small talk
Small talk  Русская матрёшка
Русская матрёшка о математике и математиках
о математике и математиках Система менеджмента качестваЧТТПиК 2009-2010
Система менеджмента качестваЧТТПиК 2009-2010 Система менеджмента качества в образовании
Система менеджмента качества в образовании Муниципальное общеобразовательное учреждение средняя общеобразовательная школа №11 г.Вичуга Ивановской области Электронное пр
Муниципальное общеобразовательное учреждение средняя общеобразовательная школа №11 г.Вичуга Ивановской области Электронное пр 1_Лекція Будова атома
1_Лекція Будова атома Гжель. Элементы росписи
Гжель. Элементы росписи БЕТМАН ПРОТИВ ДЖОКЕРА
БЕТМАН ПРОТИВ ДЖОКЕРА Урок как педагогический феномен
Урок как педагогический феномен Театральные маски. Рисуем маску сказочного героя
Театральные маски. Рисуем маску сказочного героя Портфолио Касьяновой Н.А.
Портфолио Касьяновой Н.А. Удивительное начало великой поэмы
Удивительное начало великой поэмы Власова И.В. – старший преподаватель КНО, методист отдела научной работы ГОУ ДПО ЧИПКРО, Почетный работник общего образования Твор
Власова И.В. – старший преподаватель КНО, методист отдела научной работы ГОУ ДПО ЧИПКРО, Почетный работник общего образования Твор Деятельностный подход в образовании
Деятельностный подход в образовании Атом құрылысы туралы жалпы түсінік. Квант сандары
Атом құрылысы туралы жалпы түсінік. Квант сандары Презентация на тему Русские народные танцы
Презентация на тему Русские народные танцы  Тестирование Пользовательского Интерфейсакак это делает Интел
Тестирование Пользовательского Интерфейсакак это делает Интел Институты государственной власти (тема 7)
Институты государственной власти (тема 7) Физика и техника – тебе, фронт!
Физика и техника – тебе, фронт! Известные творческие коллективы Омска
Известные творческие коллективы Омска Christmas Day
Christmas Day Thema: “Wie orientiert man sich in einer fremden Grossstadt?”
Thema: “Wie orientiert man sich in einer fremden Grossstadt?” Применение ИКТ для подготовки к ЕГЭ по математике
Применение ИКТ для подготовки к ЕГЭ по математике Николай Михайлович Карамзин
Николай Михайлович Карамзин