Содержание
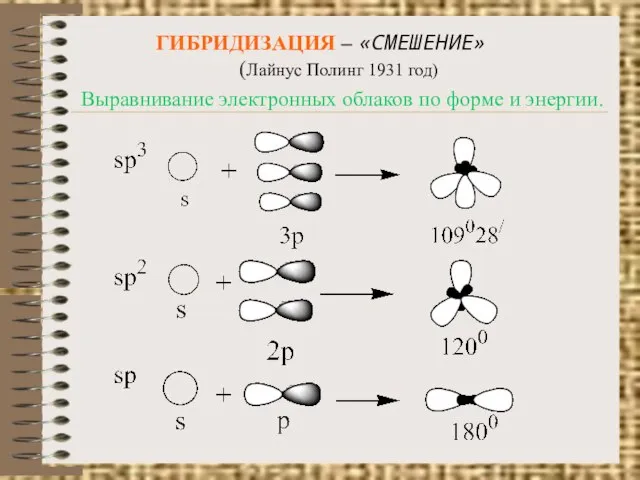
- 2. ГИБРИДИЗАЦИЯ – «СМЕШЕНИЕ» (Лайнус Полинг 1931 год) Выравнивание электронных облаков по форме и энергии.
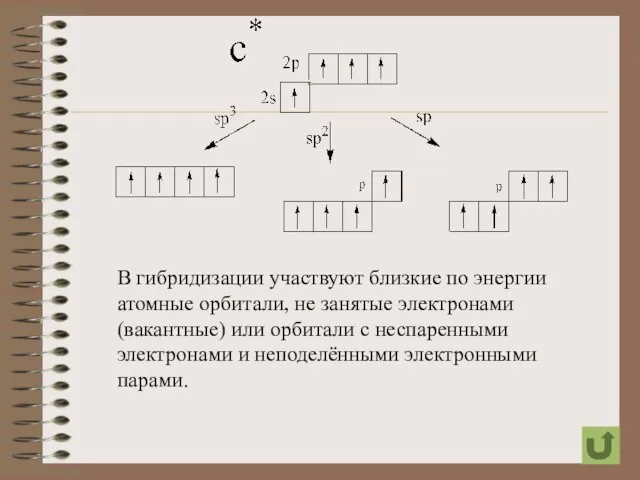
- 3. В гибридизации участвуют близкие по энергии атомные орбитали, не занятые электронами (вакантные) или орбитали с неспаренными
- 4. Определение типа гибридизации на примере молекулы метана. 1.Написать полную структурную формулу вещества. 2.Подсчитать число электронов, предоставляемые
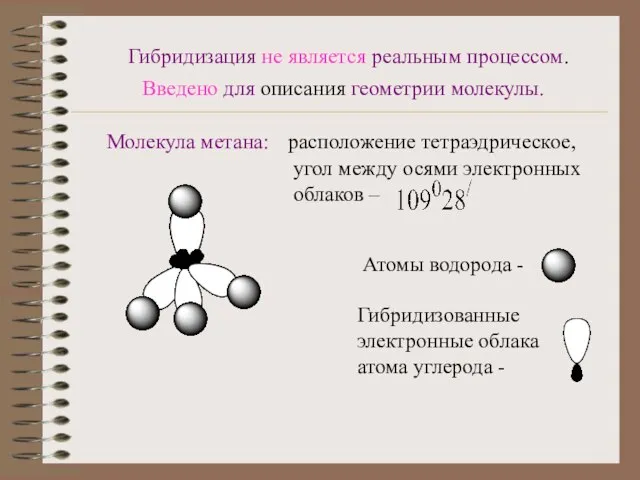
- 5. Гибридизация не является реальным процессом. Введено для описания геометрии молекулы. Молекула метана: расположение тетраэдрическое, угол между
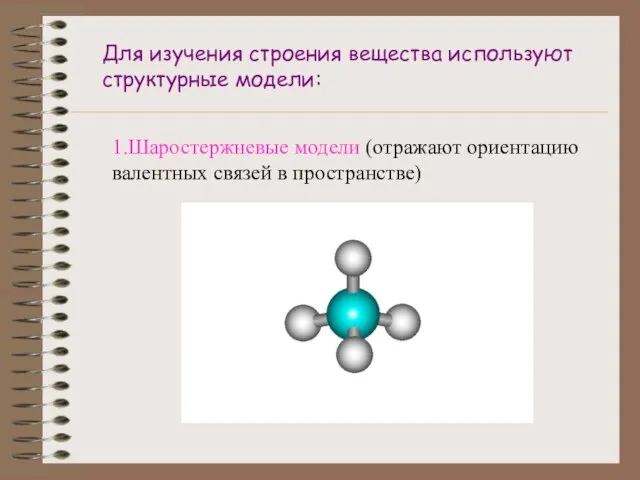
- 6. Для изучения строения вещества используют структурные модели: 1.Шаростержневые модели (отражают ориентацию валентных связей в пространстве)
- 7. Для изучения строения вещества используют структурные модели: 2. Масштабные модели Стюарта-Бриглеба (объёмная)
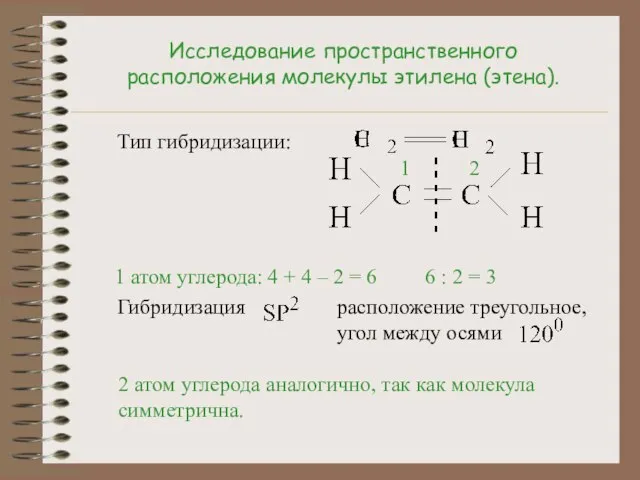
- 8. Исследование пространственного расположения молекулы этилена (этена). Тип гибридизации: 1 атом углерода: 4 + 4 – 2
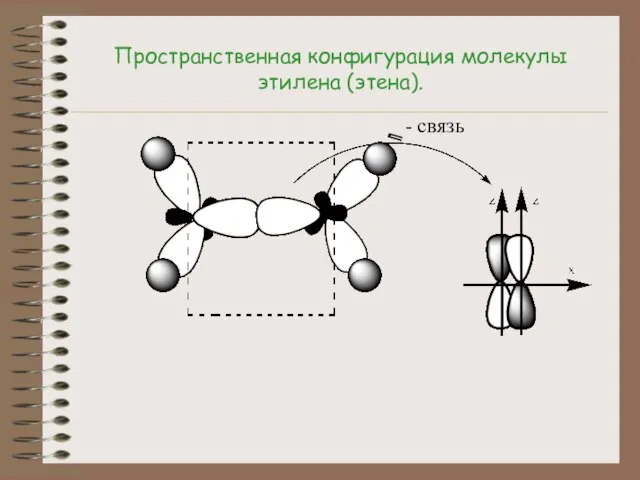
- 9. Пространственная конфигурация молекулы этилена (этена). П - связь
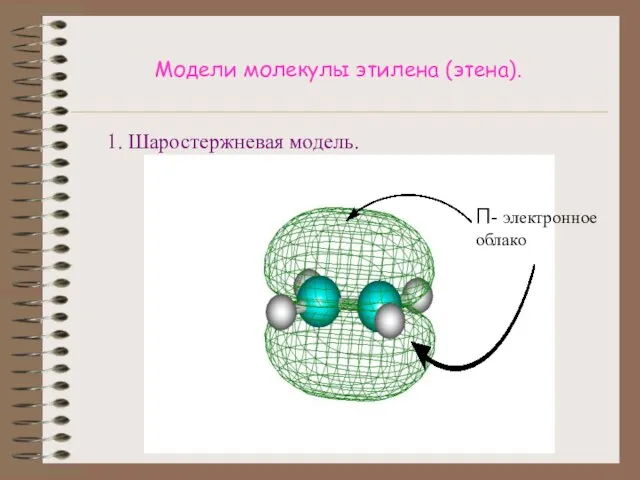
- 10. Модели молекулы этилена (этена). 1. Шаростержневая модель. П- электронное облако
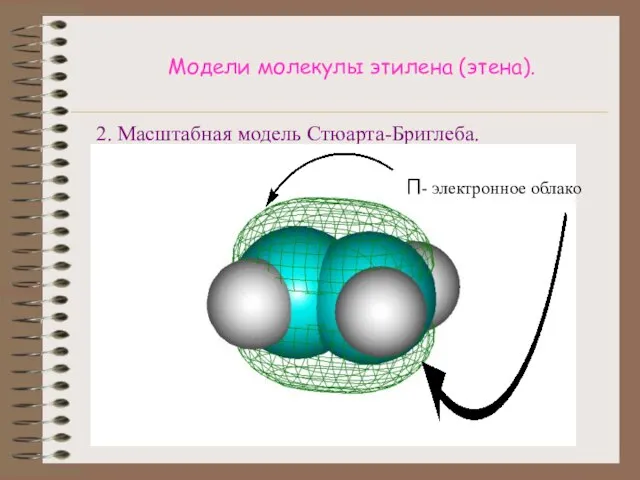
- 11. Модели молекулы этилена (этена). 2. Масштабная модель Стюарта-Бриглеба. П- электронное облако
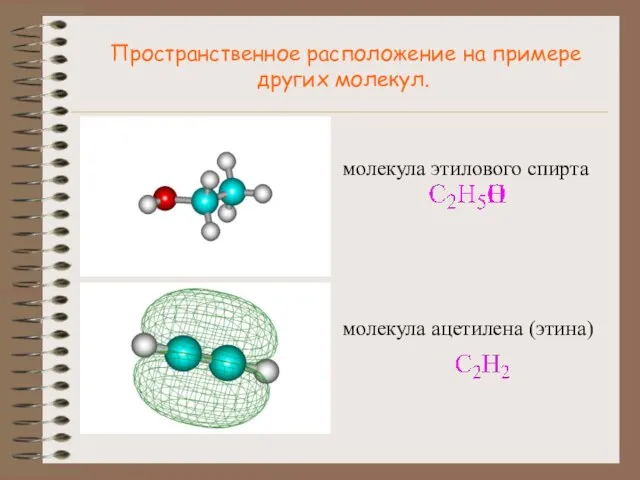
- 12. Пространственное расположение на примере других молекул. молекула этилового спирта молекула ацетилена (этина)
- 14. Скачать презентацию


 1. Доходы
1. Доходы AMANAT INVEST GROUP High Tech Logistic» Ответственное хранение грузов Ответственное хранение грузов Весь спектор операций на складе Весь спектор о
AMANAT INVEST GROUP High Tech Logistic» Ответственное хранение грузов Ответственное хранение грузов Весь спектор операций на складе Весь спектор о Native american boarding schools
Native american boarding schools Цель: выяснить отношение жителей г. Канска к проблеме лесных пожаров Красноярского края.
Цель: выяснить отношение жителей г. Канска к проблеме лесных пожаров Красноярского края. Презентация на тему Азбука города
Презентация на тему Азбука города Язык Рефлекс – диалект Си для программирования ПЛК
Язык Рефлекс – диалект Си для программирования ПЛК Туристический потенциал Балахнинского района
Туристический потенциал Балахнинского района О создании многофункциональных центров предоставления государственных и муниципальных услуг в 2008 году
О создании многофункциональных центров предоставления государственных и муниципальных услуг в 2008 году Дошкольный, школьный и подростковый возраст. Градация детского возраста на группы в СК Планета Фитнес
Дошкольный, школьный и подростковый возраст. Градация детского возраста на группы в СК Планета Фитнес Я и полиция
Я и полиция Различай С - З
Различай С - З Класс Земноводные или Амфибии 7 класс
Класс Земноводные или Амфибии 7 класс Проект Народные инициативы в 2018 году в городе Шелехове
Проект Народные инициативы в 2018 году в городе Шелехове Понятие судебных доказательств
Понятие судебных доказательств Универсальный лазерный гравировальный станок для неметаллов. Wattsan 2030FLAT BED
Универсальный лазерный гравировальный станок для неметаллов. Wattsan 2030FLAT BED Спортивная динейка. Подведение итогов
Спортивная динейка. Подведение итогов МОУ "Аликовская СОШ им. И.Я. Яковлева" Аликовского района Чувашской Республики
МОУ "Аликовская СОШ им. И.Я. Яковлева" Аликовского района Чувашской Республики Пусть меня научат - презентация для начальной школы_
Пусть меня научат - презентация для начальной школы_ Обучение технике ударов по мячу в футболе
Обучение технике ударов по мячу в футболе Понятие и виды деловой карьеры
Понятие и виды деловой карьеры Презентация на тему Славянская мифология
Презентация на тему Славянская мифология  Nanotechnologies: potential benefits or a great danger?
Nanotechnologies: potential benefits or a great danger? Обычно землетрясения происходят вблизи границ литосферных плит. Эти плиты находятся в постоянном движении. Плиты движутся по гори
Обычно землетрясения происходят вблизи границ литосферных плит. Эти плиты находятся в постоянном движении. Плиты движутся по гори Неповторимые, эксклюзивные коллекции ограниченной серии. De Luxe
Неповторимые, эксклюзивные коллекции ограниченной серии. De Luxe Организационная структура страховой компании. Понятие
Организационная структура страховой компании. Понятие СОЧЕТАННЫЕ (СИМУЛЬТАННЫЕ) ОПЕРАЦИИ В ЛАПАРОСКОПИЧЕСКОЙ ХИРУРГИИ
СОЧЕТАННЫЕ (СИМУЛЬТАННЫЕ) ОПЕРАЦИИ В ЛАПАРОСКОПИЧЕСКОЙ ХИРУРГИИ NUMUNE ALIMI ve TRANSFERi
NUMUNE ALIMI ve TRANSFERi Общие положения по монтажу внутренних газопроводов и газоиспользующего оборудования
Общие положения по монтажу внутренних газопроводов и газоиспользующего оборудования