Содержание
- 2. Тема. Вода – вещество №1
- 3. « Вода, у тебя нет ни вкуса, ни запаха, тебя невозможно описать, тобой наслаждаются, не ведая,
- 5. Цели и задачи: 1) дать научное объяснение нормальным и аномальным свойствам воды на основе взаимосвязи между
- 6. Оборудование и реактивы: термос, щипцы, ложечка, хлопчатобумажная ткань, спички, спиртовка, штатив с пробирками, «кристаллическая решётка строения
- 7. Ход урока: Изучение нового материала. (Беседа) Вопросы классу: На какие 2 группы делят вещества? Какие вещества
- 8. Задание классу: Для сложных веществ Для простых веществ Определить степень окисления х/э в следующих веществах: СО2;
- 9. Вопрос: О каком из этих 3-х веществ говорится в загадке? «С горы, сбегая без труда, она
- 10. - Земная гидросфера, сформировавшаяся в ходе длительной геохимической эволюции – эта та часть природы, которой человек
- 11. Вопрос: Какая вода существует в природе? На столе пробирки с образцами Ответы угадывают сами учащиеся: Образцы
- 12. Вывод Дистиллированная вода H2O -химически чистое вещество без примесей. Именно она позволит нам описать свойства вещества,
- 13. Чтобы определить физические свойства воды, проведем игру «Ненужный» Вопрос: Какие агрегатные состояния воды вы знаете? О
- 14. Чтобы знать свойства вещества, необходимо знать его структуру. « Вода- вещество и привычное и необычное. Кажется,
- 15. Задание классу: Задание классу: Используя данные таблицы, постройте графики зависимости температура кипения и температура плавления этих
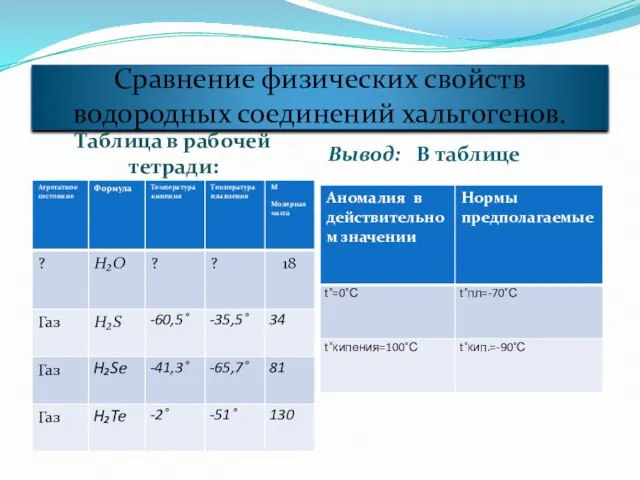
- 16. Сравнение физических свойств водородных соединений хальгогенов. Таблица в рабочей тетради: Вывод: В таблице
- 17. Вопрос: Почему нет соответствия между нормой и действительностью? Смотрим на кристаллическую решетку воды: Молекула воды имеет
- 18. На основании данных таблицы предположите значения удельной теплоемкости. По справочным данным ВОДА имеет удельную теплоемкость в
- 19. Опыт: «Несгораемый платок» Учитель: « Вода, проявляя аномальные свойства, влияет на климат Земли. Невозможно было бы
- 20. Вряд ли о воде можно сказать о воде лучше, чем сказал Антуан Де Сент-Экзюпери в своей
- 22. Завершение урока Заключение: Выполнить задание №8 стр.8( учебная тетрадь) №9, стр.9 Домашнее задание: Повторить §§17-18 Выучить
- 23. Электрическое сопротивление воды в магнитном поле.
- 24. Вода- одно из самых загадочных веществ нашей планеты. Главной задачей, стоящей перед физиками и химиками при
- 25. Электрические свойства воды. Удельное электрическое сопротивление воды существенно зависит от температуры. Минерализация воды резко понижает её
- 26. Под действием внешнего магнитного поля электрическое сопротивление вещества может увеличиваться и уменьшаться. Наиболее простой механизм появления
- 27. Длина свободного пробега в магнитном поле уменьшается . Уменьшение длины свободного пробега приводит к увеличению сопротивления.
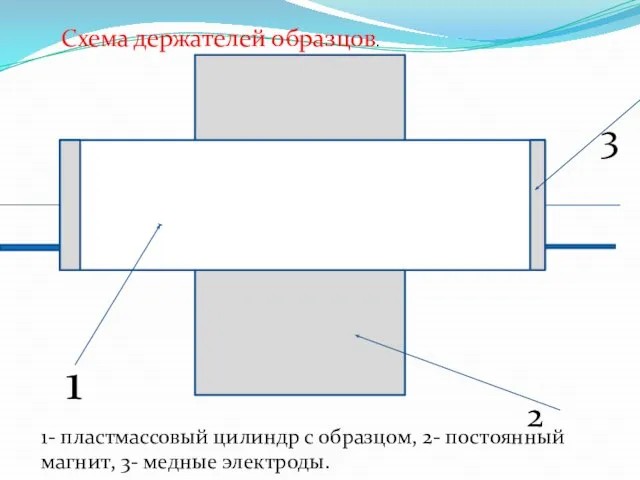
- 28. Изготовление установки. Держатель образцов представляет собой полный пластмассовый цилиндр с впаянными в торцы медными электродами диаметром
- 29. 1- пластмассовый цилиндр с образцом, 2- постоянный магнит, 3- медные электроды. 1 2 3 Схема держателей
- 30. Экспериментальные результаты. 1. Приготовление образцов. Пробы воды предназначенные для изучения магнитосопротивления воды, приготавливались по следующей технологии.
- 31. Результаты измерения Измерение сопротивления образцов проводилось с помощью характериографа путём получения вольтамперной характеристики. Сначала измерялось сопротивление
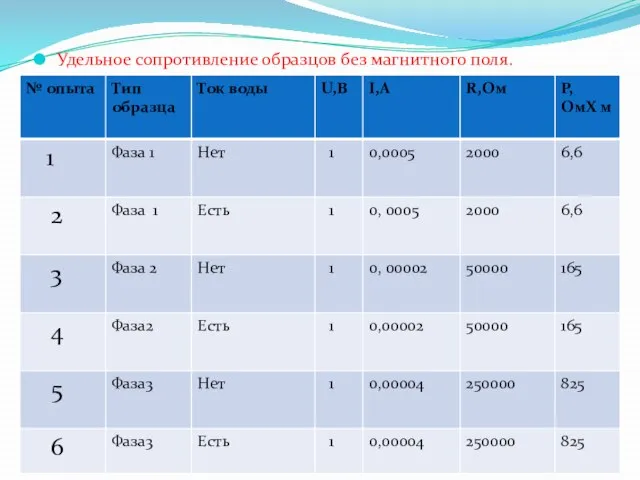
- 32. Удельное сопротивление образцов без магнитного поля.
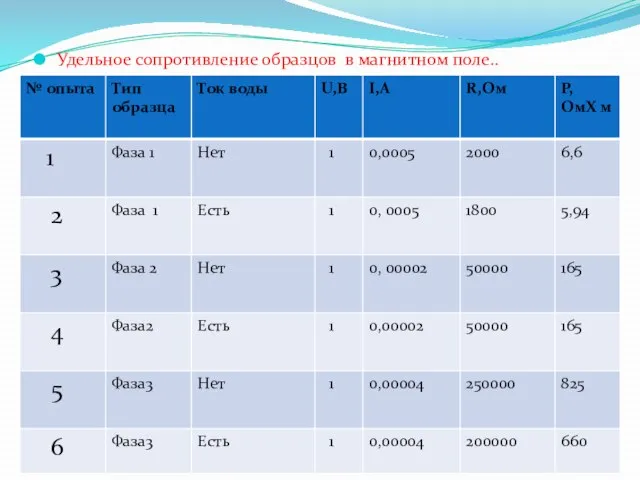
- 33. Удельное сопротивление образцов в магнитном поле..
- 34. Анализируя результаты вышеуказанной таблицы пришли к выводу, что магнитное поле незначительно влияет на сопротивление воды, движущейся
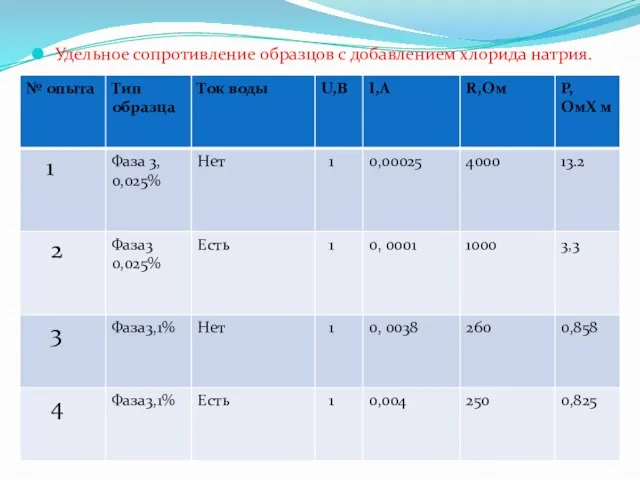
- 35. Удельное сопротивление образцов с добавлением хлорида натрия.
- 36. Повторные значения сопротивления через двое суток несколько отличаются, но влияние магнитного поля оказалось не таким существенным.
- 37. Заключение. В ходе выполнения представленной работы были проведены эксперименты по обнаружению зависимости магнитосопротивления воды от внешнего
- 38. Выводы: 1. При высоких сопротивлениях образцов магнитосопротивление не изменяется. 2. При введение в образцы хлорида натрия
- 39. Список использованной литературы. Современные проблемы физики твёрдого тела и биофизики- сборник научных трудов.-Киев:Наука, 1982-с.272. 2.Электрические свойства
- 40. Заключение. В ходе выполнения представленной работы были проведены эксперименты по обнаружению зависимости магнитосопротивления воды от внешнего
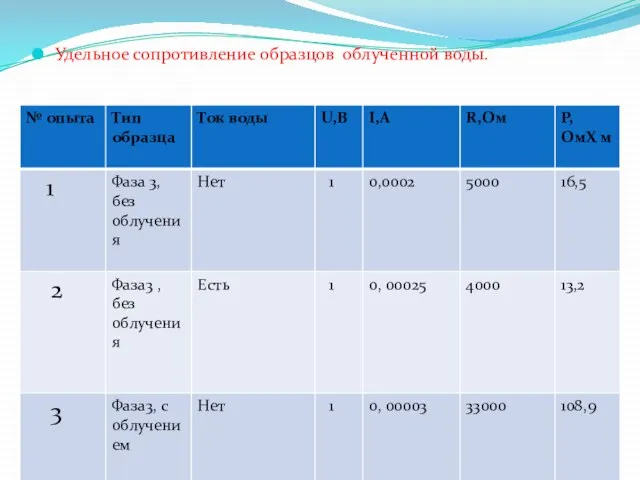
- 41. Удельное сопротивление образцов облученной воды.
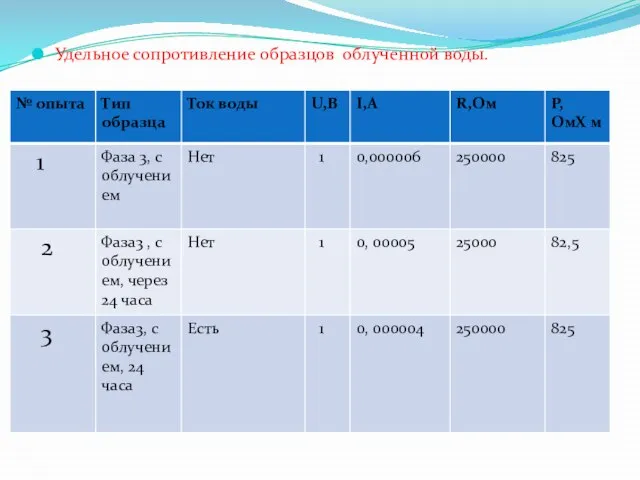
- 42. Удельное сопротивление образцов облученной воды.
- 43. Полученные результаты показывают, что изменения магнитосопротивления более существенны для менее концентрированного раствора хлорида натрия. Далее нами
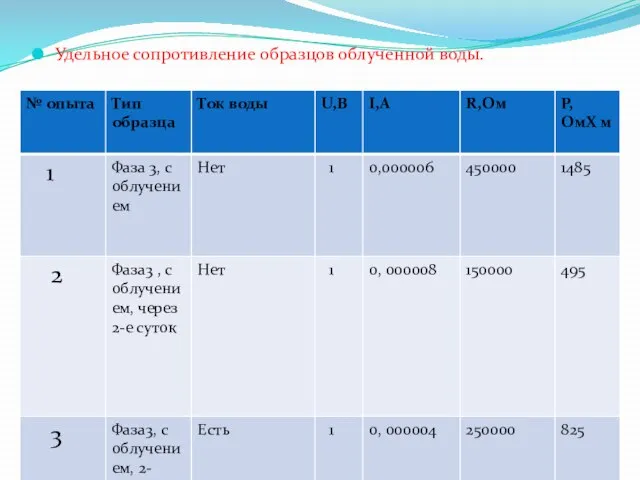
- 44. Удельное сопротивление образцов облученной воды.
- 46. Скачать презентацию



































 Операционная система персонального компьютера
Операционная система персонального компьютера Католицизм: кнут и пряник
Католицизм: кнут и пряник Презентация на тему тренажер по английскому языку
Презентация на тему тренажер по английскому языку Публичный докладдиректора школы МОУ “СОШ № 10” Н.А. Давыдовой г.Биробиджан, ЕАО
Публичный докладдиректора школы МОУ “СОШ № 10” Н.А. Давыдовой г.Биробиджан, ЕАО Декларации пожарной безопасности
Декларации пожарной безопасности  Презентация на тему: Бородинская панорама
Презентация на тему: Бородинская панорама Заседание Совета кураторов
Заседание Совета кураторов Нутромер оборудование для измерения диаметра внутренних полостей
Нутромер оборудование для измерения диаметра внутренних полостей Music
Music Устройство увеличительных приборов. Строение клетки
Устройство увеличительных приборов. Строение клетки Реклама новых книг
Реклама новых книг Роль точечных мутаций гена RUNX1 в патогенезе миелодиспластических и миелопролиферативных заболеваний у детей
Роль точечных мутаций гена RUNX1 в патогенезе миелодиспластических и миелопролиферативных заболеваний у детей FLEXWORK project materials and their use in TELESOL
FLEXWORK project materials and their use in TELESOL Презентация на тему ПРИНЦИП ГЮЙГЕНСА. ЗАКОН ОТРАЖЕНИЯ СВЕТА
Презентация на тему ПРИНЦИП ГЮЙГЕНСА. ЗАКОН ОТРАЖЕНИЯ СВЕТА Выдающаяся личность
Выдающаяся личность урок
урок Презентация услуг компании «ГЛОБАЛ КОНСАЛТИНГ»
Презентация услуг компании «ГЛОБАЛ КОНСАЛТИНГ» Храм Святой Софии в Константинополе
Храм Святой Софии в Константинополе Сечение ударной электронной ионизации. Оже-электроны
Сечение ударной электронной ионизации. Оже-электроны Россия на политической карте мира. Особенности развития на современном этапе
Россия на политической карте мира. Особенности развития на современном этапе Животные и растения Северной Америки
Животные и растения Северной Америки Иконки автомобильные
Иконки автомобильные The dark matter power complex
The dark matter power complex Система академика Л.Занкова
Система академика Л.Занкова “Практика внедрения международного стандарта ISО 14001 в ОАО “Концерн Стирол”
“Практика внедрения международного стандарта ISО 14001 в ОАО “Концерн Стирол” АООП НОО для обучающихся с НОДА
АООП НОО для обучающихся с НОДА Лига Индиго. Интеллектуально-развлекательная игра. Разрыв шаблона о корпоративных праздниках
Лига Индиго. Интеллектуально-развлекательная игра. Разрыв шаблона о корпоративных праздниках Компания МИКРОБОР НАНОТЕХ
Компания МИКРОБОР НАНОТЕХ