Слайд 2
Простые вещества. Молекулы состоят из атомов одного вида (атомов одного элемента). В
химических реакциях не могут разлагаться с образованием других веществ.
Сложные вещества (или химические соединения). Молекулы состоят из атомов разного вида (атомов различных химических элементов). В химических реакциях разлагаются с образованием нескольких других веществ.
Неорганические вещества
Простые
Металлы
Неметаллы
Сложные
Оксиды
Основания
Кислоты
Соли
Слайд 4Оксиды - это сложные вещества, состоящие из двух элементов, один из которых

кислород.
Слайд 5ОКСИДЫ
Классификация
Оксиды - это сложные вещества, состоящие из двух элементов, один из которых

кислород.
ОКСИДЫ
Несолеобразующие
CO, N2O, NO
Солеобразующие
Основные
-это оксиды металлов, в которых последние проявляют небольшую степень окисления +1, +2
Na2O; MgO; CuO
Амфотерные
(обычно для металлов со степенью окисления +3, +4). В качестве гидратов им соответствуют амфотерные гидроксиды
ZnO; Al2O3; Cr2O3; SnO2
Кислотные
-это оксиды неметаллов и металлов со степенью окисления от +5 до +7
SO2; SO3; P2O5; Mn2O7; CrO3
Основным оксидам соответствуют основания,
кислотным – кислоты,
амфотерным – и те и другие
Слайд 6Получение
1. Взаимодействие простых и сложных веществ с кислородом:
2Mg + O2 = 2MgO
4P

+ 5O2 =2P2O5
S + O2 = SO2
2CO + O2 =2CO2
2CuS + 3O2= 2CuO + 2SO2
CH4 + 2O2 = CO2 + 2H2O
4NH3 + 5O2 = 4NO + 6H2O
2. Разложение некоторых кислородсодержащих веществ (оснований, кислот, солей) при нагревании:
Cu(OH)2 = CuO + H2O
(CuOH)2CO3 = 2CuO + CO2 + H2O
2Pb(NO3)2 = 2PbO + 4NO2 + O2
2HMnO4 = Mn2O7 + H2O
Слайд 7Химические свойства
Основные оксиды
1. Взаимодействие с водой
Образуется основание:Na2O + H2O =2NaOH
CaO + H2O

= Ca(OH)2
2. Взаимодействие с кислотой или основанием:
При реакции с кислотой образуется соль и вода
MgO + H2SO4 = MgSO4 + H2O
CuO + 2HCl = CuCl2 + H2O
Слайд 8Кислотные оксиды
1. Взаимодействие с водой
Образуется кислота:
SO3 + H2O =H2SO4
P2O5 + 3H2O =2H3PO4
2.

Взаимодействие с кислотой или основанием:
При реакции с основанием образуется соль и вода
CO2 + Ba(OH)2 = BaCO3 + H2O
SO2 + 2NaOH = Na2SO3 + H2O
Слайд 9Амфотерные оксиды
Амфотерные оксиды взаимодействуют
с кислотами как основные:
ZnO + H2SO4 =ZnSO4 + H2O
с

основаниями как кислотные:
ZnO + 2NaOH = Na2ZnO2 + H2O(ZnO + 2NaOH + H2O =Na2[Zn(OH)4])
3. Взаимодействие основных и кислотных оксидов между собой приводит к солям.Na2O + CO2 ® Na2CO34.
Восстановление до простых веществ:3CuO + 2NH3 = 3Cu + N2 + 3H2O
P2O5 + 5C = 2P + 5CO
Слайд 11КИСЛОТЫ
Кислоты - сложные вещества, состоящие из атомов водорода и кислотного остатка. (С

точки зрения теории электролитической диссоциации: кислоты - электролиты, которые при диссоциации в качестве катионов образуют только H+).
Слайд 13ОСНОВАНИЯ
Основания - сложные вещества, в которых атомы металлов соединены с одной или

несколькими гидроксильными группами (с точки зрения теории электролитической диссоциации, основания - сложные вещества, при диссоциации которых в водном растворе образуются катионы металла (или NH4+) и гидроксид - анионы OH-).
Слайд 14Классификация.
Растворимые в воде (щёлочи) и нерастворимые.
Амфотерные основания проявляют также свойства слабых

кислот.
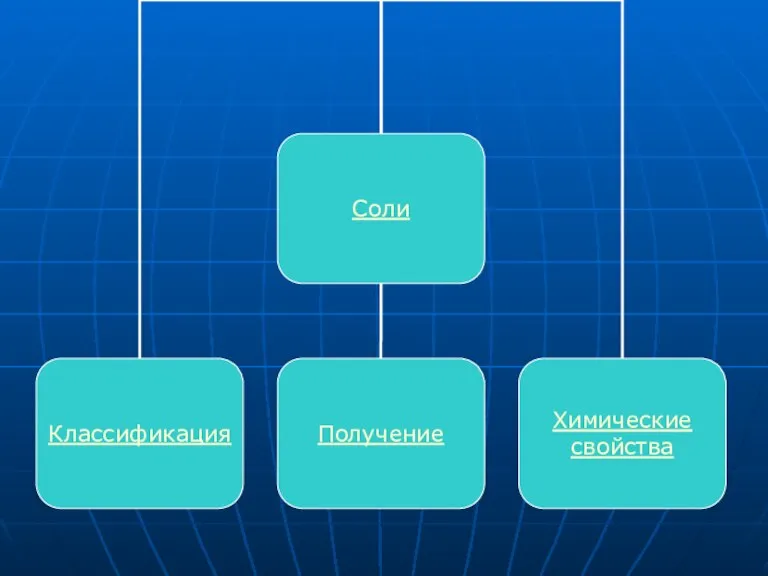
Слайд 16СОЛИ
Соли - сложные вещества, которые состоят из атомов металла и кислотных остатков.

Это наиболее многочисленный класс неорганических соединений.
Слайд 18ГЕНЕТИЧЕСКАЯ СВЯЗЬ
МЕЖДУ РАЗЛИЧНЫМИ
КЛАССАМИ
СОЕДИНЕНИЙ













 Круглый стол для потенциальных участников закупки работ по СМР для АО НК Конданефть
Круглый стол для потенциальных участников закупки работ по СМР для АО НК Конданефть Что такое Пассивный доход
Что такое Пассивный доход Презентация на тему Садоводство и виноградарство
Презентация на тему Садоводство и виноградарство  Зачем региональной компании перестраховщик
Зачем региональной компании перестраховщик Магазин IT- услуг
Магазин IT- услуг Презентация на тему Осторожно - электроприборы!
Презентация на тему Осторожно - электроприборы! Процедуры и функции. Модули
Процедуры и функции. Модули Дарите нужные подарки!
Дарите нужные подарки! Организм человека
Организм человека 1.3.2. Определение количества информации.
1.3.2. Определение количества информации. СОТРУДНИЧЕСТВО С КНР ОПЫТ ВТБ МАРТ 2011
СОТРУДНИЧЕСТВО С КНР ОПЫТ ВТБ МАРТ 2011 Бурый медведь 2 класс
Бурый медведь 2 класс Презентация на тему Учим словарь со смешариками 1 класс
Презентация на тему Учим словарь со смешариками 1 класс Приемы умножения единицы и нуля.
Приемы умножения единицы и нуля. Учебный курс. Технологии и средства разработки корпоративных систем. Основные возможности корпоративных приложений
Учебный курс. Технологии и средства разработки корпоративных систем. Основные возможности корпоративных приложений Занятие по развитию речи «Каникулы»
Занятие по развитию речи «Каникулы» МОРФОЛОГИЧЕСКАЯ ХАРАКТЕРИСТИКА СЛОВА
МОРФОЛОГИЧЕСКАЯ ХАРАКТЕРИСТИКА СЛОВА Проблемы криптопреступности и способы их решения
Проблемы криптопреступности и способы их решения Новогодняя настольная лампа "Ночь перед Рождеством"
Новогодняя настольная лампа "Ночь перед Рождеством" Development Leadership Skills
Development Leadership Skills Monash Road, Loganlea
Monash Road, Loganlea Социальная структура общества
Социальная структура общества  ПЕРСПЕКТИВЫ МЕДИЦИНСКОГО ОБРАЗОВАНИЯ В РОССИИ: НОВЫЕ ОБРАЗОВАТЕЛЬНЫЕ СТАНДАРТЫ.
ПЕРСПЕКТИВЫ МЕДИЦИНСКОГО ОБРАЗОВАНИЯ В РОССИИ: НОВЫЕ ОБРАЗОВАТЕЛЬНЫЕ СТАНДАРТЫ. Комикс «Самая скорая помощь» Переохлаждение в воде
Комикс «Самая скорая помощь» Переохлаждение в воде Как стать сказочником?
Как стать сказочником? Технологии и продукты Microsoft в обеспечении ИБ
Технологии и продукты Microsoft в обеспечении ИБ Вышивка тамбурным швом
Вышивка тамбурным швом Книжная полка
Книжная полка