Содержание
- 2. В настоящее время мы являемся свидетелями разрушения архитектурных сооружений и конструкций. От кислотных дождей катастрофически страдают
- 3. Слово коррозия происходит от латинского corrodere, что означает разъедать. Коррозией называют самопроизвольный процесс разрушения материалов и
- 4. КОРРОЗИЯ - РЖАВАЯ КРЫСА, ГРЫЗЕТ МЕТАЛЛИЧЕСКИЙ ЛОМ, В ШЕФНЕР 4Fe + 6H2O + 3O2 = 4Fe(OH)3
- 5. Виды коррозии Химическая Электрохимическая
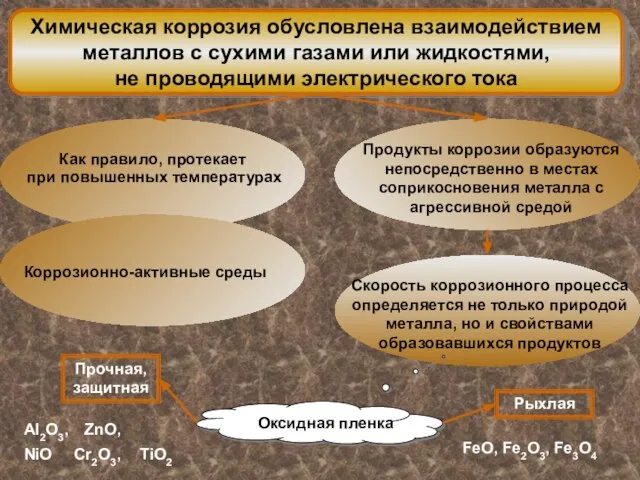
- 6. Химическая коррозия обусловлена взаимодействием металлов с сухими газами или жидкостями, не проводящими электрического тока Прочная, защитная
- 7. Электрохимическая коррозия осуществляется за счет электрохимических реакций, происходящих на поверхности металла, находящегося в контакте с раствором
- 9. Электрохимический ряд напряжений металлов Li, K, Ba, Ca, Na, Mg, Al, Mn, Zn, Cr, Fe, Ni,
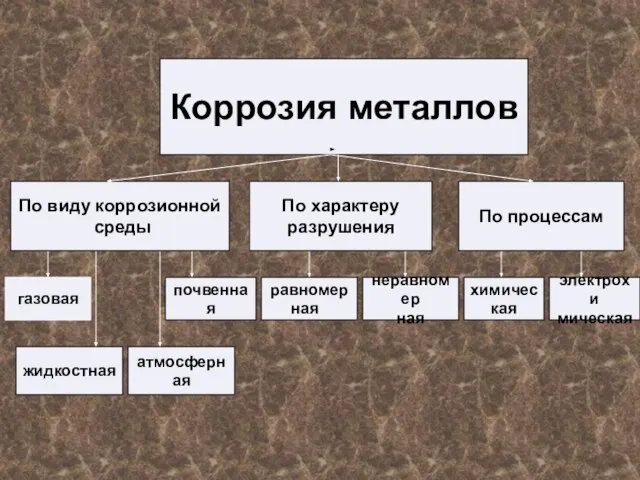
- 10. Коррозия металлов СПЛОШНАЯ МЕСТНАЯ не представляет особой опасности для конструкций и аппаратов особенно в тех случаях,
- 11. Коррозия металлов
- 12. Виды защиты от коррозии Протекторная Создание сплавов, стойких к коррозии Защита поверхности металла покрытиями Подавление влияния
- 16. Скачать презентацию











 образы физического мира
образы физического мира ТРЕТЬЕ ТЫСЯЧЕЛЕТИЕ
ТРЕТЬЕ ТЫСЯЧЕЛЕТИЕ Итоги работы секции языкознания: было представлено 5 работ.
Итоги работы секции языкознания: было представлено 5 работ. Расчет центровки, загрузки в транспортном и пассажирском вариантах. Подготовка к полету. Занятие № 4
Расчет центровки, загрузки в транспортном и пассажирском вариантах. Подготовка к полету. Занятие № 4 Смена дня и ночи
Смена дня и ночи Эффективность использования гречневой крупы при производстве мясорастительных рубленых полуфабрикатов
Эффективность использования гречневой крупы при производстве мясорастительных рубленых полуфабрикатов Васильева Любовь Геннадьевна, учитель экономики МАОУ «Бронницкая СОШ»
Васильева Любовь Геннадьевна, учитель экономики МАОУ «Бронницкая СОШ» Значение растений и их охрана
Значение растений и их охрана Тенденция использования сексуальных мотивов
Тенденция использования сексуальных мотивов Система трудовой подготовки в школе
Система трудовой подготовки в школе Съедобные и несъедобные грибы
Съедобные и несъедобные грибы Свято-Георгиевский храм. Иконостас
Свято-Георгиевский храм. Иконостас Занятие 3Что надо знать о питании при ожирении
Занятие 3Что надо знать о питании при ожирении АГ-Икс AG-X
АГ-Икс AG-X Покорение Сибирского ханства
Покорение Сибирского ханства КВН «Ох, уж эта математика!»
КВН «Ох, уж эта математика!» Игра«Морской бой»
Игра«Морской бой» Seasons and weather
Seasons and weather Seasons
Seasons Две столицы – два стиля модерн
Две столицы – два стиля модерн  Тип речи – описание
Тип речи – описание Сувенирный бутик. Бизнес – проект
Сувенирный бутик. Бизнес – проект Залоги в современной практике кредитования
Залоги в современной практике кредитования Виды стежков и строчек
Виды стежков и строчек Электрический привод. Асинхронный электропривод
Электрический привод. Асинхронный электропривод Додрукарські_просеси_поліграфічного_виробництва
Додрукарські_просеси_поліграфічного_виробництва Значение физической культуры и спорта в жизни человека
Значение физической культуры и спорта в жизни человека ФОРМИРОВАНИЕ ОРГАНИЗАЦИОННЫХ СТРУКТУР ТЕАТРАЛЬНЫХ ОРГАНИЗАЦИЙ В УСЛОВИЯХ РЫНОЧНОЙ ЭКОНОМИКИ
ФОРМИРОВАНИЕ ОРГАНИЗАЦИОННЫХ СТРУКТУР ТЕАТРАЛЬНЫХ ОРГАНИЗАЦИЙ В УСЛОВИЯХ РЫНОЧНОЙ ЭКОНОМИКИ