Содержание
- 2. Биохимия Факультет физической культуры и спорта Направление «Физическая культура» Т. Н. Замай
- 3. УДК 577.1 ББК 28.072 З-26 Электронный учебно-методический комплекс по дисциплине «Биохимия» подготовлен в рамках реализации в
- 4. Оглавление ЧАСТЬ 1. Статическая биохимия ЧАСТЬ 2. Динамическая биохимия ЧАСТЬ 3. Спортивная биохимия
- 5. БИОХИМИЯ ЧАСТЬ 1 Статическая биохимия. Строение, свойства, биологическая роль углеводов и липидов
- 6. Оглавление 1.1. Строение, свойства, биологическая роль углеводов и липидов 1.2. Строение, свойства, биологическая роль белков 1.3.
- 7. 1.1. Строение, свойства, биологическая роль углеводов и липидов
- 8. Механизмы преобразования энергии в организме человека при мышечной деятельности. Регуляция синтеза белка при мышечной нагрузке. Механизмы
- 9. Выявление и оценка биохимических факторов, лимитирующих уровень спортивных достижений; Изучение биохимических сдвигов у спортсменов в процессе
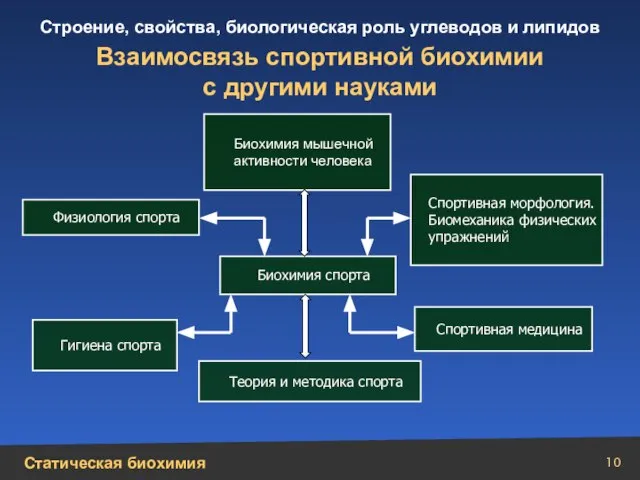
- 10. Биохимия спорта Биохимия мышечной активности человека Теория и методика спорта Физиология спорта Гигиена спорта Спортивная морфология.
- 11. Первая важная аксиома молекулярной логики живого: живые организмы создают и поддерживают присущую им упорядоченность за счет
- 12. Энергетическая функция (главный вид клеточного топлива). Структурная функция (обязательный компонент большинства внутриклеточных структур). Защитная функция (участие
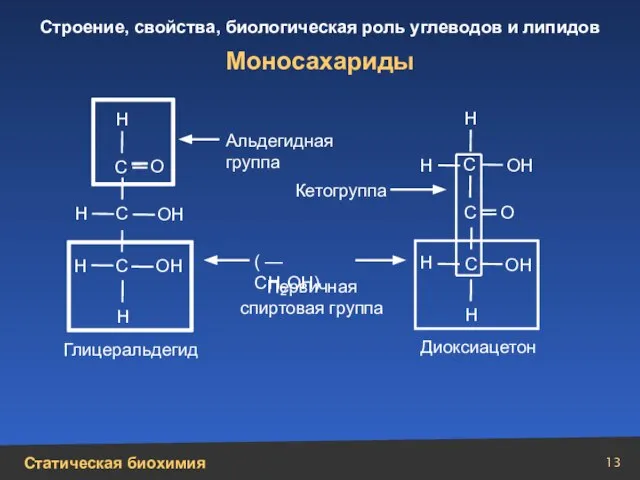
- 13. Моносахариды Н Н Н Н Н Н Н Н ОН ОН ОН ОН О О (
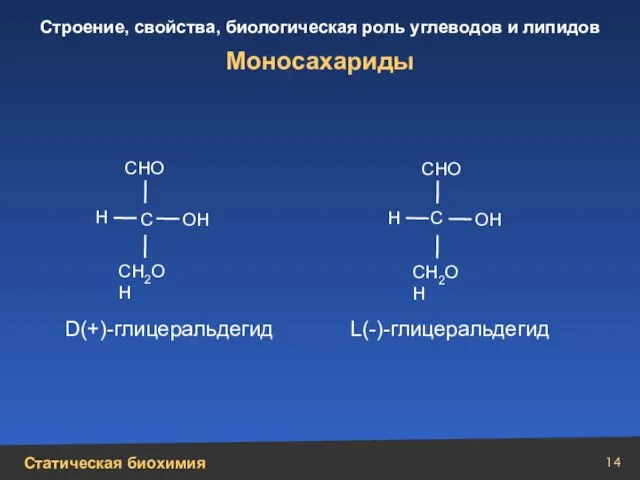
- 14. Моносахариды Н Н ОН ОН С С СН2ОН СН2ОН СНО СНО D(+)- глицеральдегид L(-)- глицеральдегид
- 15. Энантиомеры НСОН НСОН НСОН НСОН НОСН НОСН НОСН НОСН СН2ОН СН2ОН СНО СНО D- глюкоза L-
- 16. Представители моносахаридов НСОН НСОН НСОН НСОН НСОН НОСН С О СН2ОН СН2ОН СН2ОН СНО D- фруктоза
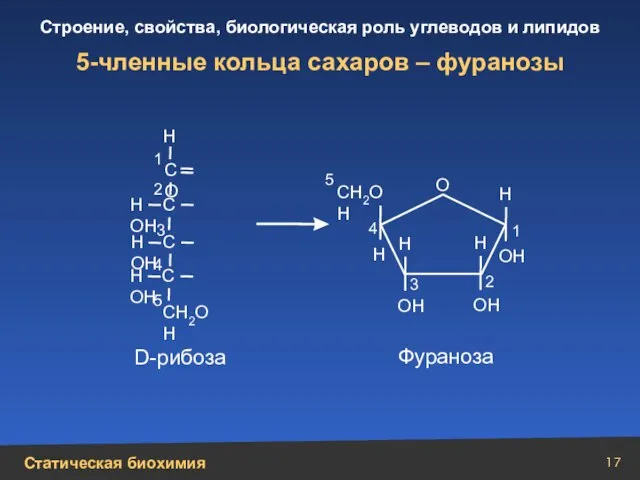
- 17. 5-членные кольца сахаров – фуранозы Н С ОН Н С ОН Н С ОН СН2ОН СН2ОН
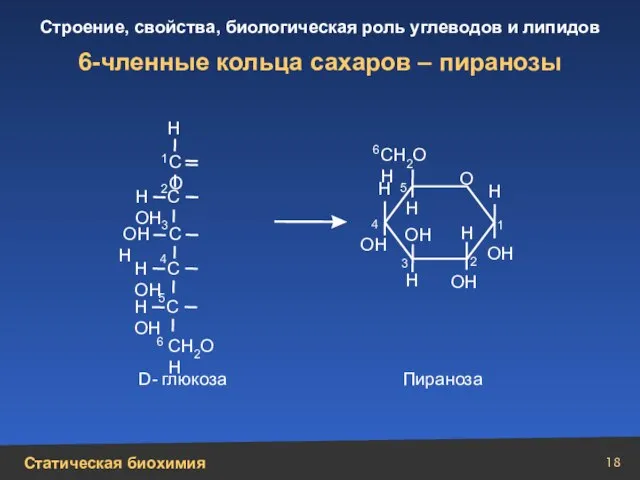
- 18. 6-членные кольца сахаров – пиранозы Н С ОН ОН С Н Н С ОН Н С
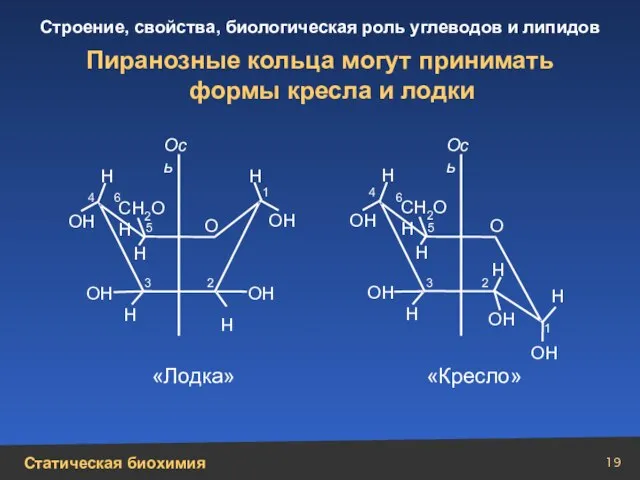
- 19. Пиранозные кольца могут принимать формы кресла и лодки СН2ОН СН2ОН Н Н Н Н Н Н
- 20. Олигосахариды Глюкоза + Глюкоза = Мальтоза Глюкоза + Галактоза = Лактоза Глюкоза + Фруктоза = Сахароза
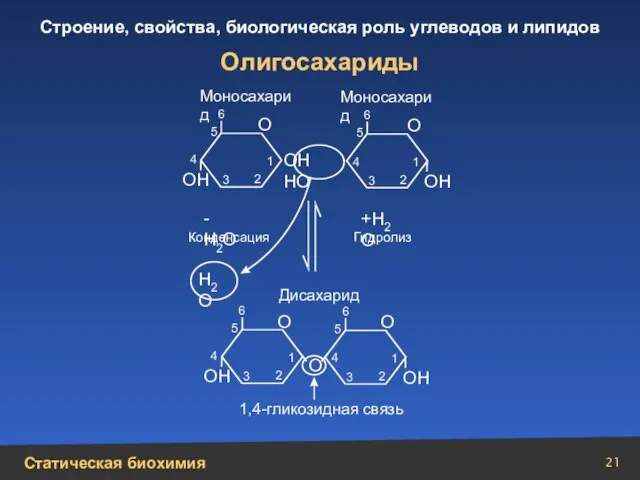
- 21. Олигосахариды ОН НО О ОН ОН ОН ОН О О О О 1 1 1 1
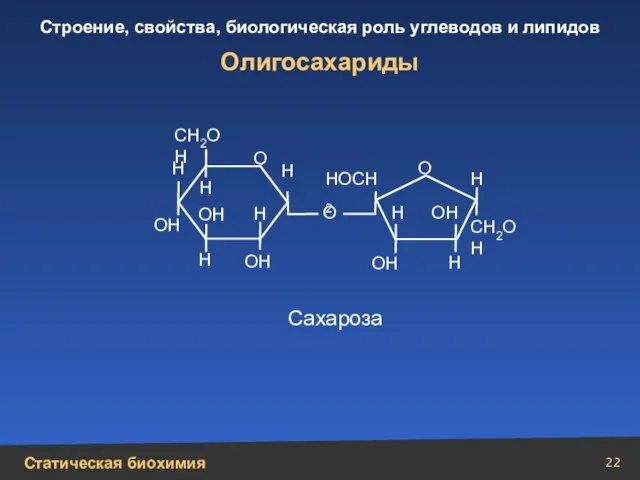
- 22. Олигосахариды СН2ОН СН2ОН НОСН2 Н Н Н Н Н Н Н О Н ОН ОН ОН
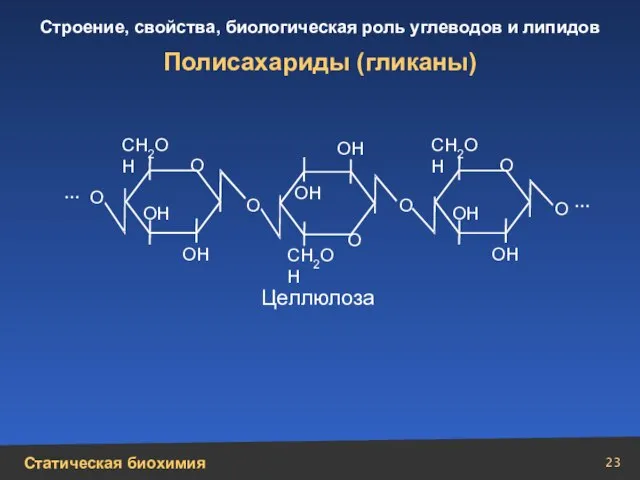
- 23. Полисахариды (гликаны) СН2ОН СН2ОН СН2ОН О О О О ОН ОН ОН ОН ОН ОН О
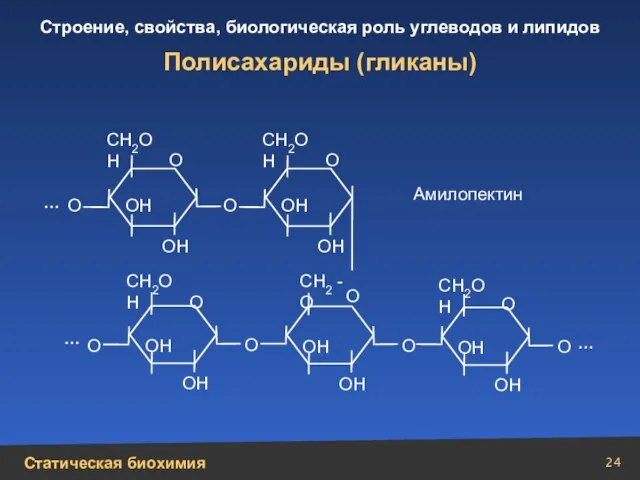
- 24. Полисахариды (гликаны) СН2ОН СН2ОН СН2ОН СН2 -О СН2ОН О О О О О О ОН ОН
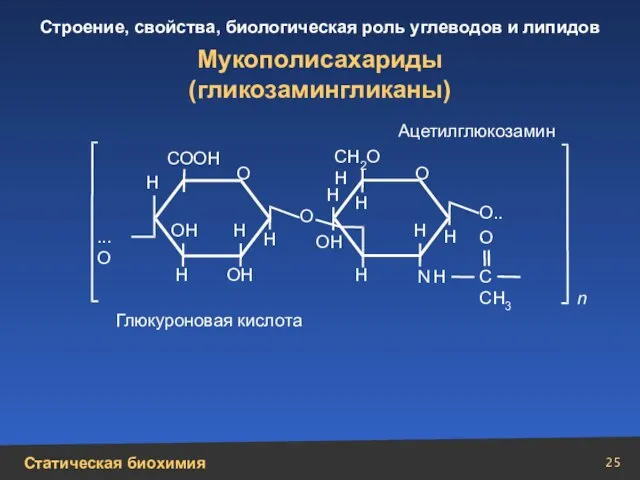
- 25. Мукополисахариды (гликозамингликаны) Н Н Н Н Н Н Н N Н Н Н ОН ОН ОН
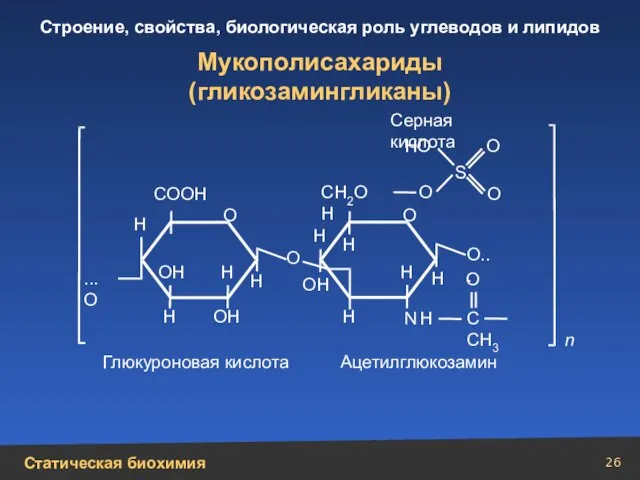
- 26. С СН3 Мукополисахариды (гликозамингликаны) Н Н Н Н Н Н Н N Н Н Н ОН
- 27. СН3СООН + С2Н5ОН СН3СООС2Н5 + Н2О Уксусная кислота Этиловый спирт Этилацетат – СОО – это сложноэфирная
- 28. Структурная функция (обязательные компоненты биологических мембран); Энергетическая функция (эффективный источник энергии в клетке); Служат формой, в
- 29. Жирные кислоты СН 2 СН 2 СН 2 СН 2 СН 2 СН 2 СН 2
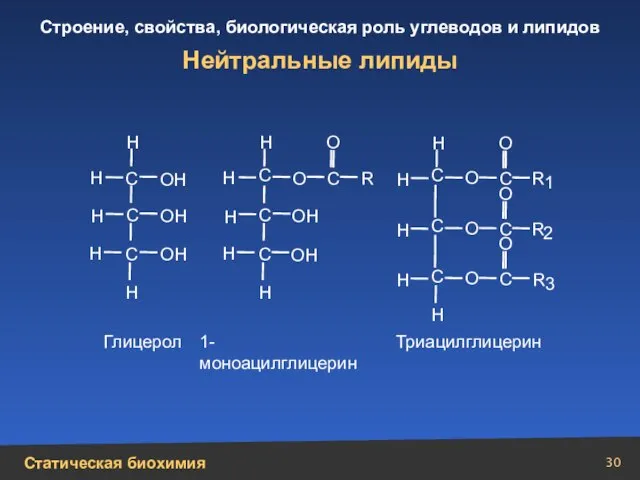
- 30. Нейтральные липиды Н Н Н Н Н Н Н Н Н Н Н Н Н Н
- 31. Нейтральные диольные липиды СН2ОН СН2ОН СН2О СН2ОН СНОН СН2ОН СН2 (СН2)7 СН3 С О Этандиол (этиленгликоль)
- 32. Нейтральные плазмалогены Н Н О О СН2О СН2О С С С С R1 R2 R3 СНО
- 33. Воска O || СН3(СН2)n – С – О – СН2 (СН2)m СН3
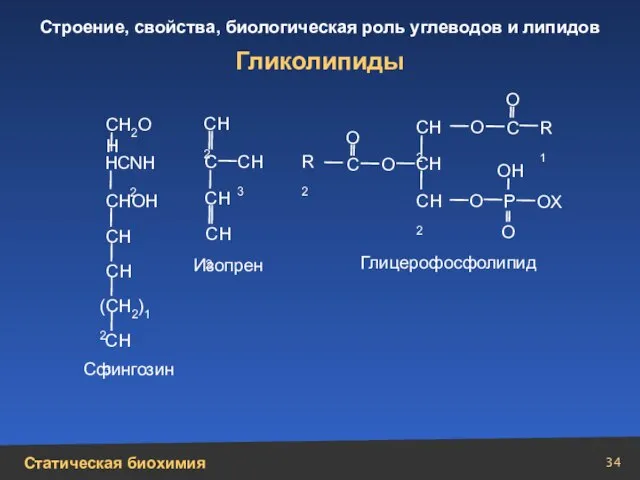
- 34. Гликолипиды ОН О О X О О О О О СН2ОН СНОН СН СН СН СН
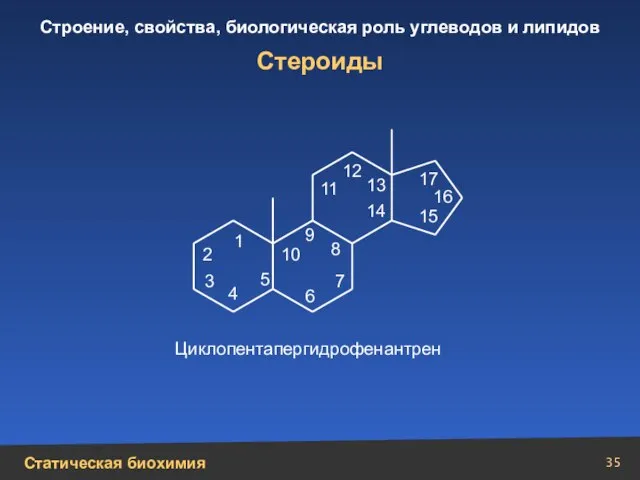
- 35. Стероиды Циклопентапергидрофенантрен 1 2 3 4 5 10 9 6 7 8 11 12 13 14
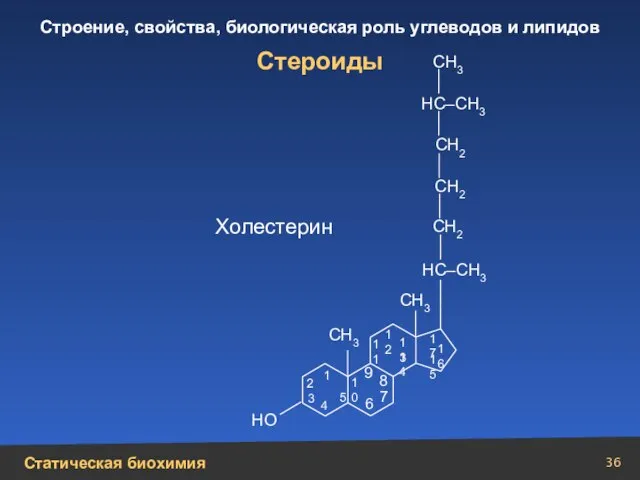
- 36. Стероиды Холестерин 1 2 3 4 5 10 9 6 7 8 11 12 13 14
- 37. Терпены CH3 | Н2С=С—СН=СН2 Изопрен
- 38. 1.2. Строение, свойства, биологическая роль белков
- 39. Общая формула аминокислот R—CH—COO– NH 3 +
- 40. неполярные, или гидрофобные (аланин, валин, лейцин, изолейцин, пролин, фенилаланин, триптофан, метионин); полярные, но незаряженные (глицин, серин,
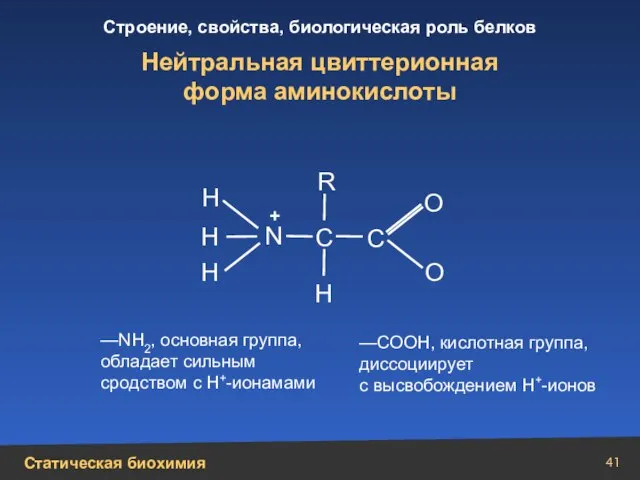
- 41. Н Н N Н Н + О О С С R Нейтральная цвиттерионная форма аминокислоты —NH2,
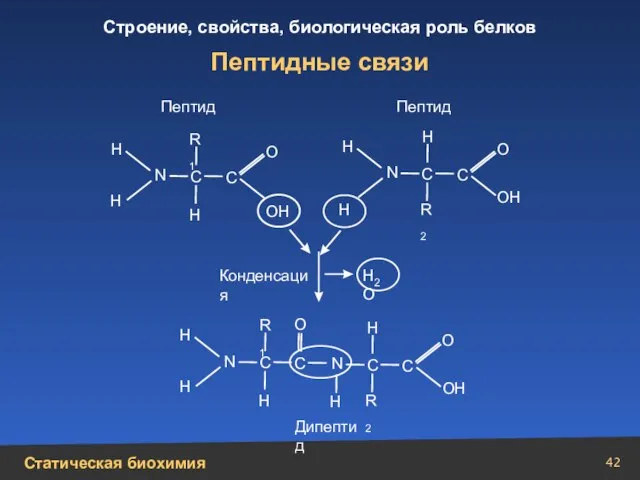
- 42. Пептидные связи Н Н Н Н N N N N Н Н Н Н Н Н
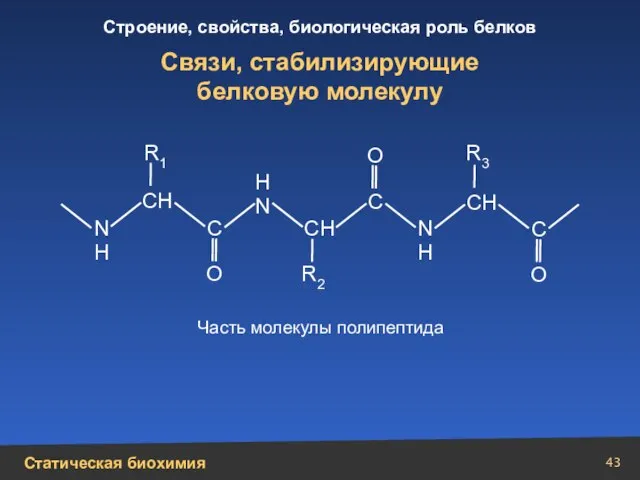
- 43. Связи, стабилизирующие белковую молекулу N Н N Н Н N О О О С С СН
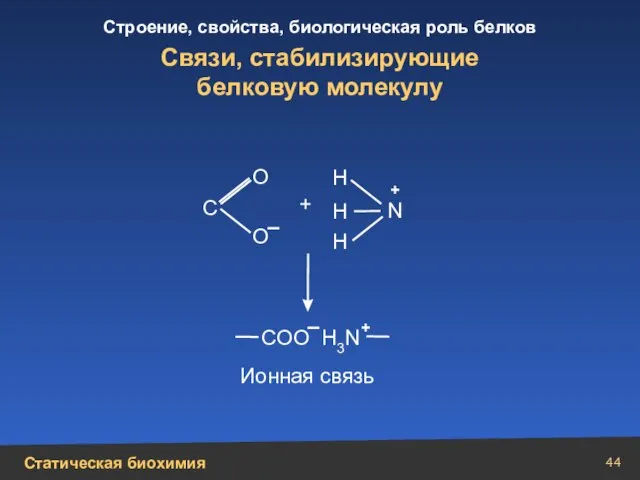
- 44. Связи, стабилизирующие белковую молекулу Н Н N Н + + О О С СОО Н3 N
- 45. Связи, стабилизирующие белковую молекулу S Н S S Н S Дисульфидная связь Окисление Восстановление
- 46. Связи, стабилизирующие белковую молекулу Водородная связь Локализованное электростатическое притяжение – ОН . . . . .
- 47. Последовательность аминокислот для каждого белка уникальна и закреплена генетически Первичная структура характеризует последовательность аминокислотных остатков в
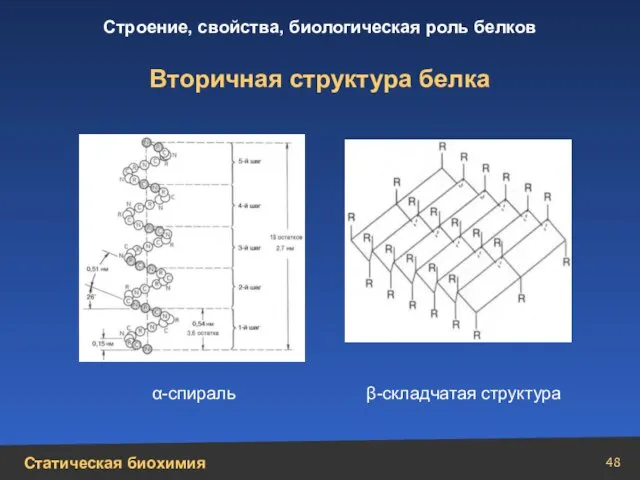
- 48. Вторичная структура белка α-спираль β-складчатая структура
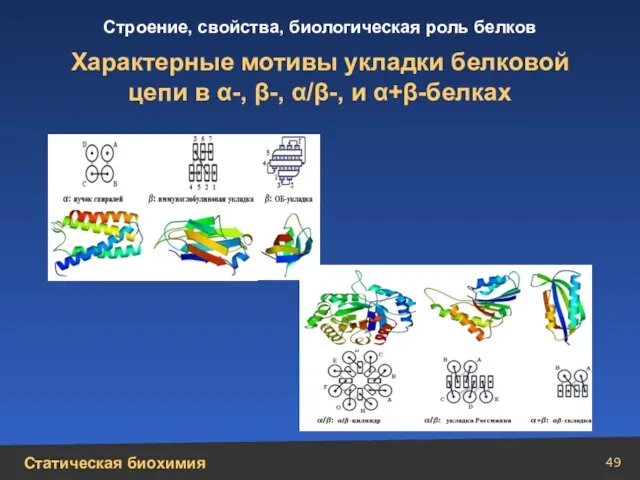
- 49. Характерные мотивы укладки белковой цепи в α-, β-, α/β-, и α+β-белках
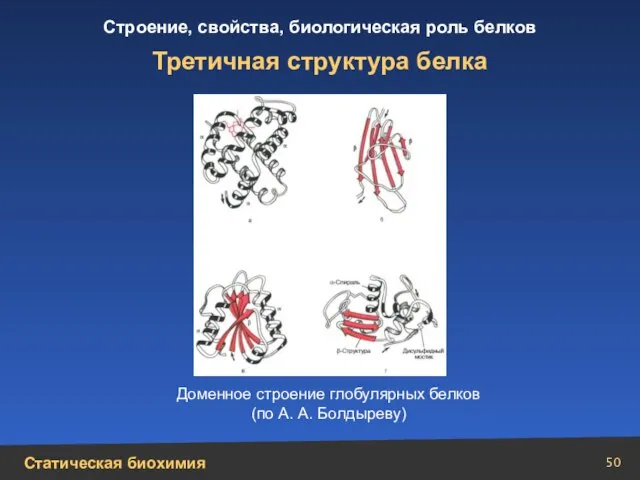
- 50. Третичная структура белка Доменное строение глобулярных белков (по А. А. Болдыреву)
- 51. Четвертичная структура белка а – гемоглобин, состоящий из четырех субъединиц (двух α-цепей и двух β-цепей), б
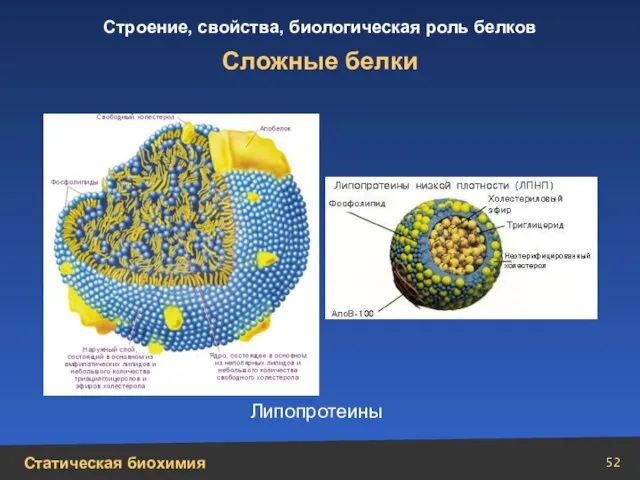
- 52. Сложные белки Липопротеины
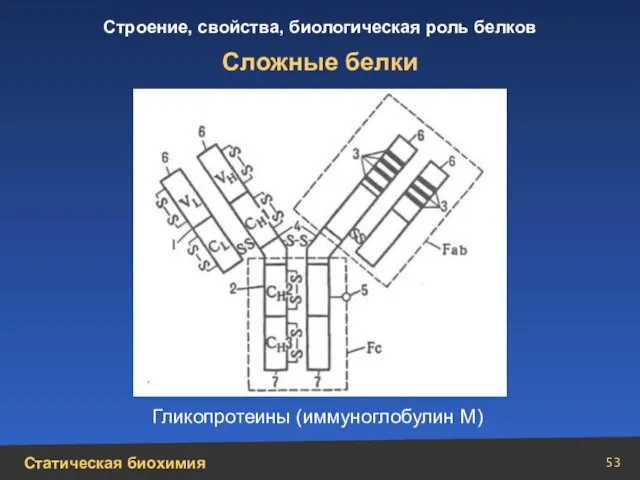
- 53. Сложные белки Гликопротеины (иммуноглобулин М)
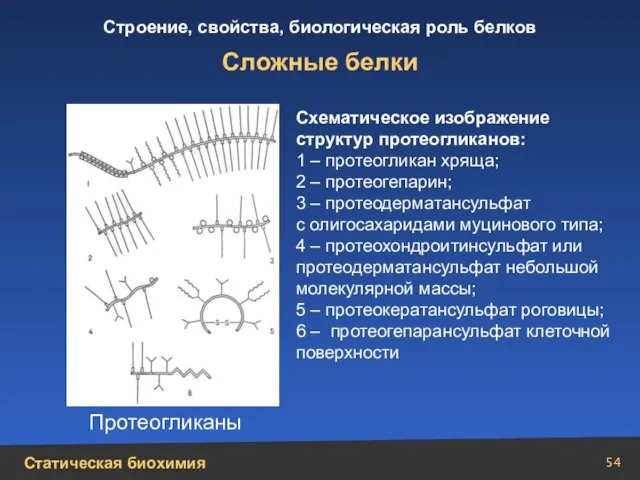
- 54. Сложные белки Схематическое изображение структур протеогликанов: 1 – протеогликан хряща; 2 – протеогепарин; 3 – протеодерматансульфат
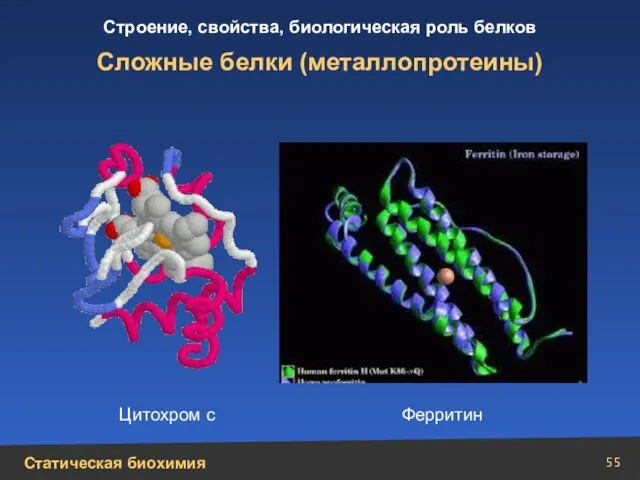
- 55. Сложные белки (металлопротеины) Цитохром с Ферритин
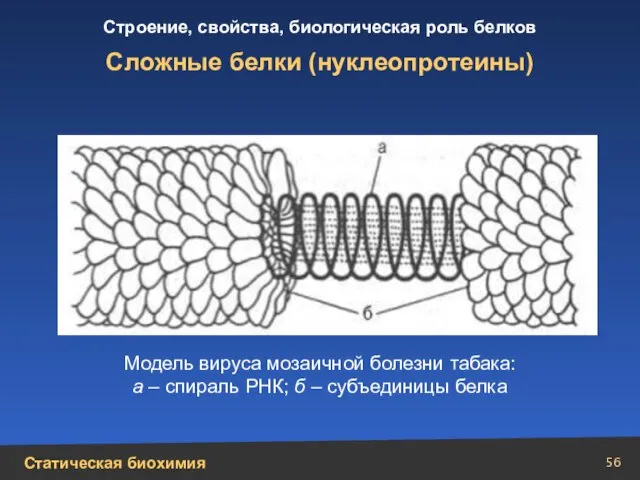
- 56. Сложные белки (нуклеопротеины) Модель вируса мозаичной болезни табака: а – спираль РНК; б – субъединицы белка
- 57. 1.3. Строение, свойства, биологическая роль нуклеотидов
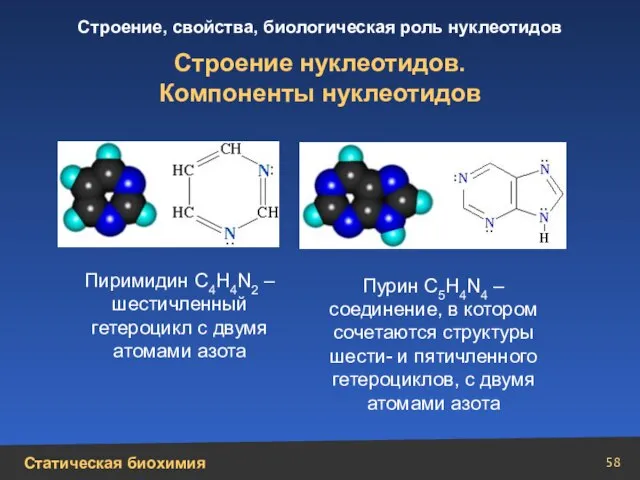
- 58. Строение нуклеотидов. Компоненты нуклеотидов Пиримидин С4Н4N2 – шестичленный гетероцикл с двумя атомами азота Пурин С5H4N4 –
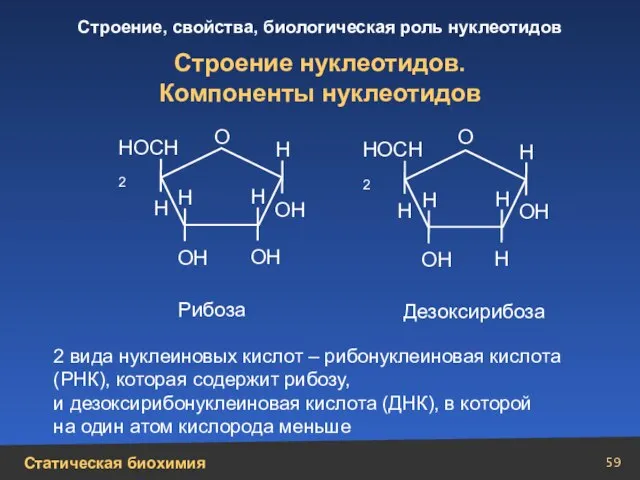
- 59. Строение нуклеотидов. Компоненты нуклеотидов 2 вида нуклеиновых кислот – рибонуклеиновая кислота (РНК), которая содержит рибозу, и
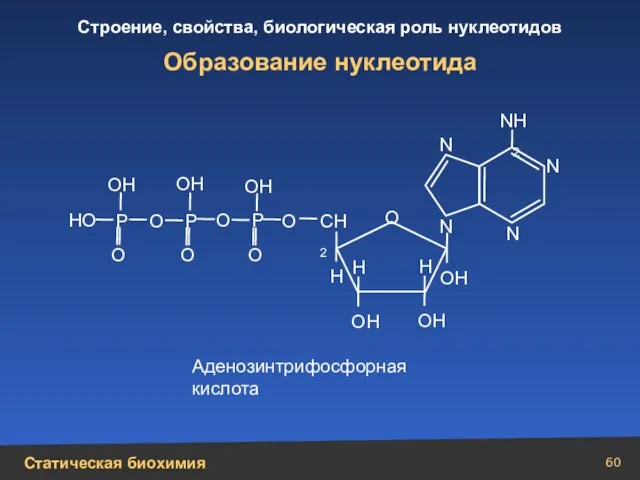
- 60. Образование нуклеотида СН2 N N N N N Н2 Н Н ОН Н ОН ОН О
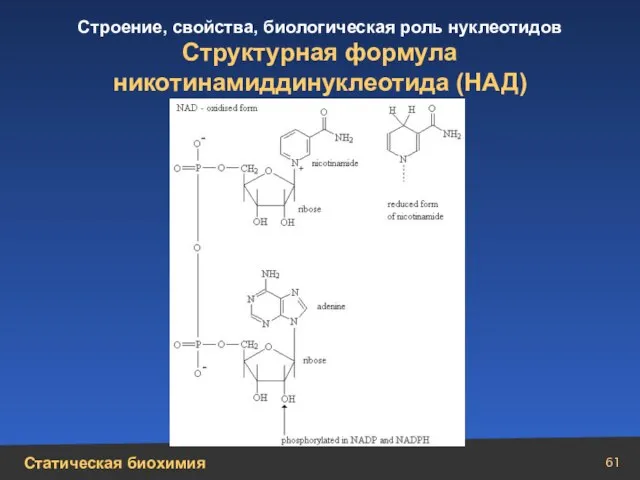
- 61. Структурная формула никотинамиддинуклеотида (НАД)
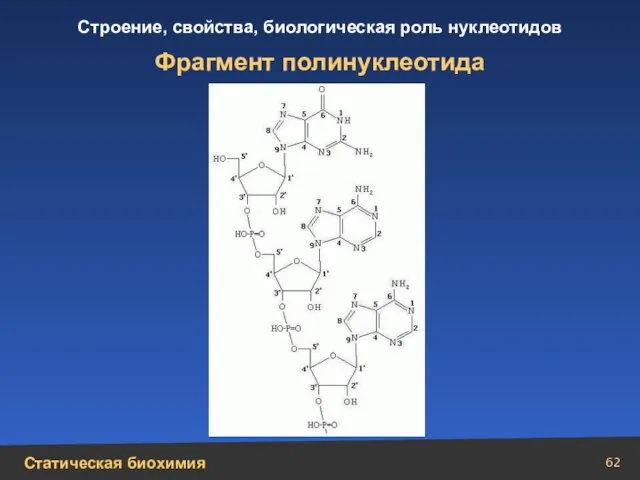
- 62. Фрагмент полинуклеотида
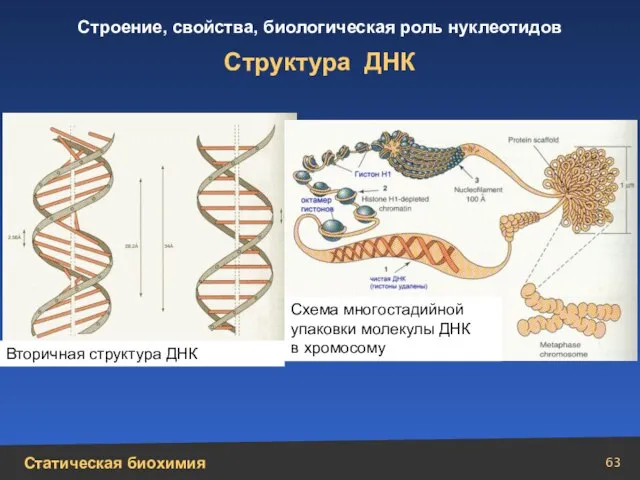
- 63. Структура ДНК Вторичная структура ДНК Схема многостадийной упаковки молекулы ДНК в хромосому
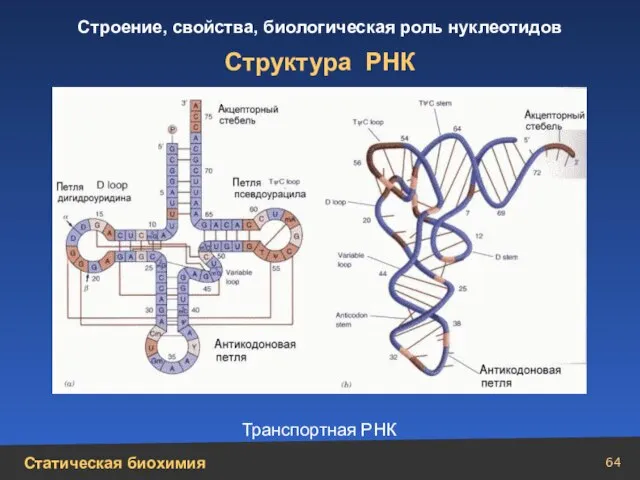
- 64. Структура РНК Транспортная РНК
- 65. 1.4. Витамины, ферменты
- 66. Водорастворимые витамины Витамин В1 (тиамин)
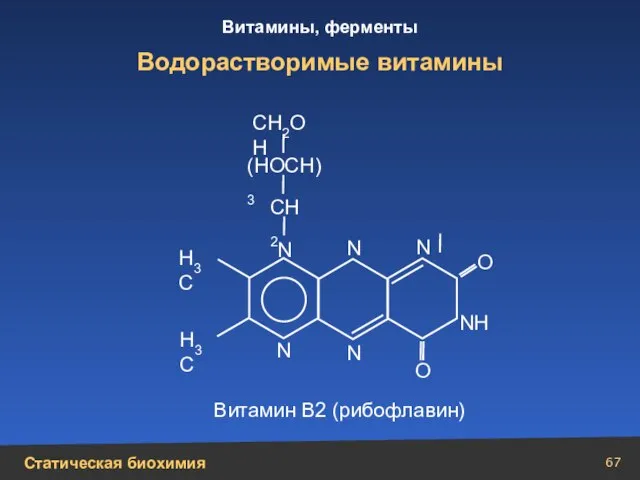
- 67. Водорастворимые витамины N N N N N СН2 СН2ОН (НОСН)3 N Н Н3С Н3С О О
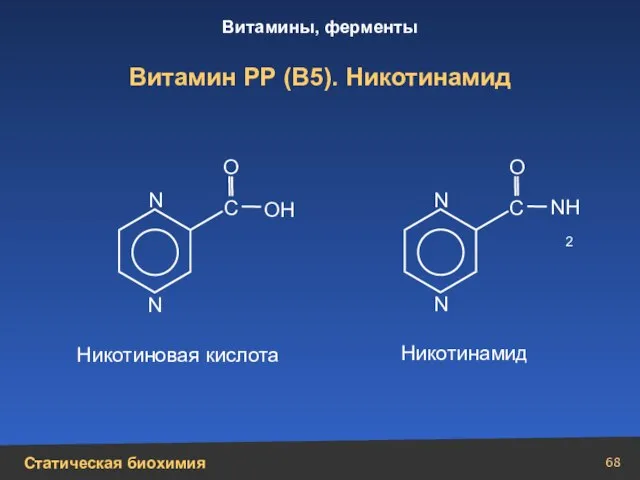
- 68. Витамин РР (В5). Никотинамид N N N N С С N Н2 ОН О О Никотиновая
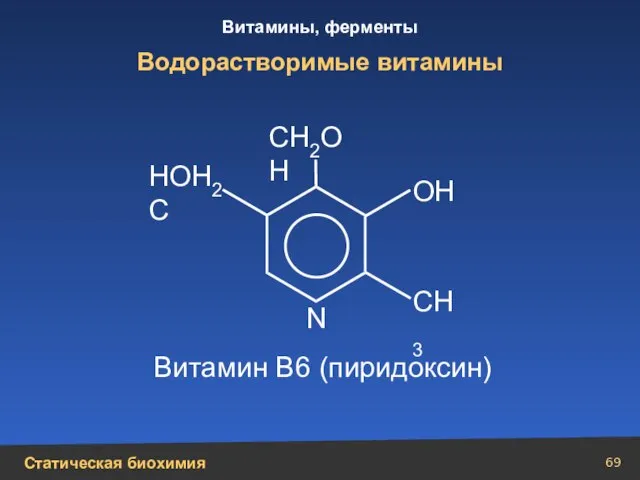
- 69. Водорастворимые витамины N СН3 СН2ОН ОН Витамин В6 (пиридоксин) НОН2С
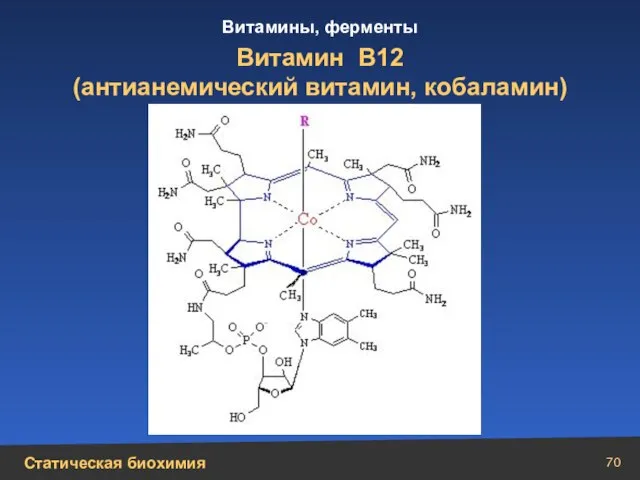
- 70. Витамин В12 (антианемический витамин, кобаламин)
- 71. Витамин C (аскорбиновая кислота)
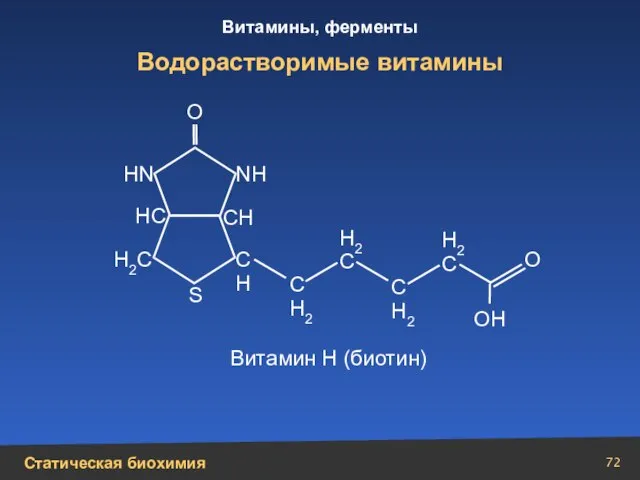
- 72. Водорастворимые витамины Н2С Н N N Н НС СН С Н С Н2 С Н2 Н2
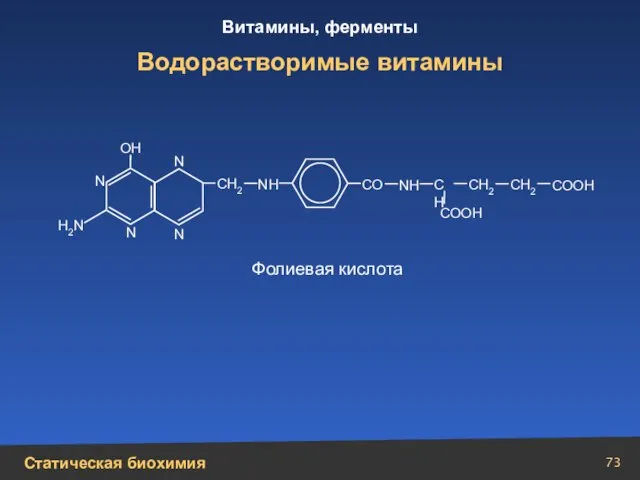
- 73. Водорастворимые витамины N N N N СН2 СН СН2 СН2 СО СООН СООН N Н N
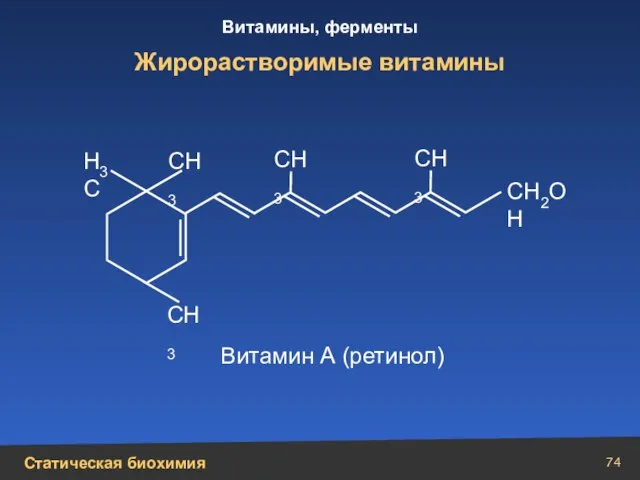
- 74. Жирорастворимые витамины Н3С СН3 СН3 СН3 СН3 СН2ОН Витамин А (ретинол)
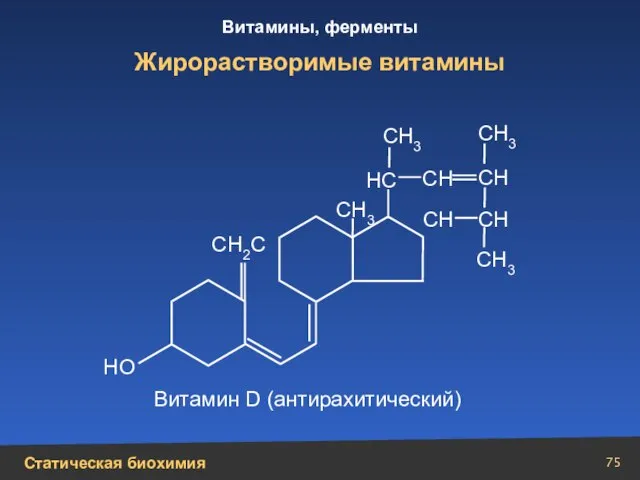
- 75. Жирорастворимые витамины НС СН СН СН СН3 СН3 СН3 СН3 СН СН2С Витамин D (антирахитический) НО
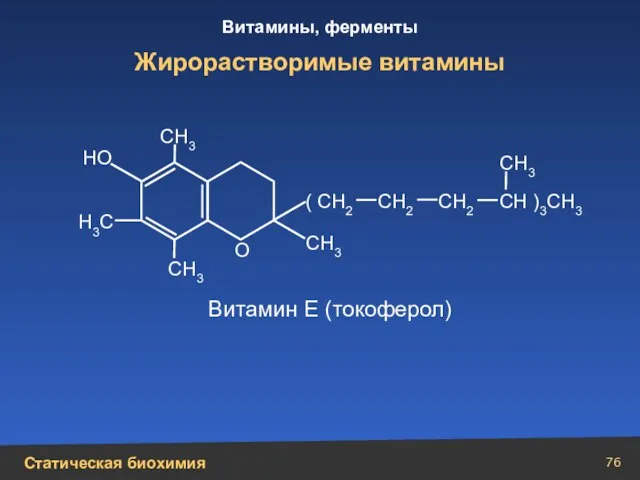
- 76. Жирорастворимые витамины СН )3СН3 СН3 СН3 СН3 СН3 Н3С ( СН2 СН2 СН2 Витамин Е (токоферол)
- 77. Ферменты Наиболее крупный специализированный класс белковых молекул, катализирующих химические реакции, из которых слагается клеточный обмен. Белки,
- 78. Химическая кинетика В соответствии с законом действующих масс для реакции А + В → С +
- 79. Кинетика ферментативных реакций Вещества, реакцию превращения которых ускоряют ферменты (E), называются субстратами (S). В ходе ферментативной
- 80. Кинетика ферментативных реакций Действие ферментов как катализаторов обладает некоторыми особенностями: фермент не способен вызвать новую химическую
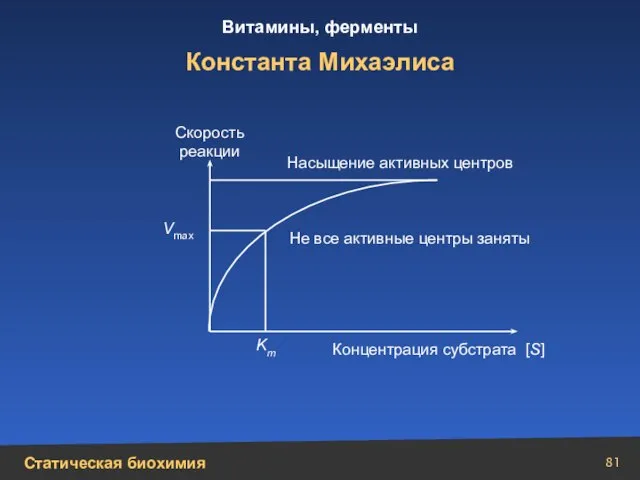
- 81. Константа Михаэлиса Km Vmax Насыщение активных центров Скорость реакции Не все активные центры заняты Концентрация субстрата
- 82. Фермент увеличивает скорость реакции понижая свободную энергию переходного состояния путем стабилизации активированного комплекса; увеличивая энергию субстрата,
- 83. Классификация активности ферментов Оксидоредуктазы (окислительно-восстановительные реакции) Оксидоредуктазы осуществляют перенос атомов Н и О или электронов от
- 84. Классификация активности ферментов Трансферазы (перенос функциональных групп) Ускоряют перенос определенной группы атомов от одного вещества к
- 85. Классификация активности ферментов Гидролазы (реакции гидролиза) Ускоряют реакции гидролиза, при которых из субстрата образуются 2 продукта.
- 86. Классификация активности ферментов Лиазы Лиазы ускоряют негидролитическое присоединение к субстрату или отщепление от него группы атомов.
- 87. Классификация активности ферментов Изомеразы (реакции изомеризации) Внутримолекулярные перестройки: АВ → ВА
- 88. Классификация активности ферментов Лигазы (образование связей за счет АТФ) Лигазы катализируют реакции синтеза высокомолекулярных полимеров из
- 89. 1.5. Гормоны: биологическая роль, классификация, механизм действия
- 90. Гормоны Гормоны – это биологически активные вещества, синтезируемые эндокринными железами, выделяемые ими в кровь или лимфу
- 91. Механизм действия гормонов Гормоны регулируют метаболизм клеток-мишеней через изменение активности ферментных систем: путем изменения индукции ферментов;
- 92. Гормоны гипоталамуса Гормоны гипоталамуса являются относительно простыми по структуре олигопептидами. К ним относятся: кортиколиберин, тиролиберин, люлилиберин,
- 93. Гормоны гипофиза Гипофиз синтезирует тропные и эффекторые гормоны Тропные гормоны: АКТГ (адренокортикотропный гормон) – пептид, регулирующий
- 94. Гормоны гипофиза Гипофиз синтезирует тропные и эффекторые гормоны Эффекторные гормоны АДГ (антидиуретический гормон, вазопрессин) – простой
- 95. Гормоны поджелудочной железы Гормоны поджелудочной железы инсулин (белок из 51 аминокислотного остатка) и глюкагон (одноцепочечный полипептид
- 96. Гормоны щитовидной железы Тиреоидные гормоны Тироксин и трийодтиронин являются производными аминокислотами тирозина и содержат в своем
- 97. Гормоны коры надпочечников Секреция гормонов коры надпочечников регулируется адренокортикотропным гормоном (АКТГ) гипофиза. Из коры надпочечников выделено
- 98. Гормоны мозгового вещества надпочечников Гормоны мозгового вещества надпочечников – адреналин и норадреналин (катехоламины).
- 99. Гормоны половых желез Мужские половые гормоны (андрогены) образуются в семенниках, женские половые гормоны (эстрогены, прогестины) продуцируются
- 100. Гормоны паращитовидной железы Паращитовидные железы секретируют 2 гормона (паратгормон и кальцитонин), которые вместе с витамином Д
- 101. Гормоны тимуса (вилочковой железы) В тимусе продуцируется 5 гормонально-активных факторов (полипептидов по природе): тимозин, гомеостатический тимусный
- 102. БИОХИМИЯ ЧАСТЬ 2 Динамическая биохимия
- 103. Оглавление 2.1. Переваривание углеводов в пищеварительном тракте. Гликолиз. Окислительное декарбоксилирование пирувата 2.2. Аэробный метаболизм углеводов 2.3.
- 104. 2.1. Переваривание углеводов в пищеварительном тракте. Гликолиз. Окислительное декарбоксилирование пирувата
- 105. В обмене веществ выделяют внешний обмен и промежуточный. Внешний обмен – внеклеточное переваривание веществ на путях
- 106. Метаболизм выполняет 4 основные функции: извлечение энергии из окружающей среды (либо в форме химической энергии органических
- 107. Метаболические пути: катаболические; анаболические; амфиболические. Метаболические пути и обмен энергии
- 108. Катаболизм включает 3 основных этапа: крупные пищевые молекулы расщепляются на составляющие их строительные блоки (аминокислоты, моносахариды,
- 109. Анаболические пути – это ферментативный синтез сравнительно крупных клеточных компонентов из простых предшественников. Процессы связаны с
- 110. Амфиболические пути – двойственные. Связывают катаболические и анаболические пути. Метаболические пути и обмен энергии
- 111. Полисахариды и олигосахариды распадаются до более простых соединений путем гидролиза. Расщепление крахмала и гликогена начинается в
- 112. Продукты полного переваривания углеводов – глюкоза, галактоза, фруктоза – через стенки кишечника поступают в кровь. Моносахариды
- 113. Гликолиз – центральный путь катаболизма глюкозы в животных, растительных клетках и микроорганизмах. Это наиболее древний путь,
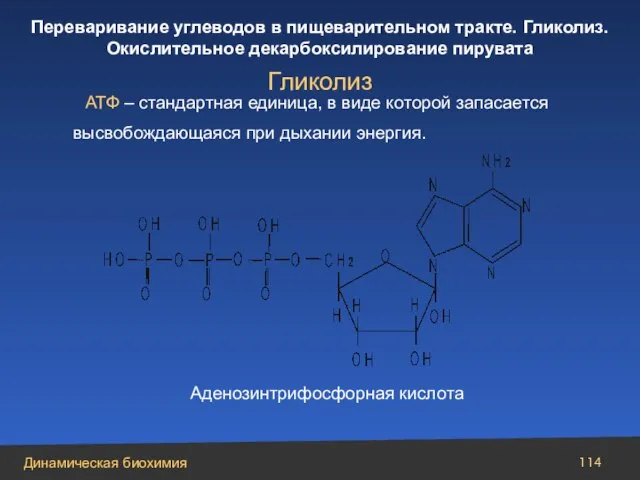
- 114. АТФ – стандартная единица, в виде которой запасается высвобождающаяся при дыхании энергия. Гликолиз Аденозинтрифосфорная кислота
- 115. (АТФ) Аденозин – Ф ~ Ф ~ Ф “Высокоэнергетическая” связь +Н2О Гидролиз (АДФ) Аденозин – Ф
- 116. Аэробные условия Анаэробные условия Гликолиз Глюкоза Продукты брожения Брожение Глюкоза Продукты брожения Брожение СО2 + Н2О
- 117. С6Н12О6 + 2Фн + 2АДФ → 2СН3СНОНСООН + 2АТФ + 2Н2О Глюкоза → 2 Лактат ΔG1`
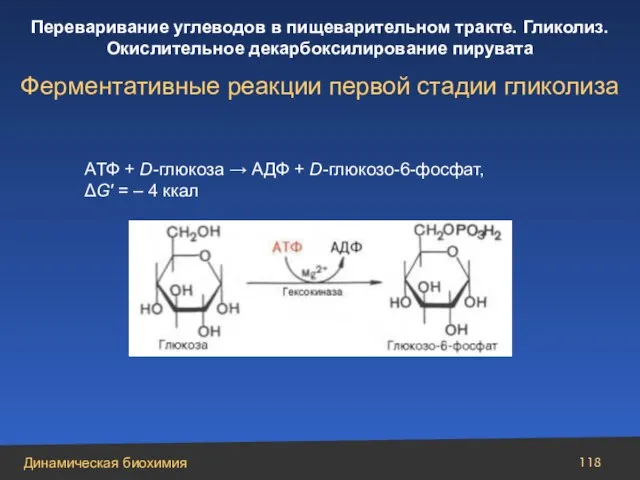
- 118. AТФ + D-глюкоза → АДФ + D-глюкозо-6-фосфат, ΔG′ = – 4 ккал Ферментативные реакции первой стадии
- 119. Гликолиз
- 120. Превращение глюкозо-6-фосфат во фруктозо-6-фосфат D-глюкозо-6-фосфат ↔ D-фруктозо-6-фосфат, ΔG′ = + 0,4 ккал
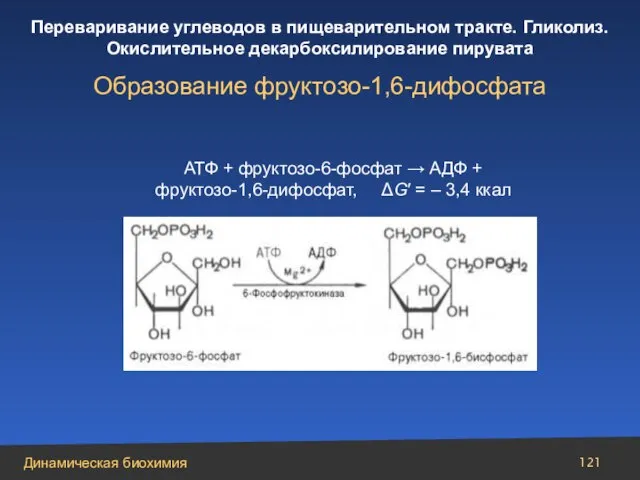
- 121. АТФ + фруктозо-6-фосфат → АДФ + фруктозо-1,6-дифосфат, ΔG′ = – 3,4 ккал Образование фруктозо-1,6-дифосфата
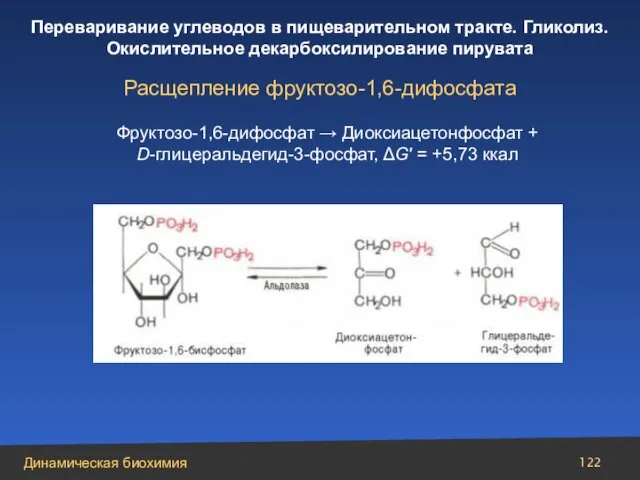
- 122. Расщепление фруктозо-1,6-дифосфата Фруктозо-1,6-дифосфат → Диоксиацетонфосфат + D-глицеральдегид-3-фосфат, ΔG′ = +5,73 ккал
- 123. Взаимопревращение триозофосфатов Диоксиацетонфосфат ↔ D-глицеральдегид-3-фосфат
- 124. Окисление глицеральдегид-3-фосфата до 1,3-дифосфоглицерата Глицеральдегид-3-фосфат+ НАД++ Фн → 1,3-дифосфоглицерат + НАД * Н + Н+, ΔG′
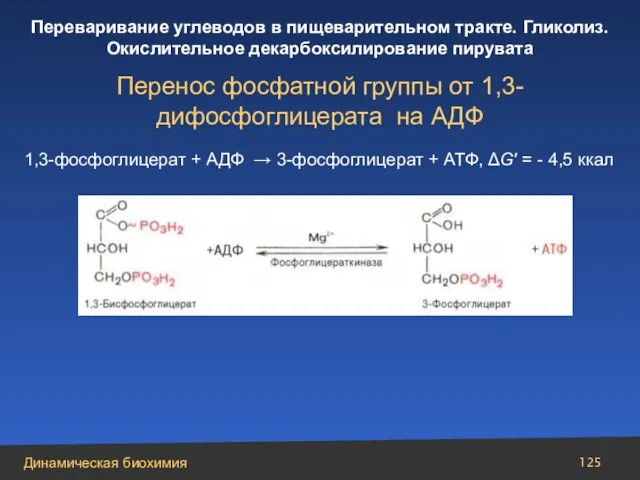
- 125. Перенос фосфатной группы от 1,3-дифосфоглицерата на АДФ 1,3-фосфоглицерат + АДФ → 3-фосфоглицерат + АТФ, ΔG′ =
- 126. Превращение 3-фосфоглицерата в 2-фосфоглицерат 3-фосфоглицерат ↔ 2-фосфоглицерат
- 127. 2-фосфоглицерат → Фосфоенолпируват + Н2О, ΔG′ = + 0,44 ккал Дегидратация 2-фосфоглицерата с образованием фосфоенолпирувата
- 128. Фосфоенолпируват + АДФ → Пируват + АТФ, ΔG′ = - 7,5 ккал Перенос фосфатной группы от
- 129. Пируват + НАД*Н + Н ↔ Лактат + НАД+, ΔG′ = - 6,0 ккал Восстановление пирувата
- 130. Глюкоза + 2АТФ + 2НАД+ + 2Фн + 4АДФ + 2НАДН +2Н+ +2Лактат + 2АДФ +
- 131. Гликоген → глюкозо-1-фосфат → глюкозо-6-фосфат → … → 2лактат Гликогенолиз
- 132. 2.2. Аэробный метаболизм углеводов
- 133. Глюкоза → 2Лактат, ΔG′ = – 47 ккал (гликолиз) Глюкоза + 6О2 → 6СО2 + 6Н2О,
- 134. Суммарная реакция цикла трикарбоновых кислот описывается уравнением: Ацетил-СоА + 3НАД+ + ФАД + ГДФ + Фн
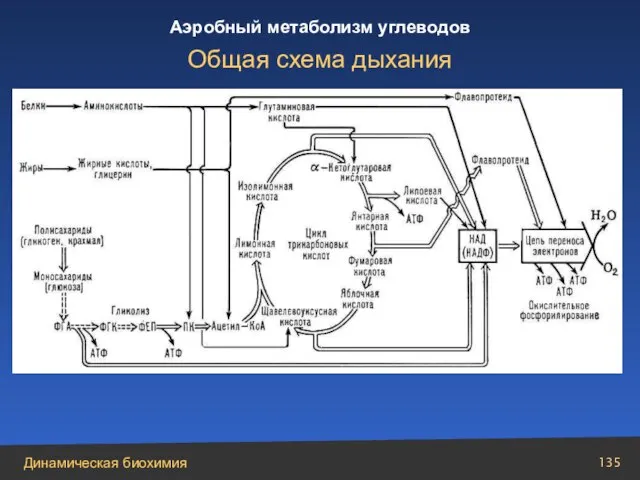
- 135. Общая схема дыхания
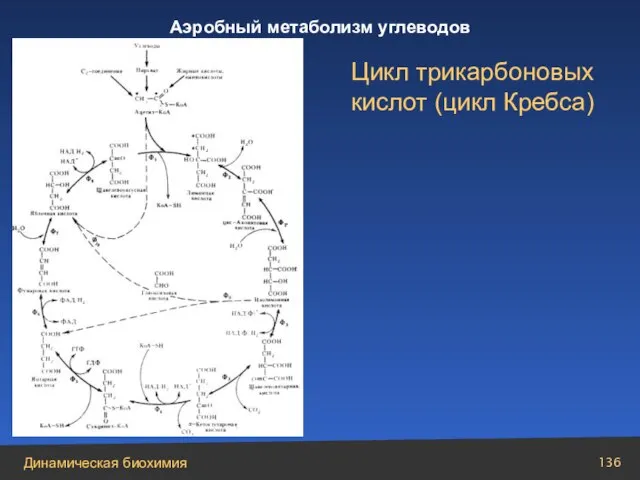
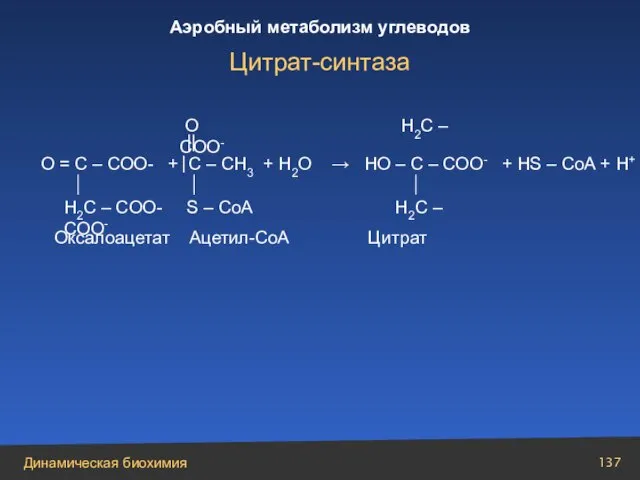
- 136. Цикл трикарбоновых кислот (цикл Кребса)
- 137. О = С – СОО- + С – СН3 + Н2О → НО – С –
- 138. СОО - COO- COO- | | | H – C – H H2O H – C
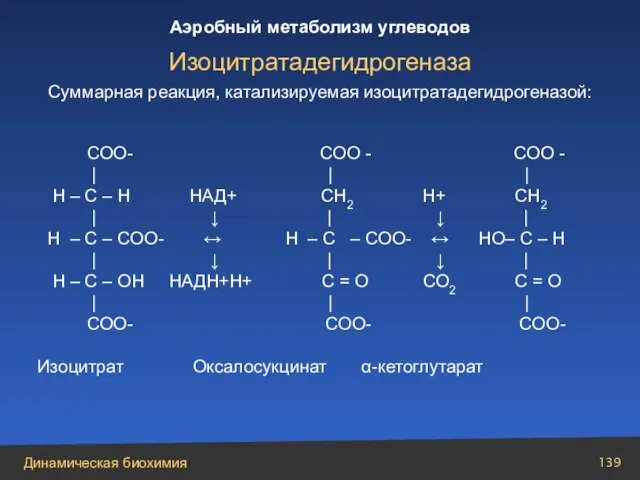
- 139. Суммарная реакция, катализируемая изоцитратадегидрогеназой: COO- СОО - СОО - | | | H – C –
- 140. α-кетоглутарат + НАД+ + КоА–SH ↔ Cукцинил-S–КоА + СО2 + НАДН + Н+ G′ = –
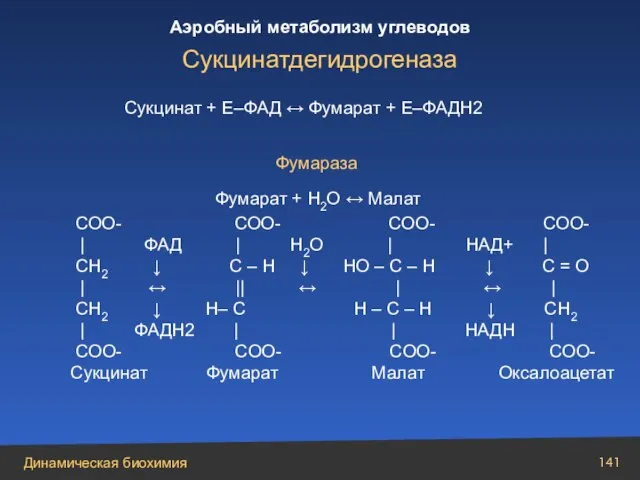
- 141. Сукцинат + Е–ФАД ↔ Фумарат + Е–ФАДН2 Фумараза Фумарат + Н2О ↔ Малат СОО- СОО- СОО-
- 142. Малат + НАД+ ↔ Оксалоацетат + НАДН + Н+ Окисление малата до оксалоацетата
- 143. НАДН + Н+ + Е1 – ФАД → НАД+ + Е1 – ФАДН2 Е1 – ФАДН2
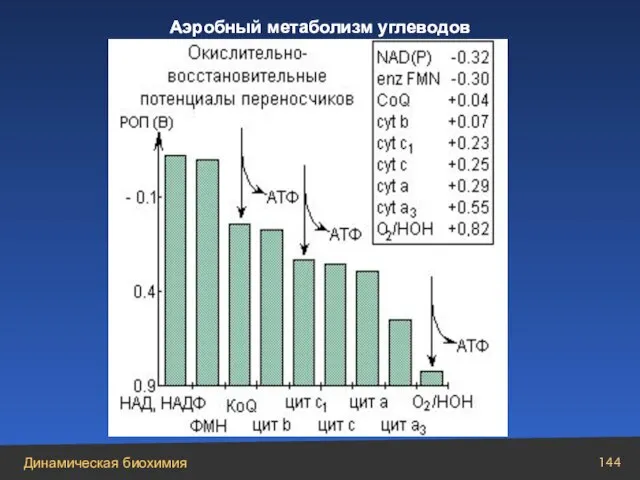
- 144. РИСУНОК Аэробный метаболизм углеводов
- 145. Суммарное уравнение процесса фосфорилирования в дыхательной цепи: НАДН + 2Н+ + 3АДФ + Фн + 1/2О2
- 146. Суммарные реакции аэробного дыхания: С6Н12О6 + 2Фн + 2АДФ + 2НАД+ → 2Пируват+2НАДН+2Н+ +2АТФ+2Н2О 2Пируват +
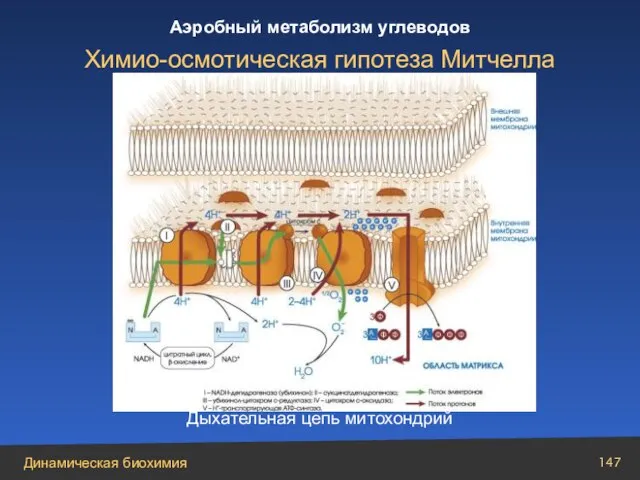
- 147. Дыхательная цепь митохондрий Химио-осмотическая гипотеза Митчелла
- 148. 2.3. Липидный обмен
- 149. Превращение липидов в процессе пищеварения. Всасывание продуктов переваривания липидов и ресинтез липидов в кишечной стенке. Внутриклеточные
- 150. 2.4. Белковый обмен
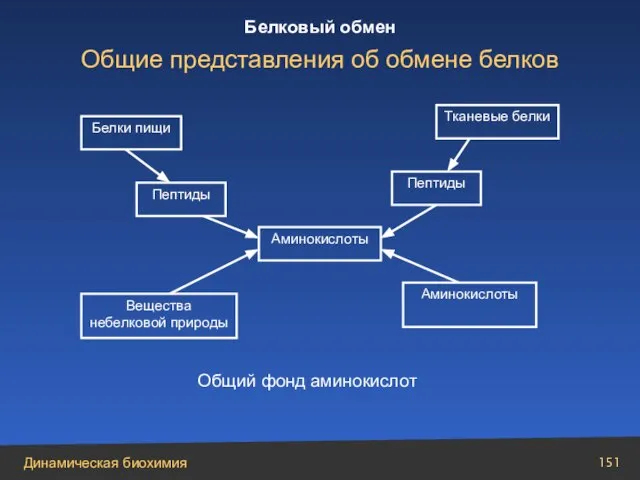
- 151. Аминокислоты Белки пищи Пептиды Вещества небелковой природы Тканевые белки Пептиды Аминокислоты Общий фонд аминокислот Общие представления
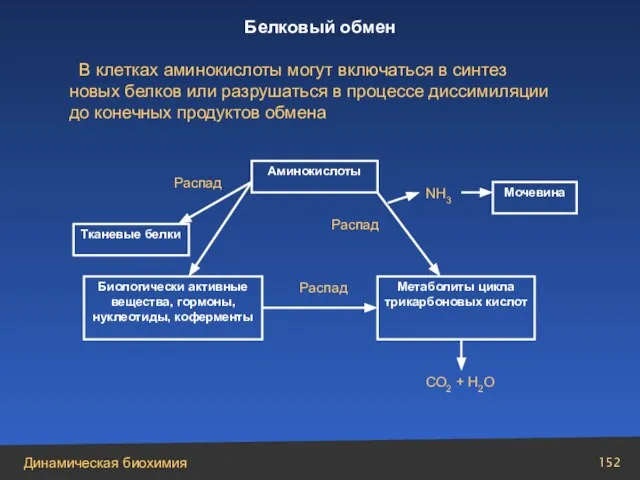
- 152. Аминокислоты Тканевые белки Биологически активные вещества, гормоны, нуклеотиды, коферменты Распад Метаболиты цикла трикарбоновых кислот Распад СО2
- 153. Пищеварение белков. Синтез белков. Внутриклеточный распад белков. Пути выведения аммиака из организма. Суммарное уравнение цикла имеет
- 154. 2.5. Интеграция клеточного обмена
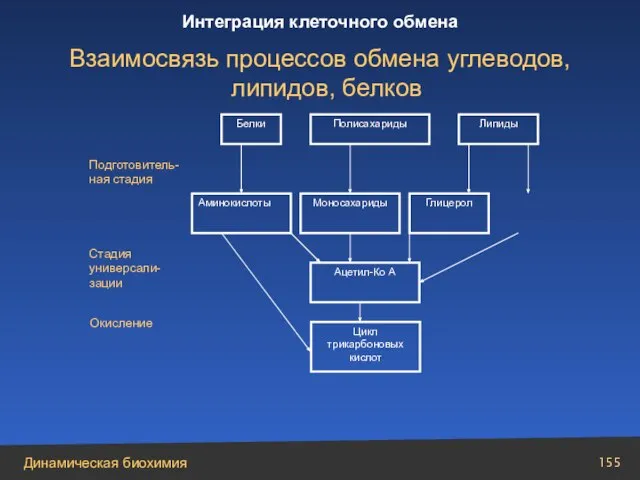
- 155. Белки Полисахариды Липиды Подготовитель-ная стадия Аминокислоты Моносахариды Глицерол Ацетил-Ко А Цикл трикарбоновых кислот Стадия универсали-зации Окисление
- 156. В клетке скорость химических реакций определяется: доступностью субстратов (концентрация реагирующих веществ); 2) активностью ферментов (конкурентное и
- 157. БИОХИМИЯ ЧАСТЬ 3 Спортивная биохимия
- 158. 3.1. Биохимия мышечного сокращения 3.2. Энергетическое обеспечение мышечной деятельности 3.3. Биохимические изменения в организме при работе
- 159. 3.1. Биохимия мышечного сокращения
- 160. Типы мышечных волокон: скелетные; сердечные (миокард); гладкие.
- 161. Поперечно-полосатая скелетная мускулатура
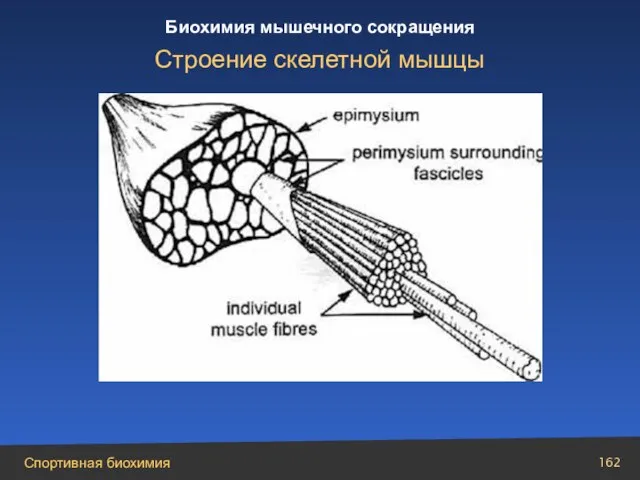
- 162. Строение скелетной мышцы
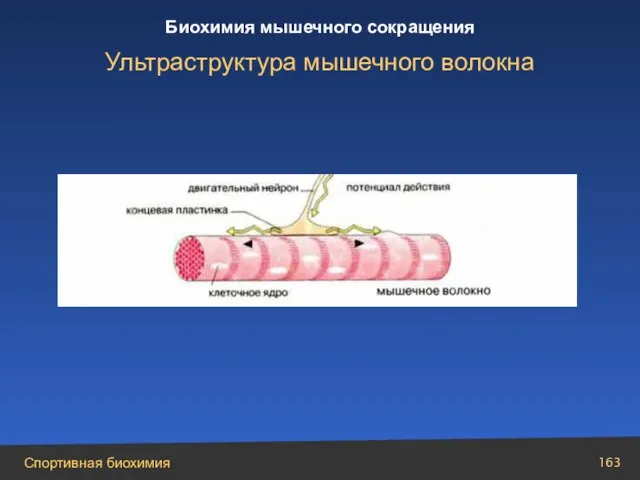
- 163. Ультраструктура мышечного волокна
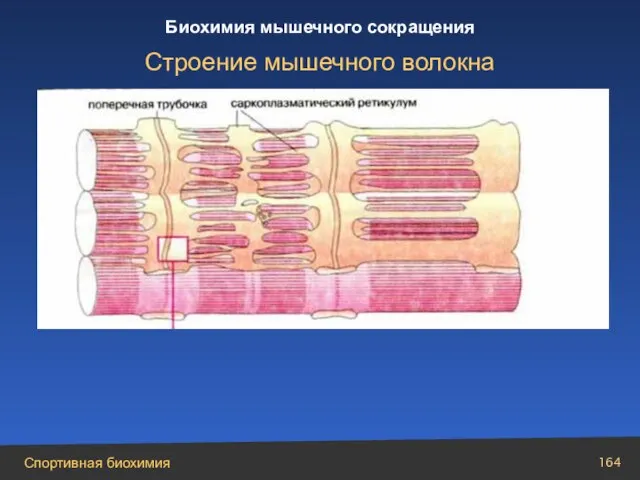
- 164. Строение мышечного волокна
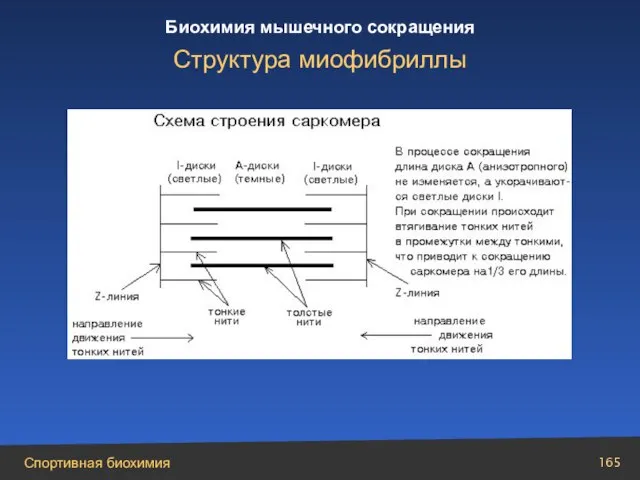
- 165. Структура миофибриллы
- 166. В основе модели скользящих нитей лежат следующие факты: при сокращении мышцы длины толстых и тонких нитей
- 167. Гидролиз ATФ до AДФ и неорганического фосфата
- 168. 3.2. Энергетическое обеспечение мышечной деятельности
- 169. Ресинтез АТФ: анаэробный механизм; аэробный механизм.
- 170. Анаэробные механизмы: креатинфосфокиназный (алактатный) механизм, обеспечивающий ресинтез АТФ за счет перефосфорилирования между креатинфосфатом и АДФ; гликолитический
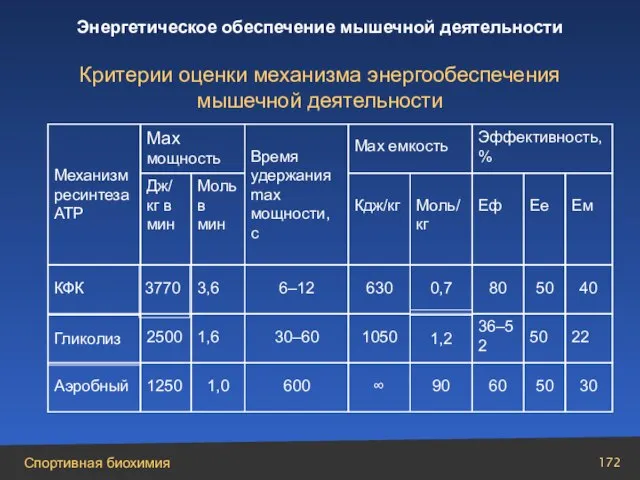
- 171. Общий КПД при преобразовании энергии метаболических процессов в механическую работу (Ем) зависит от двух показателей: эффективности
- 172. Критерии оценки механизма энергообеспечения мышечной деятельности 30 50 60 90 ∞ 600 1,0 1250 Аэробный 22
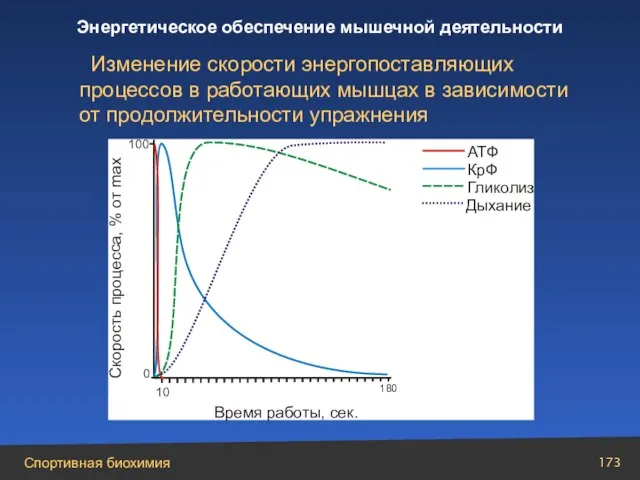
- 173. Изменение скорости энергопоставляющих процессов в работающих мышцах в зависимости от продолжительности упражнения
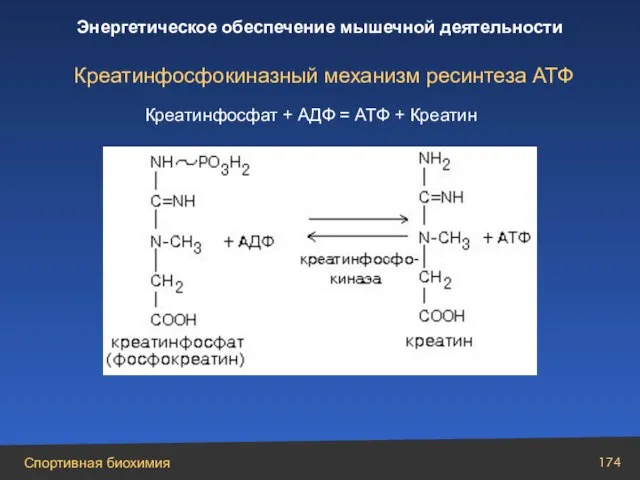
- 174. Креатинфосфокиназный механизм ресинтеза АТФ Креатинфосфат + AДФ = АТФ + Креатин
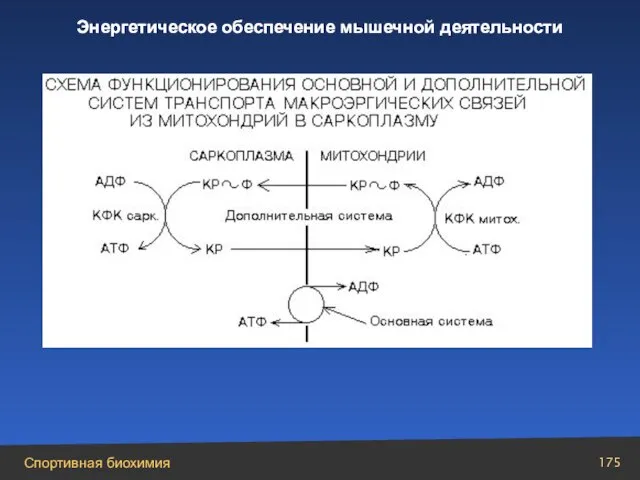
- 175. Энергетическое обеспечение мышечной деятельности
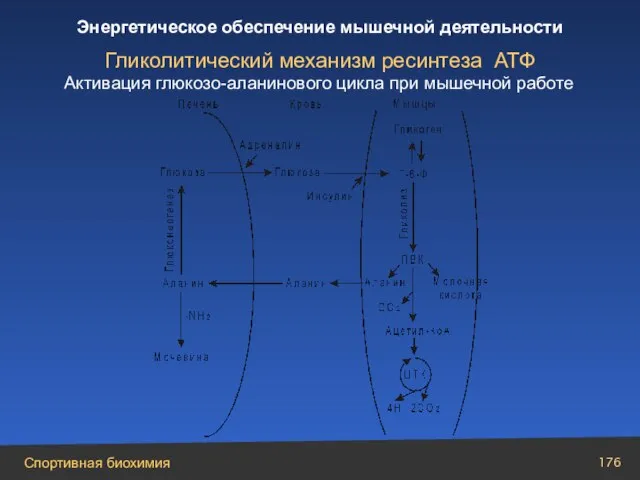
- 176. Гликолитический механизм ресинтеза АТФ Активация глюкозо-аланинового цикла при мышечной работе
- 177. Миокиназный механизм ресинтеза АТФ 2AДФ → АТФ + АМФ
- 178. Аэробный механизм ресинтеза АТФ Скорость образования АТФ в процессе окислительного фосфорилирования зависит от: соотношения АТФ/AДФ, при
- 179. Взаимосвязь анаэробных и аэробных превращений в скелетных мышцах: энерго-транспортный «челнок» с участием миофибриллярных и митохондриальных изоферментов
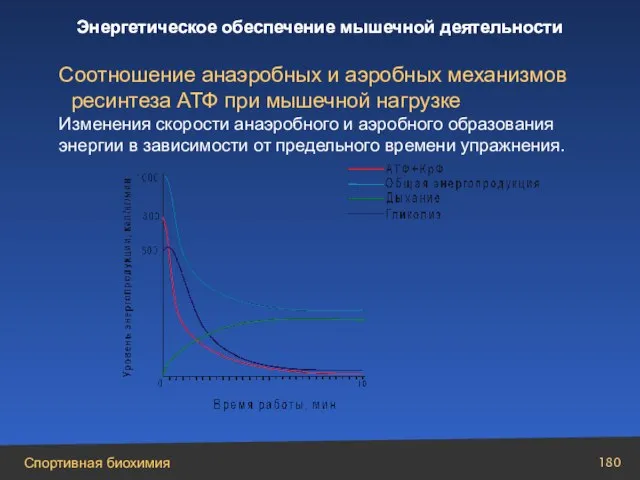
- 180. Соотношение анаэробных и аэробных механизмов ресинтеза АТФ при мышечной нагрузке Изменения скорости анаэробного и аэробного образования
- 181. Факторы, лимитирующие физическую работоспособность человека: биоэнергетические (аэробные или анаэробные) возможности человека; нейромышечные (мышечная сила и техника
- 182. Основные особенности человека, определяющие его физическую работоспособность Алактатная анаэробная способность, связанная с процессами анаэробного ресинтеза АТР
- 183. 3.3. Биохимические изменения в организме при работе различного характера. Биохимические изменения при утомлении. Общие изменения в
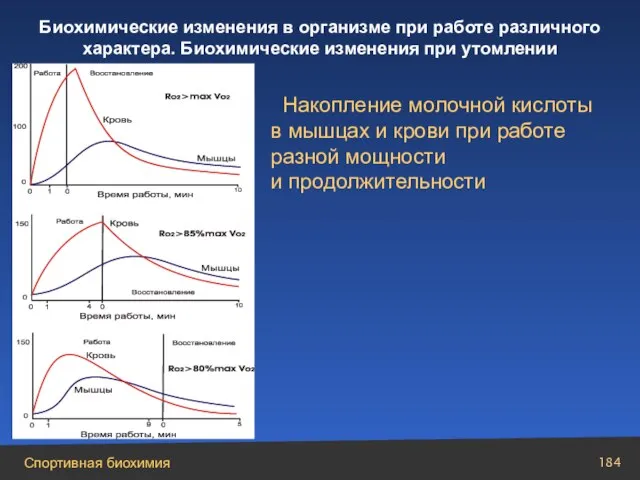
- 184. Накопление молочной кислоты в мышцах и крови при работе разной мощности и продолжительности
- 185. При переходе от состояния покоя к интенсивной мышечной деятельности происходят следующие процессы: анаэробные механизмы ресинтеза АТФ;
- 186. Специализация мышц по типу энергетического обеспечения Красные мышцы – “медленные”, оксидативные. Белые мышцы – “быстрые”, гликолитические.
- 187. В зависимости от количества мышц, участвующих в работе, ее делят на: локальную (менее ¼ всех мышц
- 188. Режимы работы мышц: статический (изометрический) происходит пережимание капилляров, велика доля участия анаэробных реакций; динамический (изотонический) обеспечивается
- 189. Уровни мощности работы: критический – максимальное потребление кислорода; порог анаэробного обмена – усиление анаэробных реакций; мощность
- 190. Зоны относительной мощности по классификации В. С. Фарфеля: максимальная – обеспечение энергией за счет АТФ и
- 191. Первопричины утомления снижение энергетических ресурсов; уменьшение активности ключевых ферментов из-за угнетающего действия продуктов метаболизма тканей; нарушение
- 192. 3.4. Биохимические превращения в период восстановления после мышечной работы. Срочное и отставленное восстановление
- 193. Ресинтез внутриклеточных запасов гликогена От 12 до 72 ч Усиление индуктивного синтеза структурных и ферментных белков
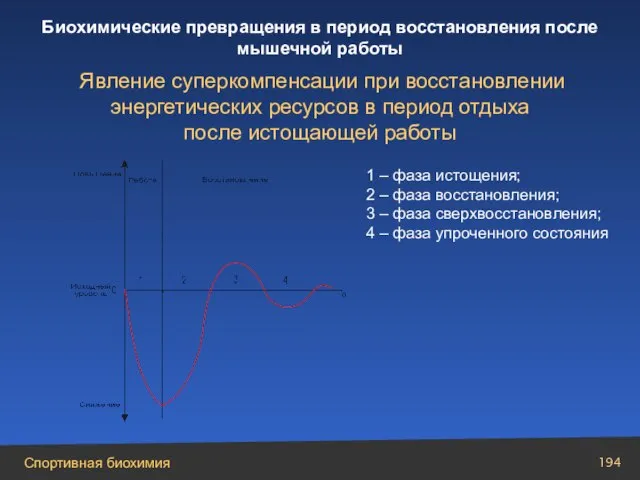
- 194. 1 – фаза истощения; 2 – фаза восстановления; 3 – фаза сверхвосстановления; 4 – фаза упроченного
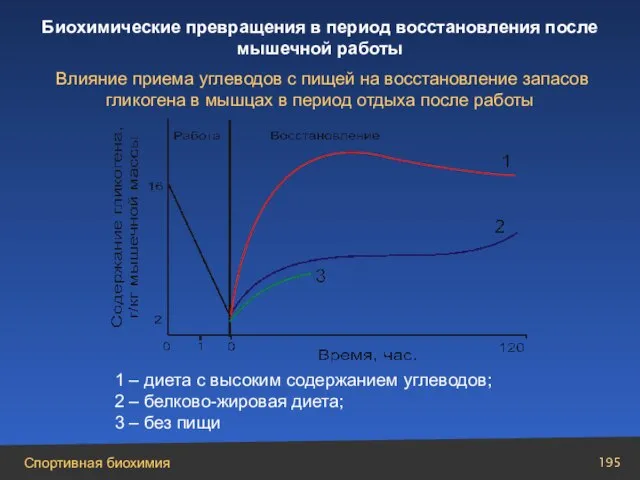
- 195. 1 – диета с высоким содержанием углеводов; 2 – белково-жировая диета; 3 – без пищи Влияние
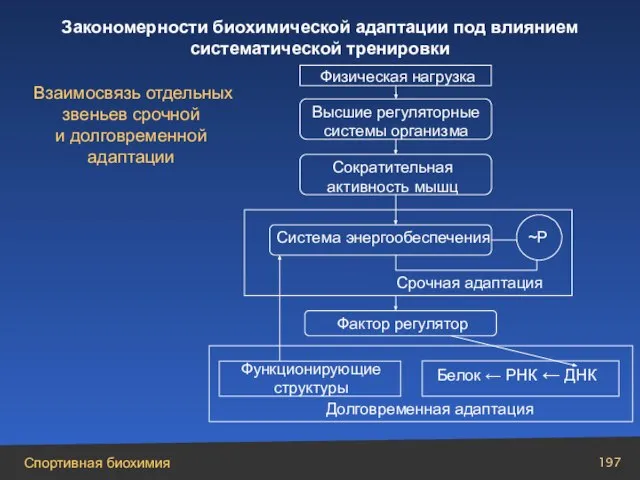
- 196. 3.5. Закономерности биохимической адаптации под влиянием систематической тренировки
- 197. Высшие регуляторные системы организма Физическая нагрузка Взаимосвязь отдельных звеньев срочной и долговременной адаптации Сократительная активность мышц
- 198. Принципы тренировок на основе закономерностей биологической адаптации: сверхотягощение; специфичность; обратимость действия; положительное взаимодействие; последовательная адаптация; цикличность.
- 199. Развитие адаптации под воздействием тренировки обеспечивается: системой внутриклеточного энергетического обмена; гормональными симпато-адреналовой и гипофизарно-адренокортикальной системами. Сверхотягощение
- 200. 3.6. Биохимический контроль при занятиях физической культурой и спортом. Биохимический контроль за развитием систем энергообеспечения организма
- 201. О более высоком уровне тренированности свидетельствуют меньшее накопление лактата (по сравнению с нетренированными) при выполнении стандартной
- 202. Регулярное применение допингов вызывает нарушение функции многих систем: сердечно-сосудистой; эндокринной, в особенности половых желез (атрофия) и
- 203. По фармакологическому действию допинги делятся на 5 классов: психостимуляторы (амфетамин, эфедрин, фенамин, кофеин, кокаин, и др.);
- 204. 3.7. Биохимические основы силы, быстроты и выносливости Морфологические и биохимические основы скоростно-силовых качеств Биохимические основы методов
- 205. 3.8. Биохимическое обоснование методики занятий физической культурой и спортом с лицами разного возраста. Биохимические основы рационального
- 206. Основными химическими компонентами пищи являются 6 групп веществ: поставщики энергии (углеводы, белки, жиры); незаменимые аминокислоты; незаменимые
- 207. Пищевые добавки способствуют: увеличению мышечной массы; коррекции компонентного состава тела (уменьшение жирового компонента, увеличение мышечного и
- 208. Графики взяты из книги: Биохимия: учеб. для институтов физической культуры / ред. В. В. Меньшикова, Н.
- 209. Основной библиографический список Биохимия : учеб. для институтов физической культуры / ред. В. В. Меньшикова, Н.
- 211. Скачать презентацию






































































































































 Основы цветоведения
Основы цветоведения Культурная практика по Древней Руси
Культурная практика по Древней Руси Развитие речи
Развитие речи Презентация на тему Культура речи Синтаксические нормы
Презентация на тему Культура речи Синтаксические нормы Ресурсы повышения эффективности индивидуальной профилактической деятельности
Ресурсы повышения эффективности индивидуальной профилактической деятельности Государство
Государство Поверхности. Начертательная геометрия
Поверхности. Начертательная геометрия Особенности современного проектирования
Особенности современного проектирования Дети, как известно, наша боль, наша радость
Дети, как известно, наша боль, наша радость Электронные платежные системы России: игроки, состояние и проблемы
Электронные платежные системы России: игроки, состояние и проблемы Faisons connaissence. Leçon 9
Faisons connaissence. Leçon 9 "Вопорсы дядюшки Светофора"
"Вопорсы дядюшки Светофора" Конструкция There is/there are-There was/there were
Конструкция There is/there are-There was/there were ИРЛАНДИЯ
ИРЛАНДИЯ Сервировка стола к завтраку
Сервировка стола к завтраку Главная улица Москвы Если вы пройдете через Александровский сад и повернете налево,
Главная улица Москвы Если вы пройдете через Александровский сад и повернете налево, Как научить ребёнка сознательно относиться к собственному здоровью
Как научить ребёнка сознательно относиться к собственному здоровью Итоги повышения квалификации специалистов учреждений МСЭ по МКФ в рамках государственной программы «Доступная среда» на 2011-2015 го
Итоги повышения квалификации специалистов учреждений МСЭ по МКФ в рамках государственной программы «Доступная среда» на 2011-2015 го Понятие и содержание законности
Понятие и содержание законности Условия назначения страховой пенсии по старости
Условия назначения страховой пенсии по старости Юрист
Юрист Пассивные операции банков, их характеристика
Пассивные операции банков, их характеристика Презентация на тему Треугольники (5 класс)
Презентация на тему Треугольники (5 класс)  Техника мраморирования в современном дизайне
Техника мраморирования в современном дизайне Речевые секреты
Речевые секреты ВОЗРОЖДЕНИЕ (Ренессанс) Торговая площадь (Гроте-маркт) и ратуша —
ВОЗРОЖДЕНИЕ (Ренессанс) Торговая площадь (Гроте-маркт) и ратуша —  Батьківський комітет. Благодійний внесок
Батьківський комітет. Благодійний внесок Сетевая лаборатория проектного предпринимательского образования
Сетевая лаборатория проектного предпринимательского образования