Содержание
- 2. Корпускулярно-хвильовий дуалізм. Рівняння Шредингера 1. Гіпотеза де-Бройля. 2. Дифракція електронів. 3. Співвідношення невизначеностей. 4. Часове і
- 3. Формула де-Бройля Оскільки світло проявляє корпускулярно-хвильовий дуалізм, Луї де-Бройль в 1924 р. висунув гіпотезу, що і
- 4. Формула де-Бройля Якщо нерелятивістська частинка має кінетичну енергію Тоді Отже, для електронів, розігнаних до 1÷100 еВ
- 5. Формула де-Бройля Подивимось з позицій корпускулярно-хвильового дуалізму на атом водню. Згідно з другим постулатом Бора mυrn
- 6. Стаціонарна орбіта
- 7. Формула де-Бройля При проходженні окремих електронів через тонкий монокристал отримуємо дифракційну картину. Отже, хвильові властивості притаманні
- 8. Співвідношення невизначеностей Розглянемо обмеження, які накладає корпускулярно-хвильовий дуалізм на можливість одночасного визначення імпульсу та координати частинок
- 9. Співвідношення невизначеностей. Такі ж висновки справедливі і для частинок. В 1927 р. В.Гейзенберг знайшов співвідношення Добуток
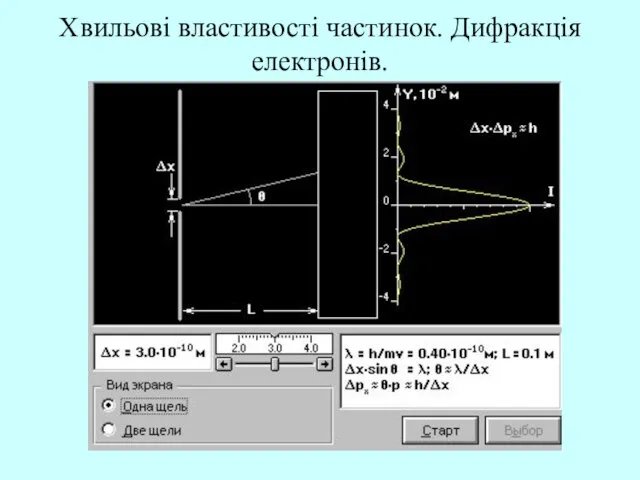
- 10. Хвильові властивості частинок. Дифракція електронів.
- 11. Співвідношення невизначеностей Розглянемо електрон в атомі. Його положення визначається з точністю до розмірів атома Δх ~
- 12. Хвильова функція Потрібно з'ясувати фізичну природу хвиль де-Бройля. Порівнювали дифракцію світла і мікрочастинки. Для світла в
- 13. Хвильова функція Отже, дифракційна картина є проявом статистичної закономірності, згідно з якою частинки потрапили в ті
- 14. Хвильова функція Звідси − умова нормування хвильової функції. Щоб функція ψ була характеристикою стану частинки, необхідно:
- 15. Хвильова функція Якщо система може знаходитись в станах ψ1, ψ2, ..., ψn, то вона може бути
- 16. Хвильова функція Одноелектронну хвильову функцію в сферично симетричному електричному полі атомного ядра, яку задають головним n,
- 17. Хвильова функція Геометричне уявлення атомної орбіталі – область простору, обмежена поверхнею рівною густини (еквіденсітною поверхнею) ймовірності
- 18. Хвильова функція Орбіталі слетеровського типу мають наступний вигляд: де A − коефіцієнт норміровки − сферична гармоніка
- 19. Густина електричного заряду У квантовій механіці густина заряду, наприклад, електрона в атомі, співвідноситься з хвильової функцією
- 20. Метод МО ЛКАО Молекула розглядається як ціле, а не як сукупність атомів, що зберегли індивідуальність. Всі
- 21. ОРБІТАЛЬ – область найбільш можливого місцезнаходження електрона в атомі (атомна орбіталь) або в молекулі (молекулярна орбіталь).
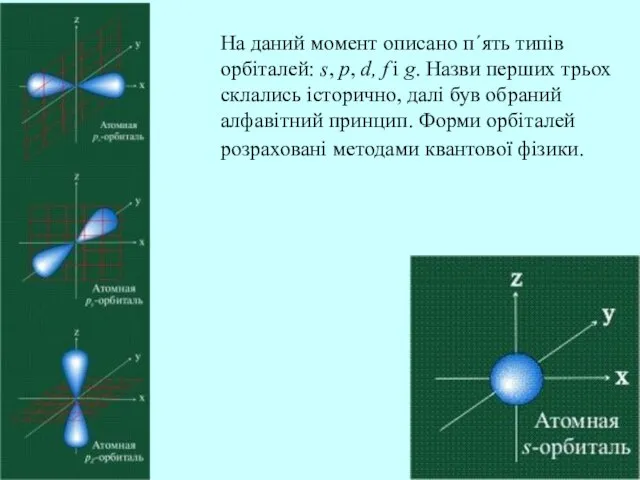
- 22. На даний момент описано п΄ять типів орбіталей: s, p, d, f і g. Назви перших трьох
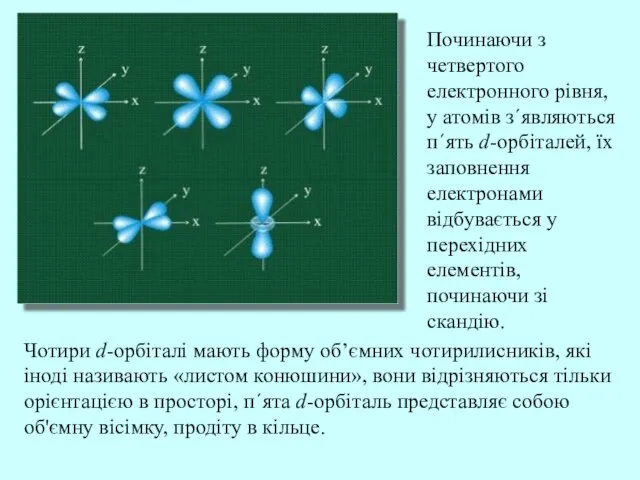
- 23. Чотири d-орбіталі мають форму об’ємних чотирилисників, які іноді називають «листом конюшини», вони відрізняються тільки орієнтацією в
- 24. В тому випадку, коли атом вуглецю бере участь в утворенні насичених сполучень (які не мають кратних
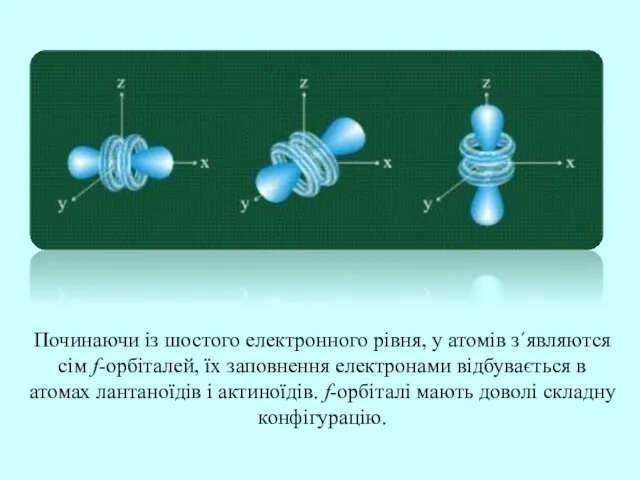
- 25. Починаючи із шостого електронного рівня, у атомів з΄являются сім f-орбіталей, їх заповнення електронами відбувається в атомах
- 26. На восьмому електронному рівні знаходяться дев΄ять g-орбіталей. Елементи, які мають електрони на цих орбіталях, повинні з'явитися
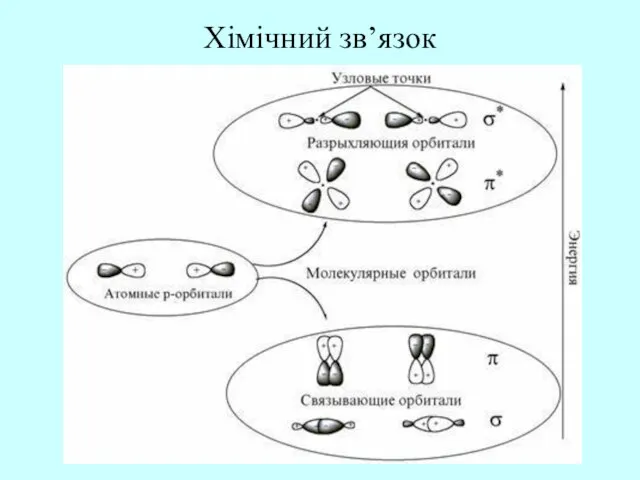
- 27. Хімічний зв’язок Хімічний зв'язок притягання між атомами або молекулами дозволяє утворення хімічних сполук, які містять два
- 28. Хімічний зв’язок
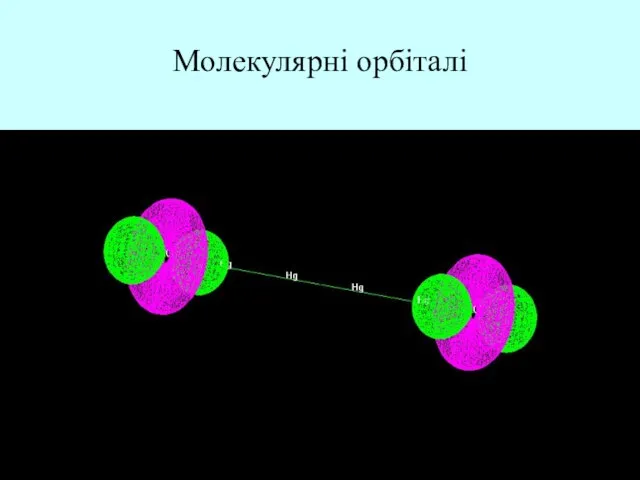
- 29. Молекулярні орбіталі
- 30. Молекулярні орбіталі
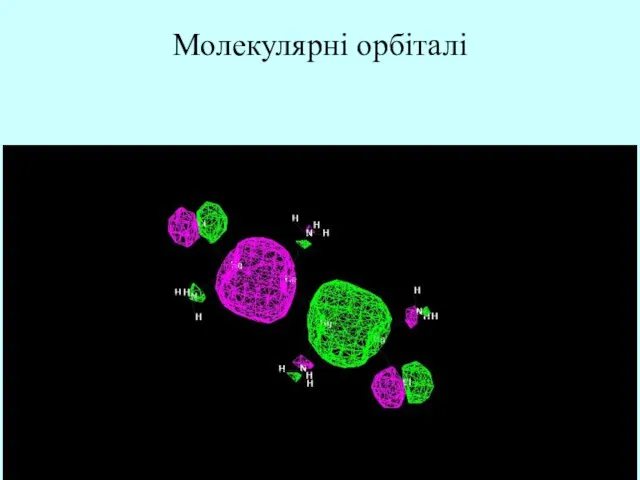
- 31. Молекулярні орбіталі
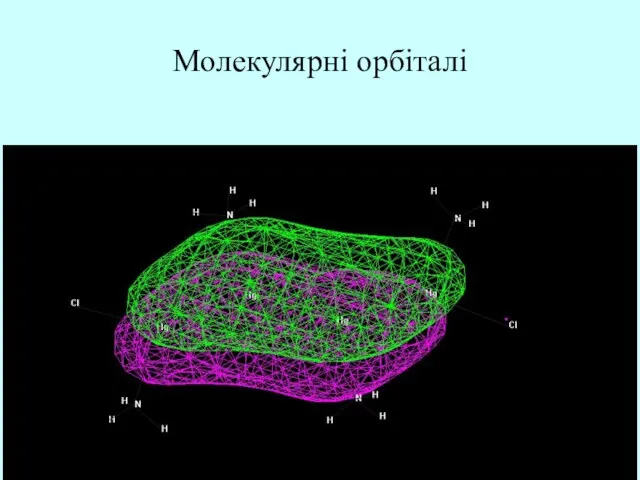
- 32. Молекулярні орбіталі
- 33. Молекулярні орбіталі
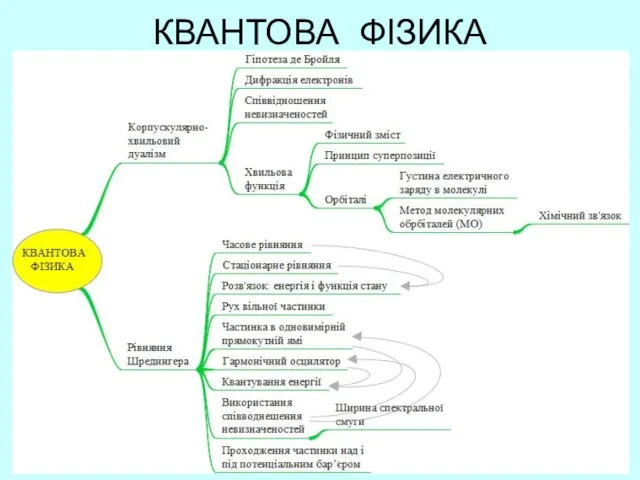
- 34. КВАНТОВА ФІЗИКА
- 35. Квантово-механічні задачі 1. Рівняння Шредінґера 2. Рух вільної частинки. 3. Частинка в одновимірній прямокутній потенціальній ямі.
- 36. Рівняння Шредінгера Хвилі де-Бройля мають статистичне трактування. Цей факт та співвідношення невизначеностей вимагають, щоб рівняння руху
- 37. Рівняння Шредінгера Таке рівняння справедливе для довільної частинки з v Розглянемо вільну частинку, якій відповідає хвиля
- 38. Рівняння Шредінгера Знайдемо похідні Звідси Ці дані підставимо в формулу
- 39. Рівняння Шредінгера Такий же вигляд має рівняння Шредінгера при U = 0. Якщо існує силове поле,
- 40. Стаціонарне рівняння Шредінгера Шукаємо розв'язок у вигляді Підставивши в рівняння Шредінгера, отримаємо Це і є стаціонарне
- 41. Рух вільної частинки Застосуємо рівняння Шредінгера до руху вільної частинки. Енергія E = Ek. Частинний розв'язок:
- 42. Рух вільної частинки Маємо суперпозицію двох плоских хвиль однакової частоти ω = Е/ħ. Порівняння з виразом
- 43. Рух вільної частинки Ймовірність знайти частинку в певній точці простору Отже, як і слід чекати для
- 44. Частинка в одновимірній прямокутній потенціальній ямі Розглянемо прямокутну потенціальну яму, для якої Рівняння Шредінгера Яма має
- 45. Частинка в одновимірній прямокутній потенціальній ямі В межах ями Розв'язок Оскільки ψ(0) = 0, то В
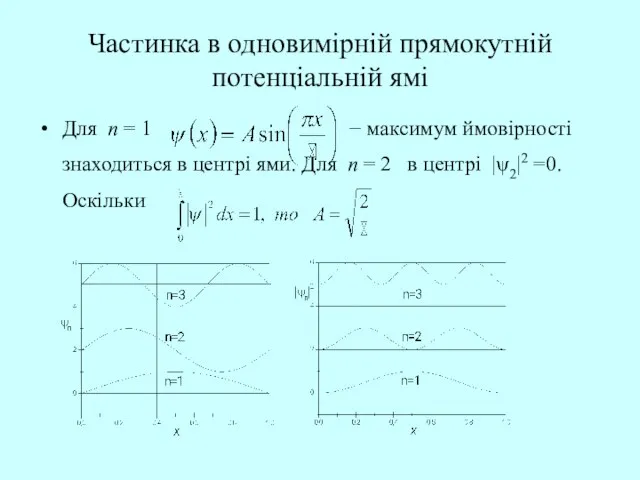
- 46. Частинка в одновимірній прямокутній потенціальній ямі Для n = 1 − максимум ймовірності знаходиться в центрі
- 47. Частинка в одновимірній прямокутній потенціальній ямі Різниця енергій двох сусідніх рівнів збільшується зі збільшенням n. Якщо
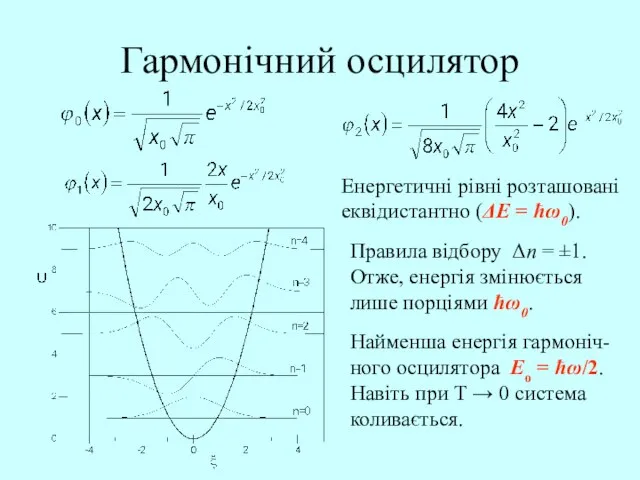
- 48. Гармонічний осцилятор Хвильове рівняння, яке описує гармонічний осцилятор, має вигляд: Розв’язком цього рівняння є: En =
- 49. Гармонічний осцилятор Енергетичні рівні розташовані еквідистантно (ΔE = ћω0). Правила відбору Δn = ±1. Отже, енергія
- 50. Використання співвідношення невизначеностей Розрахуємо співвідношення невизначеностей для розрахунку енергій в одновимірній потенціальній ямі та для гармонічного
- 51. Використання співвідношення невизначеностей Тепер розрахуємо енергію гармонічного осцилятора: Звідси
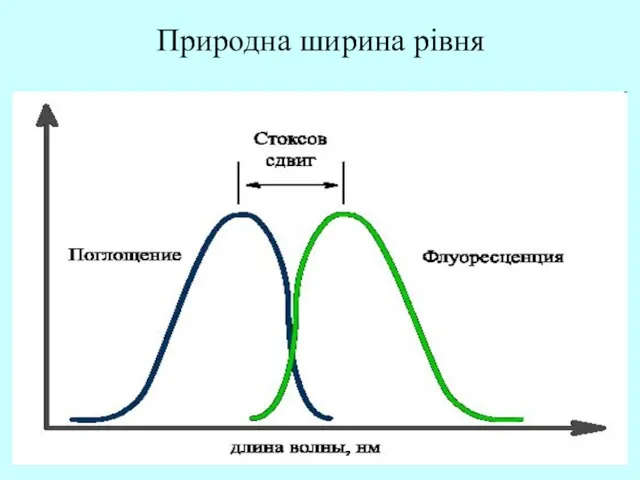
- 52. Природна ширина рівня
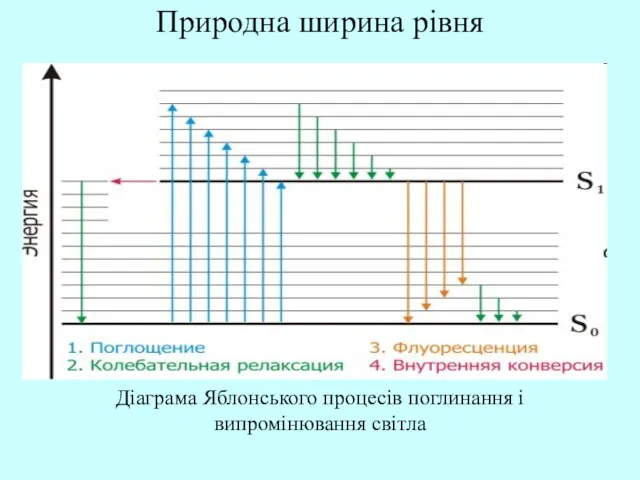
- 53. Природна ширина рівня Діаграма Яблонського процесів поглинання і випромінювання світла
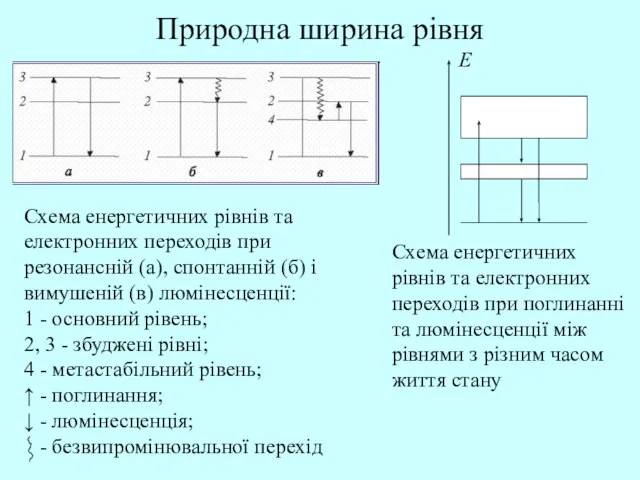
- 54. Схема енергетичних рівнів та електронних переходів при резонансній (а), спонтанній (б) і вимушеній (в) люмінесценції: 1
- 55. Природна ширина рівня ШИРИНА РІВНЯ – невизначеність енергії квантово-механічної системи (атома, молекули та ін), що має
- 56. Природна ширина рівня Час життя Δτ, а отже, і ширина рівня обумовлені можливістю квантових переходів системи
- 57. Тунельний ефект Розглянемо бар'єр прямокутної форми на шляху руху частинок. В класичній фізиці частинка з E
- 58. Тунельний ефект Для областей 1 і 3 Для області 2 Розв'язок В області 3 є лише
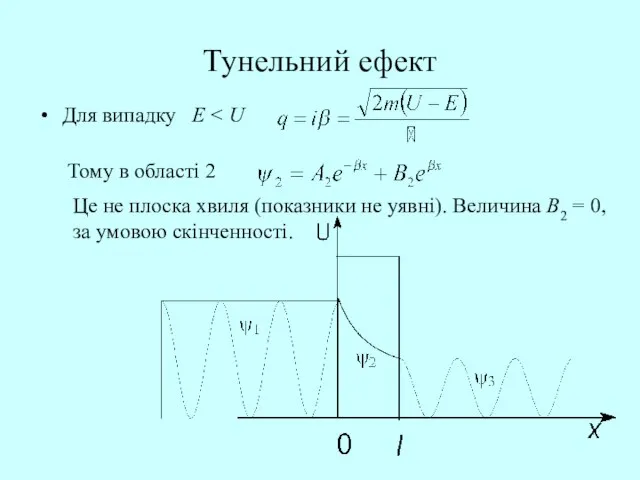
- 59. Тунельний ефект Для випадку E Тому в області 2 Це не плоска хвиля (показники не уявні).
- 60. Тунельний ефект Ймовірність проходження електрона через бар'єр (коефі-цієнт прозорості) дорівнює Щоб знайти величину D, необхідно використати
- 61. Тунельний ефект Тепер знайдемо D Для бар'єра довільної форми З формули випливає, що величина D залежить
- 62. Тунельний ефект Тунелювання є квантовим ефектом, який існує внаслідок співвідношення невизначеностей. Невизначеність Δр на відрізку Δх
- 64. Скачать презентацию














































 Презентация на тему Километр (3 класс)
Презентация на тему Километр (3 класс) Известные имена. Софья Ковалевская
Известные имена. Софья Ковалевская Особенности кризиса 2008-2ХХХгг.
Особенности кризиса 2008-2ХХХгг. Графика
Графика Общие вопросы антибактериальной терапии
Общие вопросы антибактериальной терапии Составное глагольное сказуемое
Составное глагольное сказуемое Ch1 - Lecture2
Ch1 - Lecture2 Увеличительные приборы
Увеличительные приборы Болат өндірісінің теориясы мен технологиясы
Болат өндірісінің теориясы мен технологиясы Международные транспортные коридоры
Международные транспортные коридоры Гравюра
Гравюра Природно-климатические условия среды обитания и здоровье человека. Акклиматизация и ее гигиеническое значение. Солнечная радиаци
Природно-климатические условия среды обитания и здоровье человека. Акклиматизация и ее гигиеническое значение. Солнечная радиаци Кайнозойская эра
Кайнозойская эра Греция сегодня
Греция сегодня Алгоритм с ветвлением в среде программирования Turbo Pascal
Алгоритм с ветвлением в среде программирования Turbo Pascal ИСКУССТВО ОРИГАМИ
ИСКУССТВО ОРИГАМИ Параметры областного бюджета Тверской области на 2008-2010 годы
Параметры областного бюджета Тверской области на 2008-2010 годы 90 лет ГТО
90 лет ГТО Декоративные народные промыслы
Декоративные народные промыслы Возникновение и развитие логистики
Возникновение и развитие логистики PO
PO Композиция (от лат. compositio)
Композиция (от лат. compositio) Библиотека – как информационная база. Структура библиотеки ВГУЭС
Библиотека – как информационная база. Структура библиотеки ВГУЭС Психологические особенности младших школьников с общим недоразвитием речи
Психологические особенности младших школьников с общим недоразвитием речи Презентация на тему Эра космонавтики
Презентация на тему Эра космонавтики  Чернышов Вадим Геннадьевич. Сертификат участника
Чернышов Вадим Геннадьевич. Сертификат участника САПР ТП ВЕРТИКАЛЬ
САПР ТП ВЕРТИКАЛЬ История развития психопатологии в России
История развития психопатологии в России