Слайд 2Электролиз
- совокупность процессов, происходящих при прохождении постоянного электрического тока через электрохимическую систему,

состоящую из двух электродов и расплава или раствора электролита.
Слайд 3Электролиз расплава бромида свинца
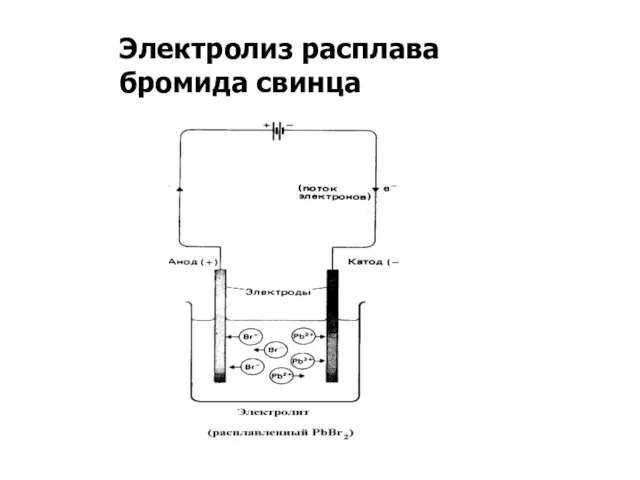
Слайд 4Процессы на электродах электролизера
Анод (+): окисление 2Br- - 2ē → Br2
Катод

(-): восстановление Pb2+ + 2ē → Pb
Слайд 5Особенности электролиза водных растворов
1. Имеется несколько типов частиц, которые могут окисляться на

аноде и восстанавливаться на катоде.
Пример:
Водный раствор хлорида натрия содержит анионы: Cl-, катионы: Na+, а также молекулы воды.
Какие частицы будут окисляться на аноде и восстанавливаться на катоде?
Слайд 6
Последовательность реакции на электродах различных ионов определяется:
1. Химической природой электродов
2. Окислительно-восстановитель-ным

(электродным) потенциалом реакции
Слайд 7
1. Инертные и активные электроды
Инертные электроды: Pt, графит в реакциях на электродах

не участвуют.
Активные электроды: Cu, Fe, Zn, Ni… принимают активное участие в реакциях.
Например, в нашем случае:
Анод (окисление): Сu - 2e = Cu2+
φо= +0,34 В
Слайд 82. Окислительно-восстановительный потенциал реакции (на инертном электроде)
А) На катоде сначала восстанавливаются частицы,

реакции которых соответствует больший окислительно-восстановительный (электродный) потенциал;
Слайд 9Решение
Принципиально возможно восстановление на катоде следующих частиц:
1. Na+ + ē → Na

φо1= -2,7 В
2. 2H2O + 2ē → H2+2OH- φо2= -0,83 В
Самый большой окислительно-восстановительный потенциал имеет 2 реакция. Поэтому на катоде будет восстанавливаться вода (реакция 2).
Слайд 10Б) На аноде сначала окисляются частицы, реакции которых соответствует меньший окислительно-восстановительный потенциал.
Сначала

восстанавливаются бескислородные анионы, затем вода, затем кислородсодержашие анионы.
Слайд 11В нашем примере принципиально возможно окисление на аноде следующих частиц:
1. 2H2О -

4ē → 4H+ + О2 φо1= +1,23 В
2. 2Cl- - 2ē → Cl2 φо2= +1,36 В
φо1< φо2 Следовательно на аноде должна окисляться вода, однако на большинстве электродов окисляются хлорид-ионы.
Это связано с явлением, которое называется перенапряжение.
Слайд 12 Перенапряжение
- добавочная по отношению к расчетной ЭДС, которую нужно приложить к
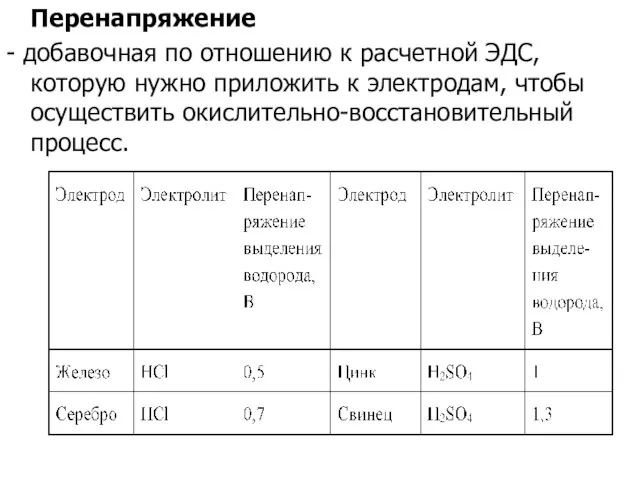
электродам, чтобы осуществить окислительно-восстановительный процесс.
Слайд 13
Законы Фарадея (1827)
1. Масса выделившегося на электроде вещества пропорциональна количеству электричества, прошедшего

через электролит.
2. Одинаковые количества электричества выделяют на электродах массы веществ, пропорциональные молярным массам их химических эквивалентов.
Слайд 14
Постоянная Фарадея
F = 96500 Кл/моль экв.
n экв(B) = Q/F= It/F
Q- количество

электричества, Кл
I - ток, А
t - время, с
m(B) = Mэкв n экв(B) = MэквIt/F
Слайд 15
Пример
Через расплавленный бромид свинца пропускали ток силой 2А в течение 30

минут.
Какая масса свинца выделилась?
Слайд 16Решение
Катод (-): восстановление Pb2+ + 2ē → Pb
Из уравнения: n(Pb)/n(ē) =

½
n(ē) = Q/F = It/F =
=2A·1800c/96500Kл/моль ē = 0,037 моль
n(Pb) = ½ ·0,037 моль= 0,0185 моль
m(Pb) = 0,0185 моль·207 г/моль = 3,83 г
Ответ: выделилось 3,83 г свинца
Слайд 17
Задача
Сколько времени нужно пропускать ток 10 А через раствор поваренной соли, чтобы

получить 44,8 л хлора (н.у.)?
Слайд 18Решение
Анод (-): окисление 2Сl- - 2ē → Cl2
n(Cl2) = 44,8 л

/22,4 л/моль = 2 моль
Из уравнения:
n(Cl2)/n(ē) = ½n(ē) n(ē) = 2 n(Cl2) = 4 моль
n(ē) = Q/F = It/F =
=10A·t c/96500Kл/моль ē = 4 моль
t c = 38600 c
Ответ: Ток следует пропускать 38600 c
Слайд 19Темы коротких сообщений
Современные ингибиторы коррозии: история создания, химический состав, области применения.

Протекторная защита и электрозащита металлов от коррозии: принцип действия, области применения.
Гальванопластика: история, принцип действия, области применения.
Использование электролиза для создания газовых смесей для дыхания под водой: электроланг А.Н. Лодыгина, системы жизнеобеспечения современных подводных лодок.


















 Преференции членов СНО
Преференции членов СНО Презентация на тему Профессии бывают разные
Презентация на тему Профессии бывают разные Ответственность, предусмотренная за нарушение требований трудового права, охраны труда и промышленной безопасности
Ответственность, предусмотренная за нарушение требований трудового права, охраны труда и промышленной безопасности Проблема проекта: Ненадлежащий вид электричек в Москве
Проблема проекта: Ненадлежащий вид электричек в Москве Я и мои права
Я и мои права Лекція 6
Лекція 6 Математика вокруг нас
Математика вокруг нас Афоризмы. Дружба
Афоризмы. Дружба Договор мены
Договор мены Форма государственного правления Российской Федерации
Форма государственного правления Российской Федерации Битумы (от лат. bitumen горная смола), твердые или смолоподобные продукты. Свойства битумов зависят от способов производства, качества
Битумы (от лат. bitumen горная смола), твердые или смолоподобные продукты. Свойства битумов зависят от способов производства, качества  Ata
Ata Юрий Визбор
Юрий Визбор Презентация на тему Становление личностных характеристик ученика начальной школы
Презентация на тему Становление личностных характеристик ученика начальной школы  Дизайн проект помещений пилотного центра занятости ГКУ ЦЗН г. Волгограда
Дизайн проект помещений пилотного центра занятости ГКУ ЦЗН г. Волгограда Still loving you
Still loving you Особенности электроснабжения обогатительных фабрик. Категории качества электроэнергии. Лекция №1
Особенности электроснабжения обогатительных фабрик. Категории качества электроэнергии. Лекция №1 Александр Анатольевич Емельянов Кафедра Математических и инструментальных методов экономики (МиИМЭ) Современные аспекты и раз
Александр Анатольевич Емельянов Кафедра Математических и инструментальных методов экономики (МиИМЭ) Современные аспекты и раз Реконструкция
Реконструкция Римское право
Римское право Город, улица, микрорайон
Город, улица, микрорайон Презентация на тему Перспективы использования интерактивных технологий в учебном процессе
Презентация на тему Перспективы использования интерактивных технологий в учебном процессе О пчелах, колоколах и вечном двигателе
О пчелах, колоколах и вечном двигателе Материнство глазами художников
Материнство глазами художников Как пополнить электронный кошелек «RBK money» через Интернет-банк Банка Русский Стандарт
Как пополнить электронный кошелек «RBK money» через Интернет-банк Банка Русский Стандарт Особенности построения сибирской избы
Особенности построения сибирской избы Презентация на тему Демографические перспективы
Презентация на тему Демографические перспективы 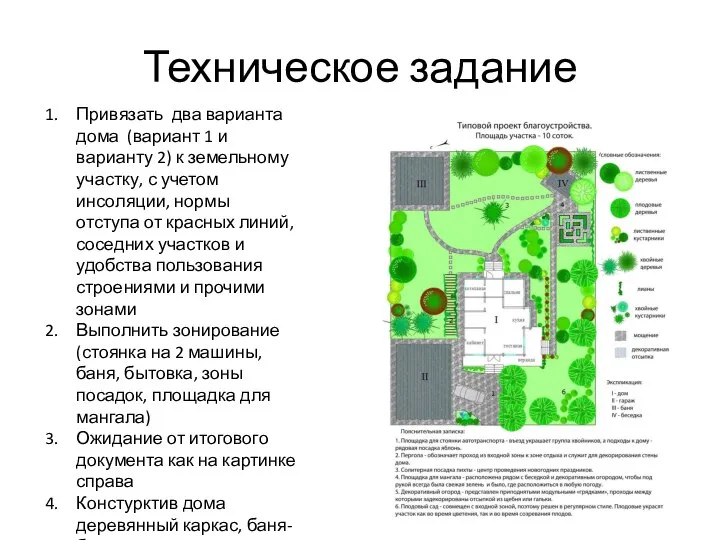 Техническое задание: привязать два варианта дома (вариант 1 и вариант 2) к земельному участку
Техническое задание: привязать два варианта дома (вариант 1 и вариант 2) к земельному участку