Содержание
- 2. Marcello Malpighi 10.03.1628 – 29.11.1694 “Nature, in order to carry out the marvelous operations in animals
- 3. Bruce Alberts “The entire cell can be viewed as a factory that contains an elaborate network
- 4. Как устроены сложные механизмы?
- 5. Биологические моторы
- 6. Молекулярные машины - основные функции: упаковщики, носильщики, сборщики, уничтожители
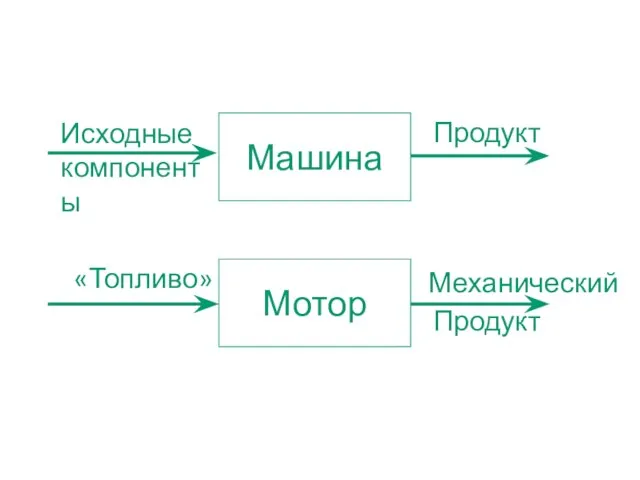
- 7. Мотор «Топливо» Продукт Механический
- 8. Примеры молекулярных моторов 1. Cytoskeletal motors 2. Nucleic acid-based motors Причины интереса к молекулярным моторам: 1.
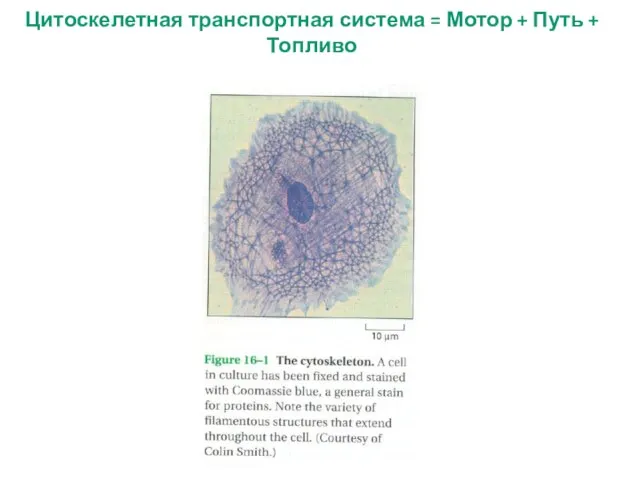
- 9. Цитоскелетная транспортная система = Мотор + Путь + Топливо
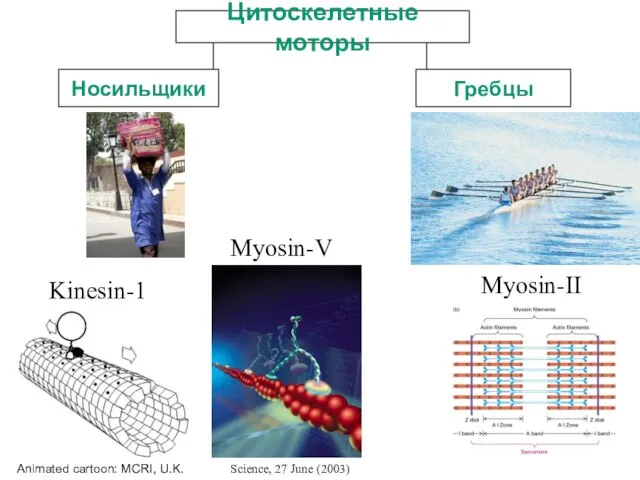
- 10. Цитоскелетные моторы Носильщики Гребцы Animated cartoon: MCRI, U.K. Kinesin-1 Myosin-V Myosin-II Science, 27 June (2003)
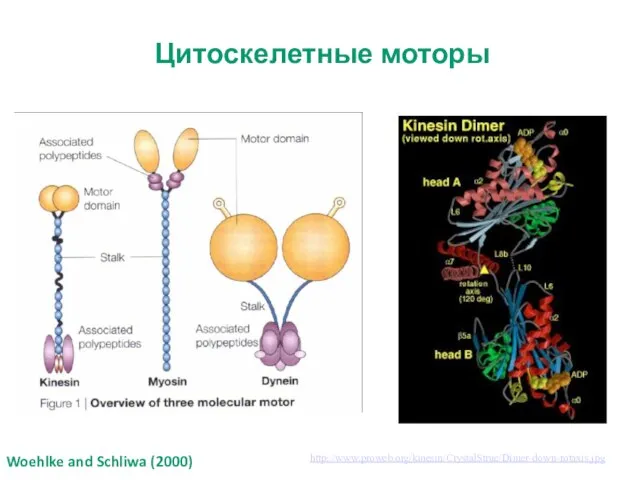
- 11. Woehlke and Schliwa (2000) Цитоскелетные моторы http://www.proweb.org/kinesin/CrystalStruc/Dimer-down-rotaxis.jpg
- 12. Линейные биологические моторы Все линейные биологические моторы превращают энергию гидролиза АТФ в механическую работу Белки-моторы передвигаются
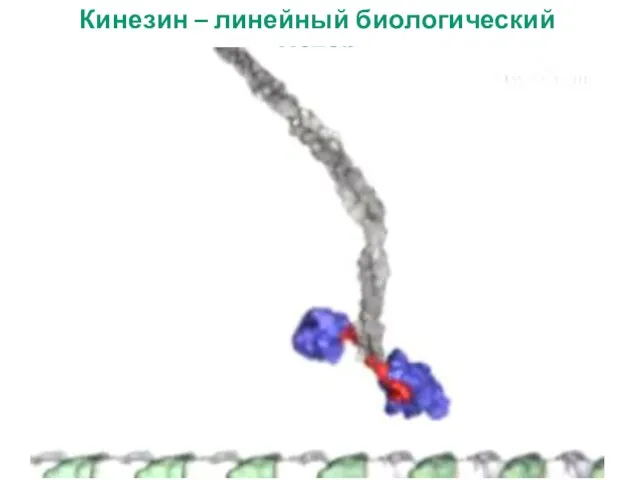
- 13. Кинезин Кинезины — суперсемейство моторных белков эукариотических клеток. Кинезины двигаются по микротрубочкам, используя энергию гидролиза АТФ.
- 14. Кинезин – линейный биологический мотор
- 15. Миозин Миозины — семейство белков, являющихся моторами цитоскелета системы микрофиламентов. Миозин — фибриллярный белок, один из
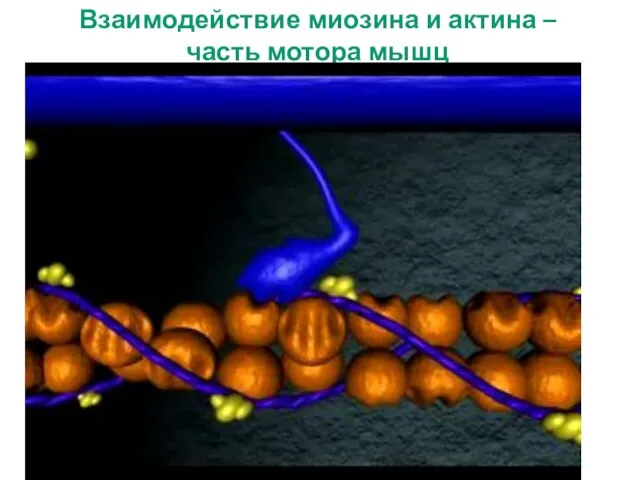
- 16. Взаимодействие миозина и актина – часть мотора мышц
- 17. Миозин Единичная головка миозина двигается с регулярностью шага 5,5 нм вдоль нити актина Молекула миозина генерирует
- 18. Динеин Динеины — группа моторных белков, способных перемещаться по поверхности микротрубочек цитоскелета, и транформирующих химическую энергию,
- 19. Молекулярные машины процессинга нуклеиновых кислот
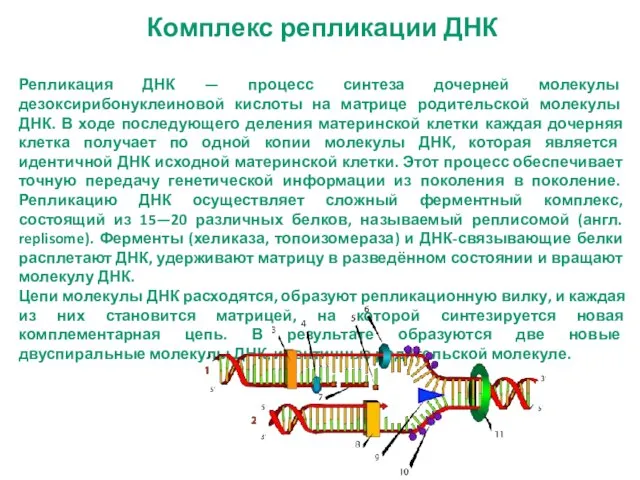
- 20. Комплекс репликации ДНК Репликация ДНК — процесс синтеза дочерней молекулы дезоксирибонуклеиновой кислоты на матрице родительской молекулы
- 21. Комплекс репликации ДНК
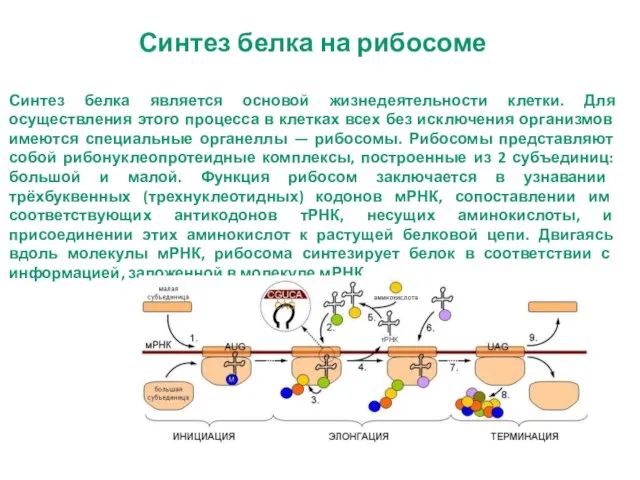
- 22. Синтез белка на рибосоме Синтез белка является основой жизнедеятельности клетки. Для осуществления этого процесса в клетках
- 23. Трансляция
- 24. Роторные молекулярные моторы – АТФ-синтаза В 60-70 годах XX века Пол Бойер (Paul Delos Boyer) -
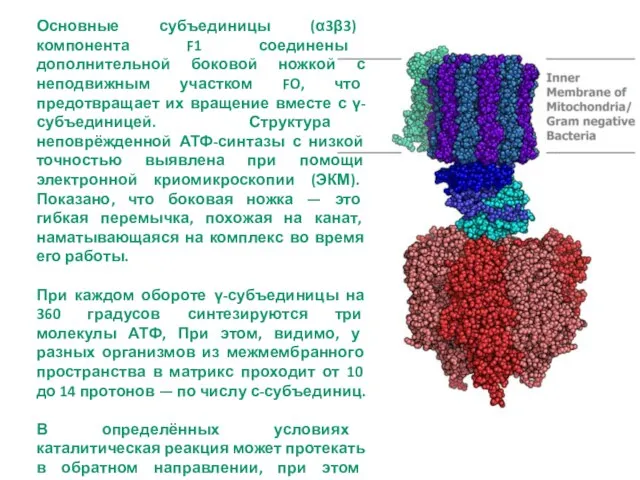
- 25. Основные субъединицы (α3β3) компонента F1 соединены дополнительной боковой ножкой с неподвижным участком FO, что предотвращает их
- 26. Роторные молекулярные моторы – АТФ-синтаза
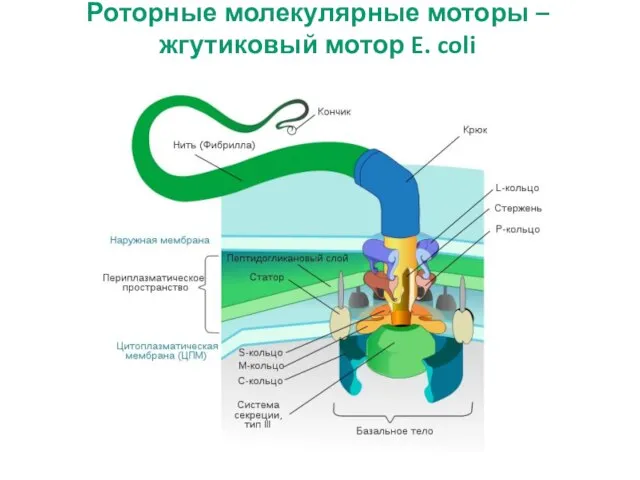
- 27. Роторные молекулярные моторы – жгутиковый мотор E. coli
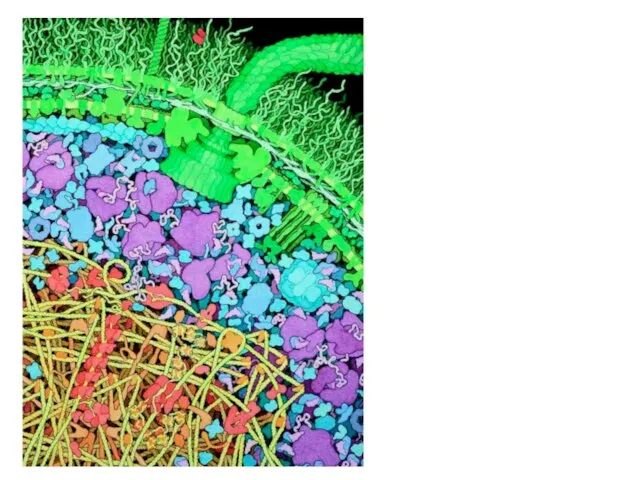
- 28. Роторные молекулярные моторы – жгутики Жгутик — поверхностная структура, присутствующая у многих прокариотических и эукариотических клеток
- 31. Роторные молекулярные моторы – жгутиковый мотор E. coli
- 32. В E. coli жгутиковый мотор может вращаться в обоих направлениях. Жгутиковые моторы могут развивать скорость 300
- 33. Перспективы На основе принципов работы биологических молекулярных моторов, с использованием достижений нанотехнологии создаются миниатюрные механические наномоторы
- 35. Скачать презентацию





















 БУР для наставників
БУР для наставників Экстремальные ситуации в природе
Экстремальные ситуации в природе Элементы безопасности кровли
Элементы безопасности кровли Интегрированная логистическая поддержка
Интегрированная логистическая поддержка Как собирать грибы
Как собирать грибы Музыкальная живопись и живописная музыка. Импрессионизм
Музыкальная живопись и живописная музыка. Импрессионизм Презентация на тему ГЛАВНЫЕ НАПРАВЛЕНИЯ ЭВОЛЮЦИИ
Презентация на тему ГЛАВНЫЕ НАПРАВЛЕНИЯ ЭВОЛЮЦИИ  Игра «Здоровый образ жизни»
Игра «Здоровый образ жизни» Туристский ваучер
Туристский ваучер Экология и здоровье человека
Экология и здоровье человека ПРОЕКТ«Мы любим Байкал 2020»
ПРОЕКТ«Мы любим Байкал 2020» УМК «Перспективная начальная школа»
УМК «Перспективная начальная школа» Ботинки с самозавязывающимися шнурками
Ботинки с самозавязывающимися шнурками EnergoJump
EnergoJump Матвеева Надежда Вианоровна
Матвеева Надежда Вианоровна Процессы управления проектами
Процессы управления проектами Презентация на тему Закаливание В мире есть лишь две абсолютные ценности: чистая совесть и здоровье
Презентация на тему Закаливание В мире есть лишь две абсолютные ценности: чистая совесть и здоровье  Тест SAM русский язык
Тест SAM русский язык Алгоритм работы школы по подготовке педагогов к участию в конкурсе лучших учителей в рамках приоритетного национального проекта
Алгоритм работы школы по подготовке педагогов к участию в конкурсе лучших учителей в рамках приоритетного национального проекта  SEO оптимизация за сайтове на малкия и среден бизнес
SEO оптимизация за сайтове на малкия и среден бизнес Городской центр психолого-медико-социального сопровождения, как ресурсный центр муниципальной системы образования г.Ярославля
Городской центр психолого-медико-социального сопровождения, как ресурсный центр муниципальной системы образования г.Ярославля Website owners identification
Website owners identification Возможно ли на этой линии что либо изобразить в этом же стиле?
Возможно ли на этой линии что либо изобразить в этом же стиле? Поиск информации в сети Интернет
Поиск информации в сети Интернет Ноутбуки. Устройство ноутбука
Ноутбуки. Устройство ноутбука Гражданин РФ (1)
Гражданин РФ (1) Начальная военная подготовка
Начальная военная подготовка Глагол
Глагол