Содержание
- 2. Основные принципы определения содержания КИМ ГИА-9 соответствие содержания экзаменационной работы объему учебного времени, отводимого на изучение
- 3. Структура варианта экзаменационной работы В работе выделены 3 части, различающиеся по назначению, содержанию, уровню сложности и
- 4. Изменения в экзаменационной работе 2011 года Общее число заданий в варианте уменьшено до 22 (было 25).
- 5. Часть 1 Содержит 15 заданий с выбором ответа (базового уровня сложности). Их обозначение в работе: А1;
- 6. Примеры заданий Части 1 A1. Атом какого химического элемента имеет приведенную ниже схему строения? 1)аргона 2)кислорода
- 7. А2. От кислотных к оснóвным меняются свойства оксидов в ряду 1) CaO → SiO2 → SO3
- 8. А4. Такую же степень окисления, как и в SO2, сера имеет в соединении 1) K2SO4 2)
- 9. А6. К химическим явлениям относится процесс 1)измельчения сахара до состояния пудры 2)превращения воды в лед 3)появления
- 10. А8. Сокращенному ионному уравнению Ba2+ + SO42- = BaSO4↓ соответствует левая часть уравнения химической реакции 1)BaСl2
- 11. А10. Химическая реакция возможна между 1) оксидом фосфора(V) и оксидом калия 2) оксидом алюминия и водой
- 12. А12. И нитрат аммония, и нитрат цинка могут взаимодействовать с 1)гидроксидом калия 2)раствором хлорида натрия 3)разбавленным
- 13. А14. Прибор, изображённый на рисунке, используют для получения 1)аммиака 2)водорода 3)кислорода 4)азота А15. Массовая доля азота
- 14. Часть 2 Содержит 4 задания с кратким ответом (повышенного уровня сложности). Их обозначение в работе: В1;
- 15. Часть 2 В1. В ряду химических элементов Si – Ge – Sn 1)увеличивается число электронных слоев
- 16. В3. Установите соответствие между схемой превращения и изменением степени окисления окислителя в ней. СХЕМА ПРЕВРАЩЕНИЙ A)Cl2
- 17. В4. Установите соответствие между веществом и реагентами, с которыми оно может вступать в реакцию. ВЕЩЕСТВО A)железо
- 18. Часть 3 Содержит 3 задания с развернутым ответом. Их обозначение в работе: С1, С2 и С3.
- 19. С1. Дана схема превращений: Cu → Cu(NO3)2 → X CuO Напишите молекулярные уравнения реакций, с помощью
- 20. После пропускания через раствор гидроксида калия 1,12 л углекислого газа (н.у.) получили 138 г раствора карбоната
- 21. C3. На занятиях химического кружка учащиеся исследовали кристаллическое вещество белого цвета. В результате добавления к нему
- 22. Определен состав вещества и записано его название: 1) NH4Cl – хлорид аммония. Составлены 2 уравнения реакций,
- 23. Шкала пересчета баллов 2011г. В 2011 г. предлагалась следующая шкала пересчета полученных баллов в школьную отметку:
- 24. Для получения отметки «4» учащимся необходимо набрать 18 баллов, например, выполнив все заданий базового уровня (Части
- 26. Скачать презентацию























 Shape
Shape Мой кумир - Джессика Альба
Мой кумир - Джессика Альба ЦО № 429 – ресурсный центр инновационной сети «Обучение по индивидуальным учебным планам в старшей школе»
ЦО № 429 – ресурсный центр инновационной сети «Обучение по индивидуальным учебным планам в старшей школе» О РАЗРАБОТКЕ МУНИЦИПАЛЬНЫХ ПРОГРАММ В ОБЛАСТИ ЭНЕРГОСБЕРЕЖЕНИЯ
О РАЗРАБОТКЕ МУНИЦИПАЛЬНЫХ ПРОГРАММ В ОБЛАСТИ ЭНЕРГОСБЕРЕЖЕНИЯ Изображение и реальность
Изображение и реальность Управление качеством в процессе закупок
Управление качеством в процессе закупок С 01 октября 2020 года денежные средства будут перечисляться банками только на карту Мир гражданам, получающим пособия
С 01 октября 2020 года денежные средства будут перечисляться банками только на карту Мир гражданам, получающим пособия Щи - национальное русское блюдо
Щи - национальное русское блюдо Век Просвещения
Век Просвещения Musical Britain
Musical Britain Проект по дизайну в сфере применения
Проект по дизайну в сфере применения «Последнее слово» Ильи Петрова. - презентация
«Последнее слово» Ильи Петрова. - презентация Формирование и развитие материально-технической базы АПК Украины
Формирование и развитие материально-технической базы АПК Украины Роль фольклора в процессе формирования духовно-нравственных качеств дошкольников
Роль фольклора в процессе формирования духовно-нравственных качеств дошкольников Конкурентные стратегииприложение к журналу «ЭТАП: Экономическая Теория, Анализ, Практика»
Конкурентные стратегииприложение к журналу «ЭТАП: Экономическая Теория, Анализ, Практика» ИНСТРУКЦИИ ПО ТЕХНИКЕ БЕЗОПАСНОСТИ НА УРОКАХ ТЕХНОЛОГИИ 5 и 6 классов
ИНСТРУКЦИИ ПО ТЕХНИКЕ БЕЗОПАСНОСТИ НА УРОКАХ ТЕХНОЛОГИИ 5 и 6 классов Презентация на тему Игры на развитие интеллектуальных способностей детей дошкольного возраста посредством ИКТ
Презентация на тему Игры на развитие интеллектуальных способностей детей дошкольного возраста посредством ИКТ The United Nations General Assembly
The United Nations General Assembly  ГРАФИЧЕСКИЕ ИНФОРМАЦИОННЫЕ МОДЕЛИ МОДЕЛИРОВАНИЕ И ФОРМАЛИЗАЦИЯ
ГРАФИЧЕСКИЕ ИНФОРМАЦИОННЫЕ МОДЕЛИ МОДЕЛИРОВАНИЕ И ФОРМАЛИЗАЦИЯ «Секреты выбора кредитных продуктов украинских банков»
«Секреты выбора кредитных продуктов украинских банков» Методика проведения международных маркетинговых исследований Дисциплина: Международный маркетинг Преподаватель: профессор ка
Методика проведения международных маркетинговых исследований Дисциплина: Международный маркетинг Преподаватель: профессор ка Повторение
Повторение Ранний период Христианской философии
Ранний период Христианской философии Бельмондо (фотографии)
Бельмондо (фотографии) Маркетинговое исследование пакетированных соков в городе Новороссийск
Маркетинговое исследование пакетированных соков в городе Новороссийск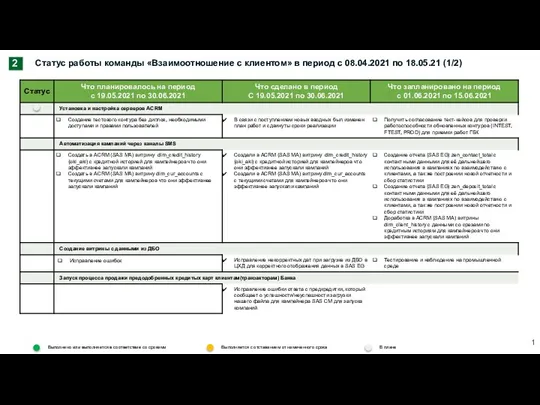 Статус работы команды Взаимоотношение с клиентом в период с 08.04.2021 по 18.05.21
Статус работы команды Взаимоотношение с клиентом в период с 08.04.2021 по 18.05.21 Электронная и цифровая техника в СЦБ
Электронная и цифровая техника в СЦБ Дистрибьюция фармпрепаратов в Украине. Тенденции развития
Дистрибьюция фармпрепаратов в Украине. Тенденции развития