Содержание
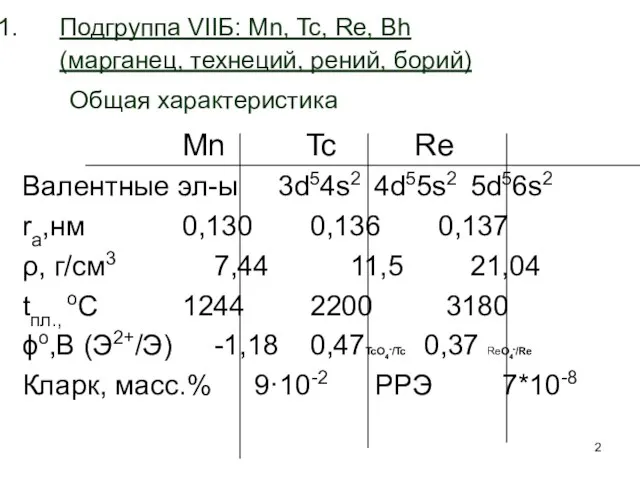
- 2. Подгруппа VIIБ: Mn, Tc, Re, Bh (марганец, технеций, рений, борий) Общая характеристика Mn Tc Re Валентные
- 3. Природные cоединения Mn: MnO2 - пиролюзит Tc: первый элемент, полученный искусственно (1937 г.), предсказан Д.И.Менделеевым в
- 4. Получение металлов Mn Сплав ферромарганец (Mn + Fe): MnO2 + Fe2O3 + C → (Mn +
- 5. Степени окисления Возможные: +2 +3 +4 +5 +6 +7 Характерные: Mn +2 +4 +6 +7 Tc,
- 6. Химические свойства металлов Э + Г2 → MnF3, MnF4, ReF6, ReCl5 Mn + O2 → MnO2
- 7. Химические свойства металлов Взаимодействие с кислотами Mn + HCl (H2SO4 разб.) → Re (Tc) + HCl,
- 8. Химические свойства металлов Re (Tc) + HNO3 → + NO + H2O (t) Re (Tc) +
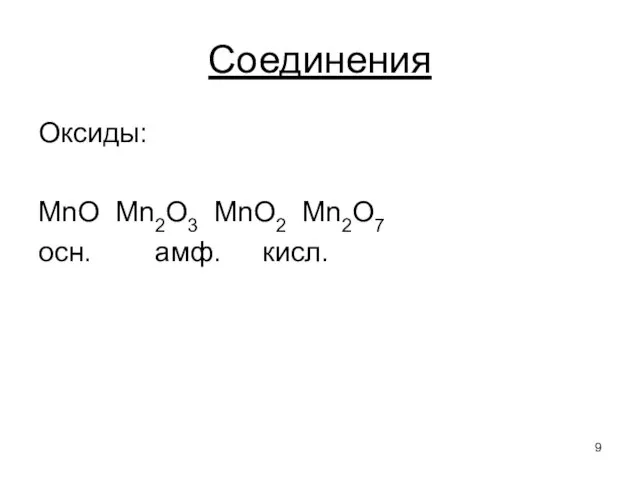
- 9. Оксиды: MnO Mn2O3 MnO2 Mn2O7 осн. амф. кисл. Соединения
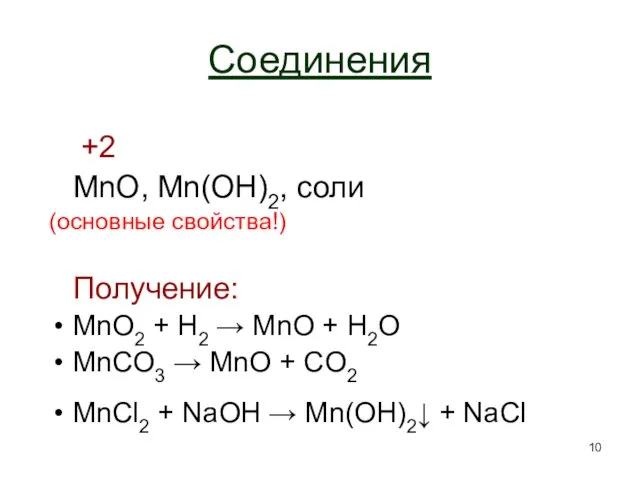
- 10. Соединения +2 MnO, Mn(OH)2, соли (основные свойства!) Получение: MnO2 + H2 → MnO + H2O MnCO3
- 11. Характерные соединения Свойства: MnO + HCl → MnCl2 + H2O Mn(OH)2 + HCl → … MnO,
- 12. Характерные соединения +3 Mn2O3 Получение: MnO2 → Mn2O3 + O2 (500oC) Свойства: Mn2O3 + H2SO4(р) →
- 13. Характерные соединения +4 MnO2, TcO2, ReO2 - черные Получение: MnO2 – пиролюзит NH4ReO4 → ReO2 +
- 14. Характерные соединения Свойства: MnO2 – химически инертен (высокая Eк.р.) MnO2 – амфотерен MnO2 + NaOH →
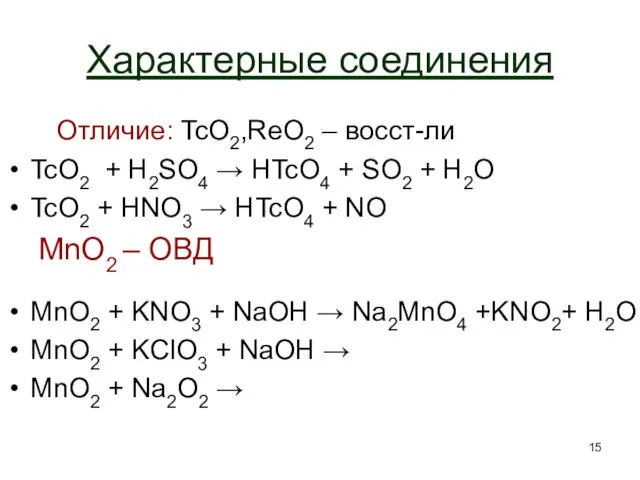
- 15. Характерные соединения Отличие: TcO2,ReO2 – восст-ли TcO2 + H2SO4 → HTcO4 + SO2 + H2O TcO2
- 16. Характерные соединения +6 Оксиды MnO3 TcO3 ReO3 не сущ. ув-ся устойчивость Получение: Re2O7 (Tc2O7) + Re→
- 17. Характерные соединения Кислоты, соли MnO42- TcO42- ReO42- манганат технат ренат Получение: KЭO4 + K2SO3 + KOH
- 18. Характерные соединения Свойства: Ионы стабильны в щелочной среде: ЭO42- + H2O → ЭO4- + ЭO2 +
- 19. Характерные соединения +7 Оксиды Mn2O7 Tc2O7 Re2O7 tпл.оС 6 120 301 красный желтый желтый не устойчив
- 20. Характерные соединения Свойства: Mn2O7 → MnO2 + O2 (55оС) Mn2O7 + С2H5OH → MnO2 + CO2
- 21. Характерные соединения Кислоты, соли MnO4- TcO4- ReO4- перманганат пертехнат перренат HMnO4 – существует в р-рах с
- 22. Характерные соединения Получение KMnO4 В промышленности: 1) MnO2 + KOH + O2 → K2MnO4 + H2O
- 23. Характерные соединения HMnO4 – сильная кислота (как HCl), не устойчивая Перманганаты – термически неустойчивы KMnO4 →
- 25. Скачать презентацию


















 Научный руководитель: кандидат исторических наук, доцент Е.А. Красулин
Научный руководитель: кандидат исторических наук, доцент Е.А. Красулин - Мы делаем мир понятнее ДЛЯ ЧЕГО?
- Мы делаем мир понятнее ДЛЯ ЧЕГО? struktura-kpprimer-O4ZWKr
struktura-kpprimer-O4ZWKr Мезенская роспись
Мезенская роспись Кинезиологические упражнения
Кинезиологические упражнения Презентация на тему "Современный учитель : пути профессионального развития в новой школе" - скачать презентации по Педагогике
Презентация на тему "Современный учитель : пути профессионального развития в новой школе" - скачать презентации по Педагогике Вводные слова и вводные предложения. Знаки препинания при них
Вводные слова и вводные предложения. Знаки препинания при них УРОК№4
УРОК№4 Системы сигнализаций в сетях связи
Системы сигнализаций в сетях связи  Двоичная арифметика
Двоичная арифметика Урок математики «Геометрия площади» 6 класс
Урок математики «Геометрия площади» 6 класс Осциллограф ВМ8020
Осциллограф ВМ8020 Особенности развития личности подростка
Особенности развития личности подростка История Деда Мороза
История Деда Мороза Соревнования по корэш на празднике Сабантуй
Соревнования по корэш на празднике Сабантуй Разобьем части компьютера на четыре основные группы: 1. Системный блок; 2. Периферийные устройства. 3. Средства манипулирования; 4. Ср
Разобьем части компьютера на четыре основные группы: 1. Системный блок; 2. Периферийные устройства. 3. Средства манипулирования; 4. Ср Алгебра высказываний
Алгебра высказываний The history of chocolate
The history of chocolate Портфолио Эбаут Майселф
Портфолио Эбаут Майселф Уголовное право
Уголовное право Правила работы и безопасное поведение в кабинете информатике.
Правила работы и безопасное поведение в кабинете информатике. Публичное выступление на общественно значимую тему
Публичное выступление на общественно значимую тему Вербальное и невербальное общение
Вербальное и невербальное общение Завершение сделки. Процесс оказания помощи клиенту в принятии решения
Завершение сделки. Процесс оказания помощи клиенту в принятии решения Презентация на тему: Эстафета пионерских поколений
Презентация на тему: Эстафета пионерских поколений Проторенессанс. Искусство Возрождения
Проторенессанс. Искусство Возрождения Создание изделий из текстильных материалов Швейная машина
Создание изделий из текстильных материалов Швейная машина Николай Трофимович Грищенко
Николай Трофимович Грищенко