Слайд 2План
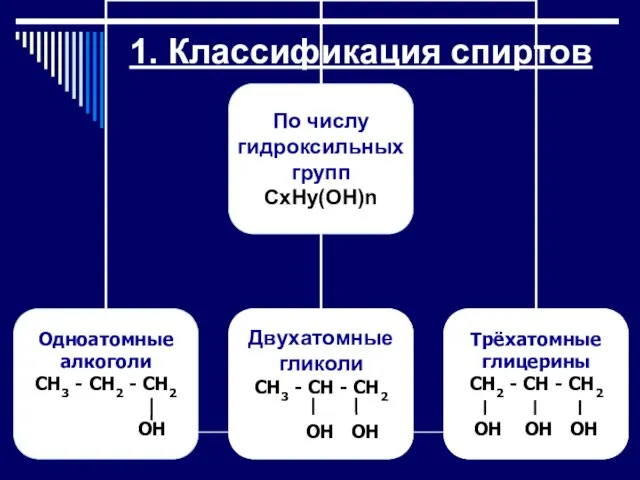
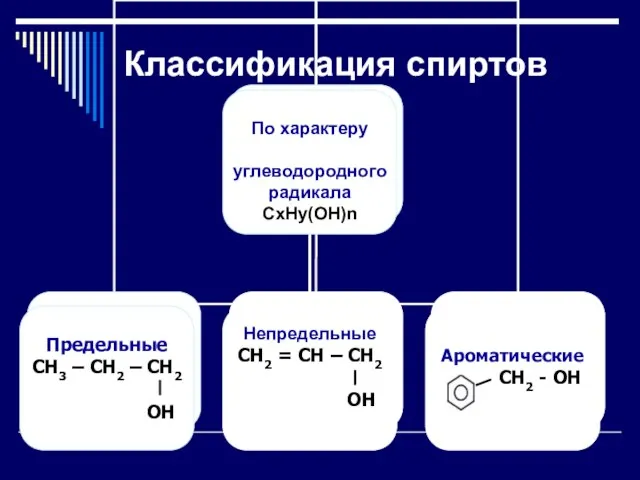
Классификация спиртов
Номенклатура спиртов
Изомерия спиртов
Отдельные представители
Метанол
Этанол
Этиленгликоль
Глицерин

Слайд 3Определение
Спирты́ (устаревшее алкого́ли) — органические вещества, содержащие одну или несколько

гидроксильных групп (гидроксил, OH), связанных углеводородным радикалом.
Общая формула спиртов CnH2n+1(OH)
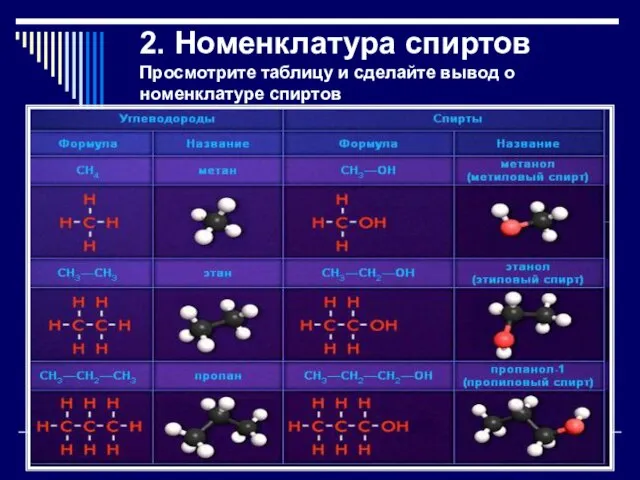
Слайд 62. Номенклатура спиртов
Просмотрите таблицу и сделайте вывод о номенклатуре спиртов
Слайд 7Вывод
Названия одноатомных спиртов образуются из названия углеводорода с самой длинной углеродной цепью,

содержащей гидроксильную группу, путём
добавления суффикса -ол.
Для многоатомных спиртов перед суффиксом -ол по-гречески (-ди-, -три-, ...) указывается количество гидроксильных групп.
Например: CH3-CH2-OH этанол
Слайд 83. Виды изомерии спиртов
Структурная
1. Положения
функциональной группы
2. Углеродной цепи

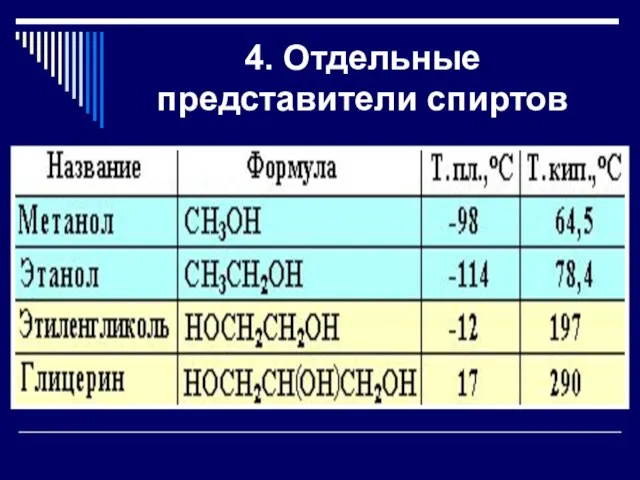
Слайд 94. Отдельные представители спиртов
Слайд 10Одноатомный спирт - метанол
Жидкость без цвета, с характерным запахом. Легче воды. Горит

бесцветным пламенем.
Применяется в качестве растворителя и
топлива в двигателях внутреннего сгорания, для получения красителей , лекарств, формальдегида.
Слайд 11Метанол
Историческое название –
древесный спирт.
Получают перегонкой твердых
пород дерева.
При попадании в

организм превращается в формальдегид и муравьиную кислоту.
Повреждает сетчатку глаза, вызывает гибель зрительного нерва, что приводит к полной потере зрения.
50 мл метанола – вызывает смерть.
Слайд 12Метанол - яд
Ядовитое действие метанола основано на поражении нервной и сосудистой системы.

Приём внутрь 5—10 мл метанола приводит к тяжёлому отравлению, а 30 мл и более — к смерти.
Слайд 13Одноатомный спирт - этанол
Бесцветная жидкость с характерным запахом и жгучим вкусом. Легче
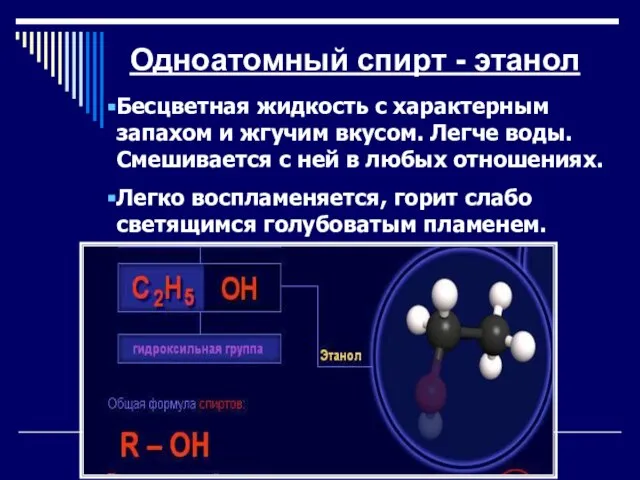
воды. Смешивается с ней в любых отношениях.
Легко воспламеняется, горит слабо светящимся голубоватым пламенем.
Слайд 14Этанол
Этанол – этиловый спирт.
Крепость спирта выражают в %.
Чистым медицинским спиртом

называют 96% (спирта 96% и 4% воды), абсолютный спирт -100% получают, обрабатывая химически связывающими веществами.
Технический спирт –денатурат, добавляют ядовитые вещества, плохо пахнущие, имеющие отвратительный вкус.
Получают брожением сахаристых веществ.
Слайд 15Применение этанола
Этиловый спирт употребляется при приготовлении различных спиртных напитков.
В медицине

для приготовления экстрактов из лекарственных растений, а также для дезинфекции.
В косметике и парфюмерии этанол — растворитель для духов и лосьонов.
Слайд 16Биологическое значение спиртов
Где белки – там и жизнь. В результате разрушения белков

в клетках наступает смерть. (Смертельная доза этанола – 7 г/кг веса).
Окисляясь в печени, спирты превращаются в альдегиды, т.е. вреден и страшен не сам спирт, а продукт его окисления.
Слайд 17Историческая справка.
Арабская легенда утверждает, что алхимик впервые получил спирт перегонкой и назвал

его «вода жизни»
1350 г. ирландский полководец Саваж алкоголем поднимал боевой дух воинов.
В 15 веке слово «алкоголь» применил немецкий врач Парацельс.
Слайд 18Историческая справка.
Водка в России появилась
в XVI веке.
В 1552 году

Иван Грозный устроил в России первый кабак, где водку подавали только опричникам. Спаивание народа безудержным становится в конце XIX века.
Первые попытки искоренить пьянство были предприняты в 1917 году.
Слайд 19Физиологическое значение
Этанол проникает в яйцеклетки и сперматозоиды, нарушая генетические структуры

(гены).
Употребление алкоголя повреждает мозг, разрушает нервные клетки.
Больные диабетом – даже при умеренном потреблении спиртного рискуют вызвать у себя коматозное состояние.
Алкоголь вызывает ожирение сердца, разрушает эритроциты, способствует развитию гипертонии.
Сильный вред наносит алкоголь печени.
Цирроз печени – удел многих злоупотребляющих.
Слайд 20 Социальные исследования показывают:
В пьющих семьях 40% детей недоразвитые и больные.

В таких семьях мертворожденные дети появляются в 2 раза чаще, а детская смертность в 3 раза выше, чем в непьющих семьях.
Одна рюмка водки снижает работоспособность на 20-30%.
До 40% правонарушений совершается в нетрезвом состоянии.
В состоянии опьянения совершается 55% всех краж, 79% грабежей, 69% нападений.
Средняя продолжительность жизни на 15-20 лет меньше у людей, употребляющих алкоголь.
Слайд 21Будущей России – здоровую молодежь!
Число людей, которые
себя погубили, куда
значительнее,

нежели
число погубленных
другими.
Леббок
Здоровое тело- продукт здравого рассудка.
Б. Шоу
Слайд 22Вино губит людей и их потомство.
Человек, употребляющий алкоголь –
теряет человеческий облик.
Наступает

деградация личности.
Слайд 23
Самая большая победа – это победа над собой,
а самое

постыдное – это быть побежденным своими страстями.
Демокрит.
Слайд 24Многоатомный спирт -этиленгликоль
Этиленгликоль — представитель предельных двухатомных спиртов — гликолей.
Название гликоли

получили вследствие сладкого вкуса многих представителей ряда (греч. «гликос» — сладкий).
Этиленгликоль - сиропообразная жидкость сладкого вкуса, без запаха, ядовит. Хорошо смешивается с водой и спиртом, гигроскопичен.
Слайд 25Применение этиленгликоля
Важным свойством этиленгликоля является способность понижать температуру замерзания воды, от чего

вещество нашло широкое применения как компонент автомобильных антифризов и незамерзающих жидкостей.
Он применяется для получения лавсана (синтетического волокна).
Слайд 26Этиленгликоль - яд
Дозы вызывающие смертельное отравление этиленгликолем варьируются в широких пределах

- от 100 до 600 мл. По данным ряда авторов смертельной дозой для человека является 50-150 мл. Смертность при поражении этиленгликолем очень высока и составляет более 60% всех случаев отравления.
Этиленгликоль быстро всасывается (в том числе через поры кожи) и в течение нескольких часов циркулирует в крови в неизмененном виде, достигая максимальной концентрации через 2-5 часов. Затем его содержание в крови постепенно снижается, и он фиксируется в тканях.
Слайд 27Многоатомный спирт - глицерин
Глицерин – трехатомный предельный спирт. Бесцветная, вязкая, гигроскопичная, сладкая

на вкус жидкость. Смешивается с водой в любых отношениях , хороший растворитель. Реагирует с азотной кислотой с образованием нитроглицерина. С карбоновыми кислотами образует жиры и масла.
Слайд 28Применение глицерина
Применяется в производстве взрывчатых веществ нитроглицерина.
При обработке кожи.
Как компонент некоторых

клеёв.
При производстве пластмасс глицерин используют в качестве пластификатора.
В производстве кондитерских изделий и напитков (как пищевая добавка E422).
Слайд 29Способы получения спиртов
Гидролиз галогеналканов:
CH3-CL+ NaOH CH3-OH + NaCL
Гидратация алкенов:
CH2=CH2+H2O

C2H5OH
Синтез метанола из синтез-газа
CO + 2H2 CH3-OH (при повышенном давлении, высокой температуре и катализатора оксида цинка)
Брожение глюкозы:
C6H12O6 2C2H5OH + 2CO2
Слайд 30
Химические свойства
I. Реакции с разрывом связи R-OH
Спирты реагируют с щелочными и щелочноземельными

металлами, образуя солеобразные соединения – алкоголяты.
2СH3CH2CH2OH + 2Na → 2СH3CH2CH2ONa + H2↑
Взаимодействие с органическими кислотами (реакция этерификации) приводит к образованию сложных эфиров.
CH3COОH + HOC2H5 → CH3COОC2H5 + H2O
Слайд 31
С галогеноводородами:
R–OH + HBr ↔ R–Br + H2O
II.
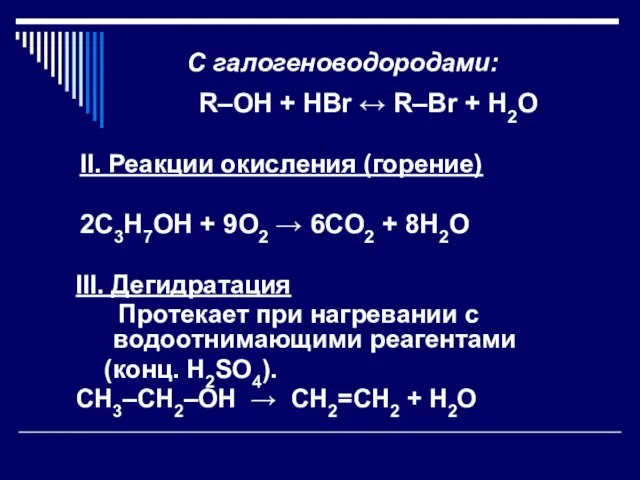
Реакции окисления (горение)
2С3H7ОH + 9O2 → 6СO2 + 8H2O
III. Дегидратация
Протекает при нагревании с водоотнимающими реагентами
(конц. Н2SO4).
CH3–CH2–OH → CH2=CH2 + H2O
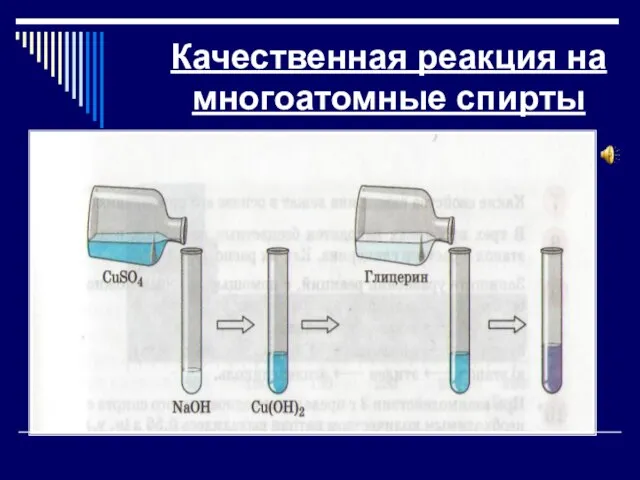
Слайд 32Качественная реакция на многоатомные спирты





























 Презентация на тему Весенние праздники русского народа
Презентация на тему Весенние праздники русского народа Предложение по международной франшизеDollar
Предложение по международной франшизеDollar Степень числа. Квадрат и куб числа
Степень числа. Квадрат и куб числа Презентация на тему Устный счет до десяти
Презентация на тему Устный счет до десяти  ПАТОЛОГИЯ ВСПОМОГАТЕЛЬНОГО АППАРАТА ГЛАЗА
ПАТОЛОГИЯ ВСПОМОГАТЕЛЬНОГО АППАРАТА ГЛАЗА ЗНАНИЯ И ОСНОВНЫЕ МОДЕЛИ ИХ ПРЕДСТАВЛЕНИЯ
ЗНАНИЯ И ОСНОВНЫЕ МОДЕЛИ ИХ ПРЕДСТАВЛЕНИЯ Что такое текст?
Что такое текст? Holidays go round and round
Holidays go round and round Линия. Штрих
Линия. Штрих Образы античной мифологии
Образы античной мифологии Past Continuous Прошедшее продолженное время
Past Continuous Прошедшее продолженное время « Использование И К т на уроках окружающего мира »
« Использование И К т на уроках окружающего мира » Современное состояние науки
Современное состояние науки Политическая система Великобритании
Политическая система Великобритании Долобене гель
Долобене гель Изготовления гусеницы из пластилина (2 класс)
Изготовления гусеницы из пластилина (2 класс) ПЕЙЗАЖ НАСТРОЕНИЯ
ПЕЙЗАЖ НАСТРОЕНИЯ Гранит Карелии
Гранит Карелии Рисунки Людмилы Тумановой
Рисунки Людмилы Тумановой Ответственность за нарушение требований охраны труда
Ответственность за нарушение требований охраны труда Физико-механические свойства горных пород
Физико-механические свойства горных пород Из опыта проектирования реальных объектов:проблемы и решения
Из опыта проектирования реальных объектов:проблемы и решения Программа «Гармония»под редакцией Н.Б. Истоминой
Программа «Гармония»под редакцией Н.Б. Истоминой Филимоновская игрушка. История игрушки
Филимоновская игрушка. История игрушки 10 причин отмечать День Рождения
10 причин отмечать День Рождения Как вести себя, если вы стали заложником террористов
Как вести себя, если вы стали заложником террористов факты о Jacquot Компания «JACQUOT» создана во Франции в 1920 году. Семейное предприятие Годовой оборот более – 160 млн.$ Объем производства –
факты о Jacquot Компания «JACQUOT» создана во Франции в 1920 году. Семейное предприятие Годовой оборот более – 160 млн.$ Объем производства –  Экскурсия по Москве
Экскурсия по Москве