Содержание
- 2. Домашнее задание: Выучить параграф № 33. Упражнение № 3,4. Повторить записи в тетради.
- 3. Разминка Органическая химия. Валентность. Химическое строение. Основные положения теории А.М. Бутлерова. Предельные углеводороды. Гомологический ряд. Гомологи
- 4. Приведите структурные формулы: 2-метил-3-этилгептан 2,2- дихлорпропан 2,3-диметилпентан 3-этилгексан 2-метилбутан 2-метил-3-хлороктан
- 5. Цель урока:1. Познакомиться с непредельными углеводородами как самостоятельным классом углеводородов. 2.Рассмотреть гомологию, изомерию и номенклатуру алкенов.
- 6. Алкены Определение алкенов Изомерия Номенклатура Химические свойства Получение Применение Физические свойства Назад
- 7. Непредельные, или ненасыщенные, УВ содержат кратные углерод- углеродные связи (>C=C Непредельными называются углеводороды, в молекулах которых
- 8. Алкены CnH2n, n>2 Алкены – это УВ, в молекулах которых два атома углерода связаны друг с
- 9. Изомерия Для алкенов возможны 4 типа изомерии: Изомерия углеродной цепи Изомерия положения двойной связи Цис,- транс-
- 10. CnH2n ан -- ен или илен В качестве главной выбирают цепь, включающую двойную связь, даже если
- 11. Физические свойства С2-С4 газы, С5-С16 жидкости, С>19 твердые, р Назад
- 12. Химические свойства Активны из-за наличия кратной связи Характерны реакции присоединения Гидрирование( присоединение водорода) СН3-СН=СН2 +Н2→ CH3-CH2-CH3(кат.Ni)
- 13. II. Реакция окисления Горение: С2Н4 +3О2 → 2СО2 +2Н2О
- 14. в)действие окислителей типа KMnO4 - качественная реакция.
- 15. III.Реакции полимеризации. Полимеризацией называется процесс соединения одинаковых молекул (мономеров), протекающий за счет разрыва кратных связей, с
- 16. Получение алкенов. 1)Крекинг нефтепродуктов С16Н34 --- С8Н18 + С8Н16( t ) 2) Дегидрирование алканов ( де
- 17. Применение алкенов
- 18. Приведите структурные формулы: а) 3-метилпентен-2, б) 2-метилбутен -1, в) 2-метил 3-хлорбутен -1, г) 3,3- диметилбутен-1 Приведите
- 19. Реакция присоединения воды называется: а)гидрирования б) дегидратации в) гидратации г) дегидрирования Какие вещества,названия которых приведены ниже,
- 20. Укажите значение относительной молекулярной массы для алкена с 6-ю атомами углерода в молекуле: а) 86 б)
- 22. Скачать презентацию



















 Вышивка. Образ птицы
Вышивка. Образ птицы Орфографическая диктовка
Орфографическая диктовка Для сх
Для сх Натюрморт
Натюрморт Права несовершеннолетних
Права несовершеннолетних СТОП вырубке ёлок!
СТОП вырубке ёлок! Русский мир
Русский мир Исследование развития речи детей старшего дошкольного возраста в игровой деятельности
Исследование развития речи детей старшего дошкольного возраста в игровой деятельности Предпрофильная подготовка и профильное обучение. Государственная (итоговая) аттестация выпускников
Предпрофильная подготовка и профильное обучение. Государственная (итоговая) аттестация выпускников Физиология мотивации
Физиология мотивации Маркетинговая стратегия
Маркетинговая стратегия СОЦИАЛЬНАЯ МОБИЛЬНОСТЬ
СОЦИАЛЬНАЯ МОБИЛЬНОСТЬ  Иконы православных праздников
Иконы православных праздников Олимпийские игры в Древней Греции
Олимпийские игры в Древней Греции Бумажная филигрань Бумагокручение Квиллинг
Бумажная филигрань Бумагокручение Квиллинг Бенчмаркинг, как инструмент управления организацией
Бенчмаркинг, как инструмент управления организацией Стандартизация. Общие положения стандартизации
Стандартизация. Общие положения стандартизации «Поспорили однажды корень, стебель, лист – кто из них важнее?»
«Поспорили однажды корень, стебель, лист – кто из них важнее?» В море коварном товаров и цен. Бизнес-корабль ведёт…
В море коварном товаров и цен. Бизнес-корабль ведёт… ИНФОРМАЦИЯ. ИНФОРМАТИКА.ИНФОРМАТИЗАЦИЯ.
ИНФОРМАЦИЯ. ИНФОРМАТИКА.ИНФОРМАТИЗАЦИЯ. Служу Отечеству
Служу Отечеству Продукты для «1С:Предприятия»
Продукты для «1С:Предприятия» Dadaisms mērķis. Veidot izpratni par modernisma virzienu dadaismu
Dadaisms mērķis. Veidot izpratni par modernisma virzienu dadaismu Урок -путешествие
Урок -путешествие Прогнозирование и анализ временных рядов
Прогнозирование и анализ временных рядов هدف از معامله کردن در بازار فارکس
هدف از معامله کردن در بازار فارکس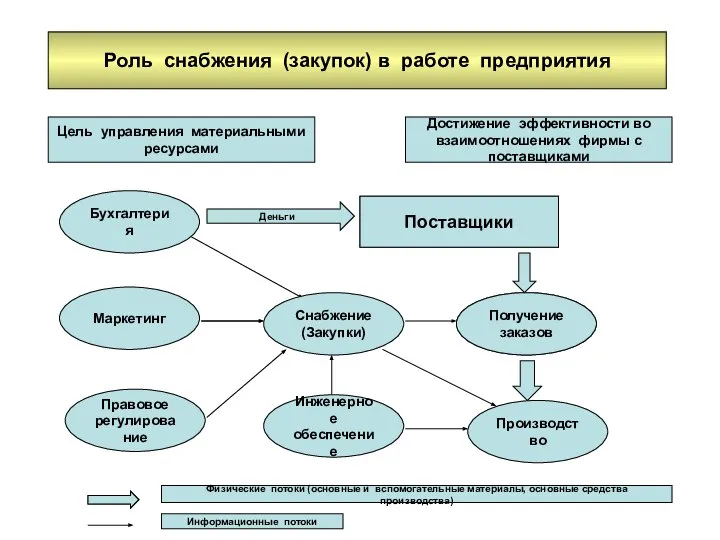 Роль снабжения, закупок в работе предприятия
Роль снабжения, закупок в работе предприятия Правописание о – е после шипящих и ц в окончаниях существительных 5 класс
Правописание о – е после шипящих и ц в окончаниях существительных 5 класс