Содержание
- 2. Металлические свойства усиливаются (восстановительные свойства- отдача электронов) ПОЧЕМУ? Cs +3Li) ) 2 1 +4Be) ) 2
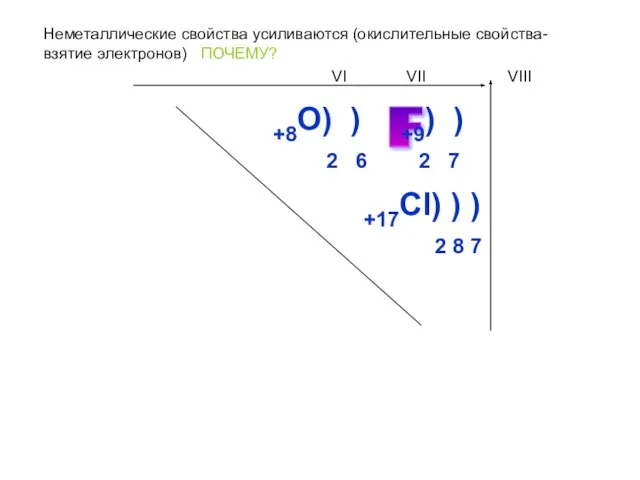
- 3. Неметаллические свойства усиливаются (окислительные свойства- взятие электронов) ПОЧЕМУ? F +8О) ) 2 6 +9) ) 2
- 4. Неметаллические свойства усиливаются, кислотные свойства соединений тоже Na2O MgO Al2O3 SiO2 P2O5 SO3 Cl2O7 основные амфотерный
- 5. Работа с учебником стр.5 1.Положение в ПСХЭ. 2.Строение атома +12 Mg) ) ) 2 8 2
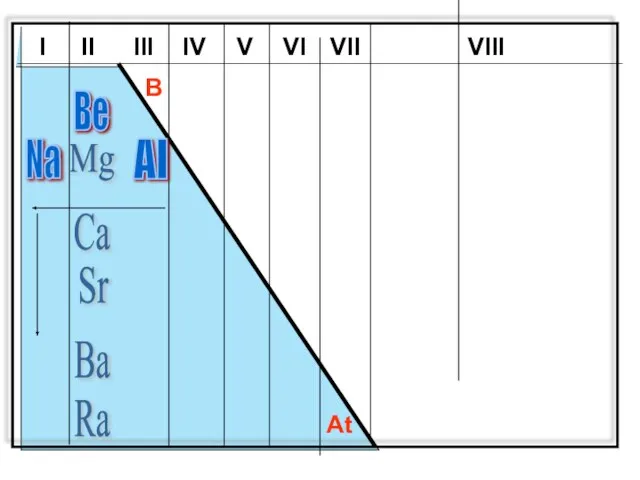
- 6. I II III IV V VI VII VIII B At Mg Ca Sr Ra Ba Na
- 7. 5. Сравнение с соседями по подгруппе: Магний обладает восстановительными cвойствами и : Ca >Mg > Be
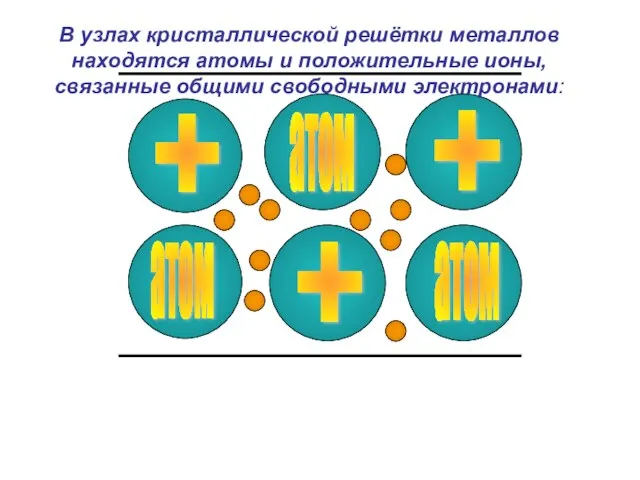
- 8. + В узлах кристаллической решётки металлов находятся атомы и положительные ионы, связанные общими свободными электронами:
- 9. 7. Оксид магния является основным оксидом MgO видео 8. Гидроксид магния является основанием Mg(OН)2 Напишите уравнения
- 10. Работа с учебником стр.5 1.Положение в ПСХЭ. 2.Строение атома +16 S) ) ) 2 8 6
- 11. 5. Сравнение с соседями по подгруппе: по окислительным свойствам : Cl >S >P 6.Как простое вещество
- 12. 7. Оксид cеры(IV) является кислотным оксидом SO2 и получается при горении серы, Высший оксид SO3 получают
- 14. Скачать презентацию








 Shape
Shape Мой кумир - Джессика Альба
Мой кумир - Джессика Альба ЦО № 429 – ресурсный центр инновационной сети «Обучение по индивидуальным учебным планам в старшей школе»
ЦО № 429 – ресурсный центр инновационной сети «Обучение по индивидуальным учебным планам в старшей школе» О РАЗРАБОТКЕ МУНИЦИПАЛЬНЫХ ПРОГРАММ В ОБЛАСТИ ЭНЕРГОСБЕРЕЖЕНИЯ
О РАЗРАБОТКЕ МУНИЦИПАЛЬНЫХ ПРОГРАММ В ОБЛАСТИ ЭНЕРГОСБЕРЕЖЕНИЯ Изображение и реальность
Изображение и реальность Управление качеством в процессе закупок
Управление качеством в процессе закупок С 01 октября 2020 года денежные средства будут перечисляться банками только на карту Мир гражданам, получающим пособия
С 01 октября 2020 года денежные средства будут перечисляться банками только на карту Мир гражданам, получающим пособия Щи - национальное русское блюдо
Щи - национальное русское блюдо Век Просвещения
Век Просвещения Musical Britain
Musical Britain Проект по дизайну в сфере применения
Проект по дизайну в сфере применения «Последнее слово» Ильи Петрова. - презентация
«Последнее слово» Ильи Петрова. - презентация Формирование и развитие материально-технической базы АПК Украины
Формирование и развитие материально-технической базы АПК Украины Роль фольклора в процессе формирования духовно-нравственных качеств дошкольников
Роль фольклора в процессе формирования духовно-нравственных качеств дошкольников Конкурентные стратегииприложение к журналу «ЭТАП: Экономическая Теория, Анализ, Практика»
Конкурентные стратегииприложение к журналу «ЭТАП: Экономическая Теория, Анализ, Практика» ИНСТРУКЦИИ ПО ТЕХНИКЕ БЕЗОПАСНОСТИ НА УРОКАХ ТЕХНОЛОГИИ 5 и 6 классов
ИНСТРУКЦИИ ПО ТЕХНИКЕ БЕЗОПАСНОСТИ НА УРОКАХ ТЕХНОЛОГИИ 5 и 6 классов Презентация на тему Игры на развитие интеллектуальных способностей детей дошкольного возраста посредством ИКТ
Презентация на тему Игры на развитие интеллектуальных способностей детей дошкольного возраста посредством ИКТ The United Nations General Assembly
The United Nations General Assembly  ГРАФИЧЕСКИЕ ИНФОРМАЦИОННЫЕ МОДЕЛИ МОДЕЛИРОВАНИЕ И ФОРМАЛИЗАЦИЯ
ГРАФИЧЕСКИЕ ИНФОРМАЦИОННЫЕ МОДЕЛИ МОДЕЛИРОВАНИЕ И ФОРМАЛИЗАЦИЯ «Секреты выбора кредитных продуктов украинских банков»
«Секреты выбора кредитных продуктов украинских банков» Методика проведения международных маркетинговых исследований Дисциплина: Международный маркетинг Преподаватель: профессор ка
Методика проведения международных маркетинговых исследований Дисциплина: Международный маркетинг Преподаватель: профессор ка Повторение
Повторение Ранний период Христианской философии
Ранний период Христианской философии Бельмондо (фотографии)
Бельмондо (фотографии) Маркетинговое исследование пакетированных соков в городе Новороссийск
Маркетинговое исследование пакетированных соков в городе Новороссийск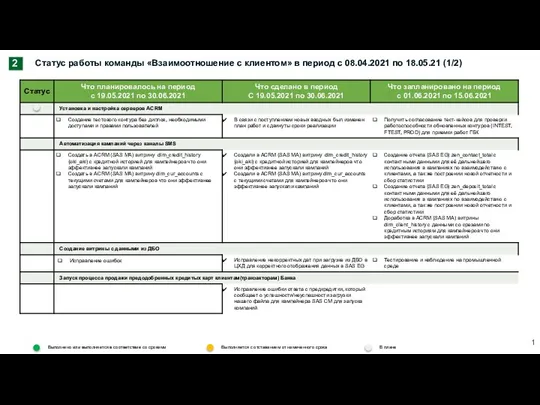 Статус работы команды Взаимоотношение с клиентом в период с 08.04.2021 по 18.05.21
Статус работы команды Взаимоотношение с клиентом в период с 08.04.2021 по 18.05.21 Электронная и цифровая техника в СЦБ
Электронная и цифровая техника в СЦБ Дистрибьюция фармпрепаратов в Украине. Тенденции развития
Дистрибьюция фармпрепаратов в Украине. Тенденции развития