Содержание
- 2. ФИЗИЧЕСКАЯ ХИМИЯ ХИМИЧЕСКАЯ КИНЕТИКА Лекция 1 2017 г
- 3. Химическая кинетика Химическая кинетика наряду с термоди-намикой и строением вещества составляет теоретический фундамент современной химии. Она
- 4. Предмет и основные понятия Химическая кинетика – это учение о скорости и механизме процесса и его
- 5. Формальная кинетика Направление химической кинетики, позволившее разработать методику расчета скорости химических реакций и динамику изменения концентрации
- 6. Типы химических реакций Простые реакции является совокупностью однотипных элементарных химических актов, представляющих собой превращение реагентов в
- 7. Типы химических реакций Химические реакции в своем большинстве являются сложными, т. е., включают несколько элементарных (простых)
- 8. Энергия активации процесса Необходимым условием протекания любой химической реакции является реакционная способность реагентов, т. е. наличие
- 9. Cостояние реагирующей системы Различают статические химические реакции, протекающие в закрытых системах, неспособных обмениваться массой с окружающей
- 10. Открытые системы Системы, в которых имеет место материальный обмен с окружающей средой, называются открытыми системами. Большинство
- 11. Типы химических реакций Химические реакции, протекающие в гомогенных системах (в их объеме), называются гомогенными, т.е. осуществляются
- 12. Кинетика гомогенных химических реакций Формальная кинетика В кинетике скорость химической реакции представляется как функция концентрации реагентов
- 13. Скорость химических реакций
- 14. Реакционное пространство R
- 15. Глубина протекания реакции
- 16. В закрытых системах изменение количества вещества с течением времени происходит только за счет протекания в них
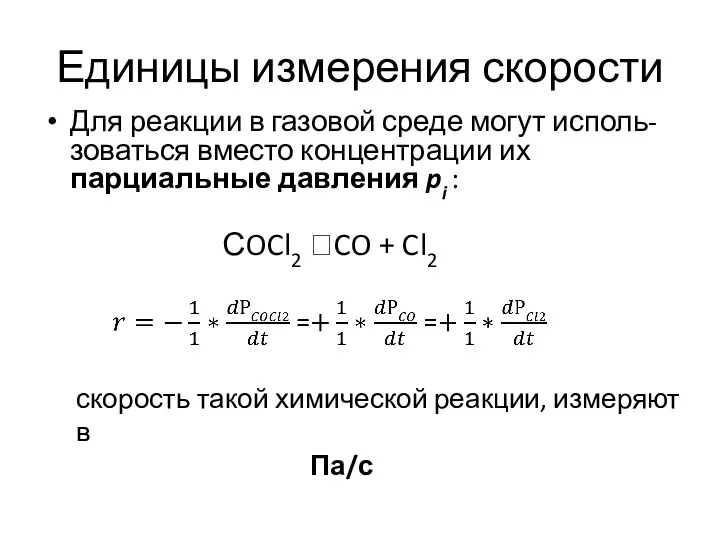
- 17. Единицы измерения скорости Для реакции в газовой среде могут исполь-зоваться вместо концентрации их парциальные давления pi
- 18. Кинетическое уравнение химических реакций Кинетическое уравнение это зависимость скорости реакции от концентрации реагентов. Для простых реакций
- 19. Закон действующих масс Величина k численно равна скорости реакции при концентрациях всех реагентов, равных единице. Она
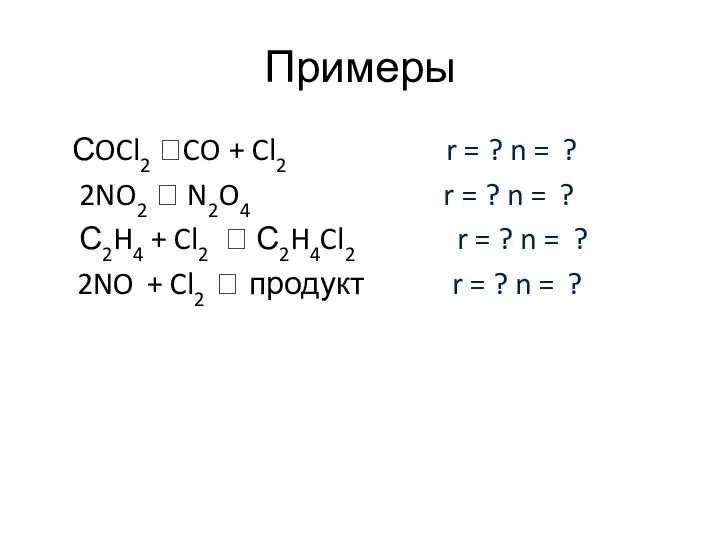
- 20. Примеры СOCl2 ?CO + Cl2 r = ? n = ? 2NO2 ? N2O4 r =
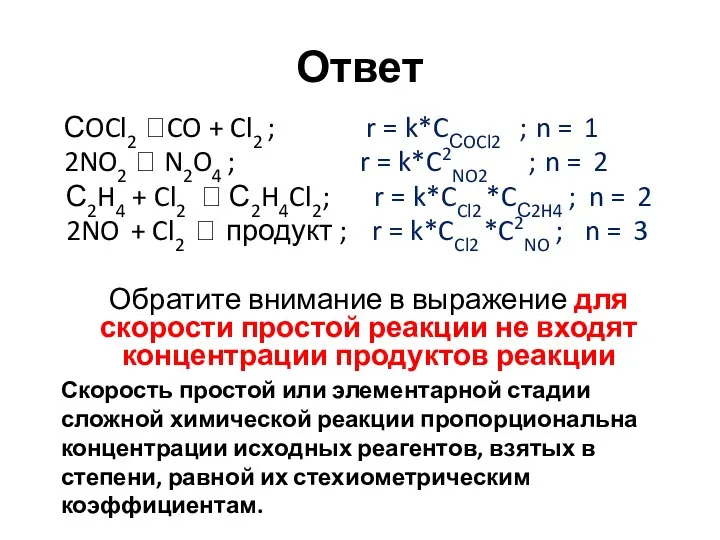
- 21. Ответ СOCl2 ?CO + Cl2 ; r = k*CСOCl2 ; n = 1 2NO2 ? N2O4
- 22. Пример
- 23. Молекулярность и порядок В кинетике химические реакции разделяют по признаку молекулярности реакции и по признаку порядка
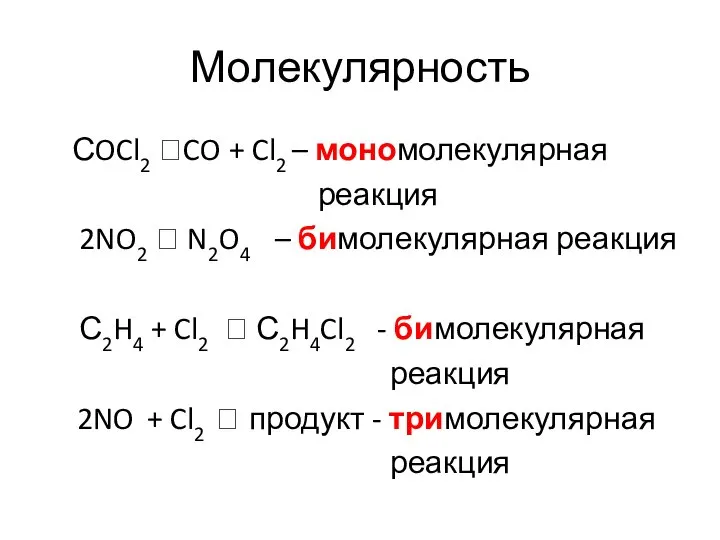
- 24. Молекулярность СOCl2 ?CO + Cl2 – мономолекулярная реакция 2NO2 ? N2O4 – бимолекулярная реакция С2H4 +
- 25. Порядок реакции Порядок ni реакции по компоненту – это показатель степени при концентрации i-го реагентов в
- 26. Примеры СOCl2 ?CO + Cl2 ; n = 1 (реакция 1 порядка) 2NO2 ? N2O4 ;
- 27. Критерии простой реакции Стехиометрическое уравнение реакции описывает реальной механизм химической реакции. Молекулярность простой реакции совпадает с
- 28. Пример вопроса на экзамене Понятие простой и сложной реакции. Для некоторой реакции А + В ?C
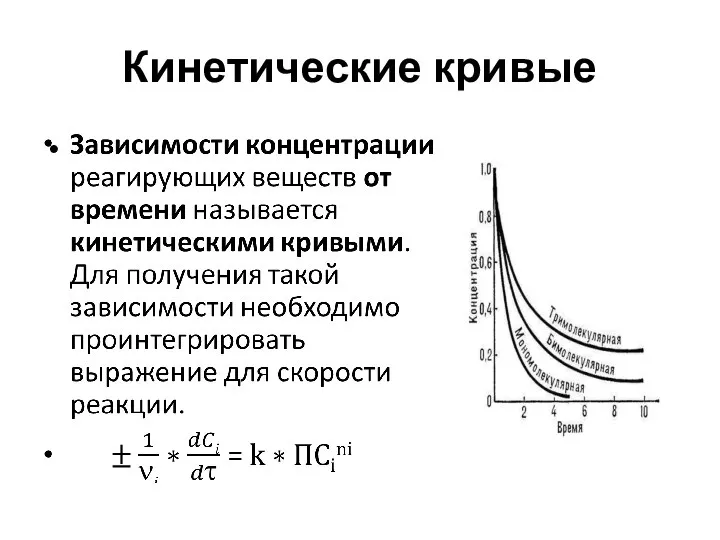
- 29. Кинетические кривые
- 30. Формальная кинетика простых реакций Лекция 2 2018
- 31. Реакция «0» порядка (y =ax + b) tgα = a tgα = -k
- 32. Время полупревращения Для характеристики скорости реакции наряду с константой скорости часто пользуются временем, или периодом полупревращения
- 33. Реакция 1 порядка N2O5 ? 2NO2 + 1/2O2
- 36. Вывод интегрального уравнения
- 38. Размерность константы скорости
- 40. Задание
- 42. Скачать презентацию




























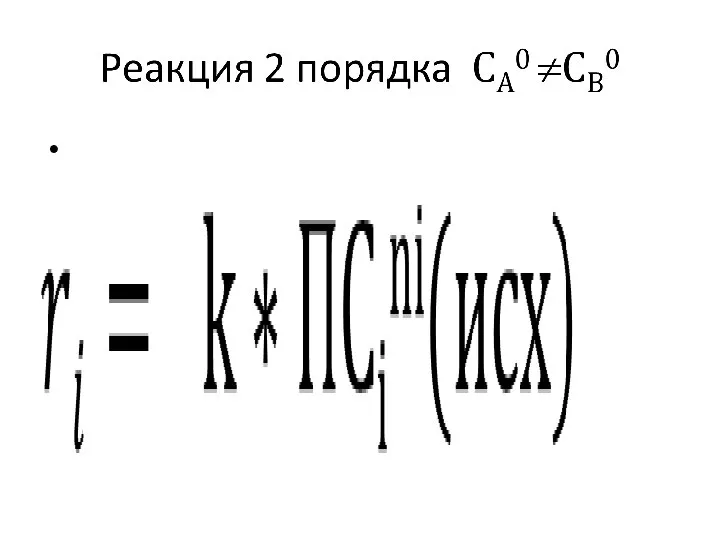



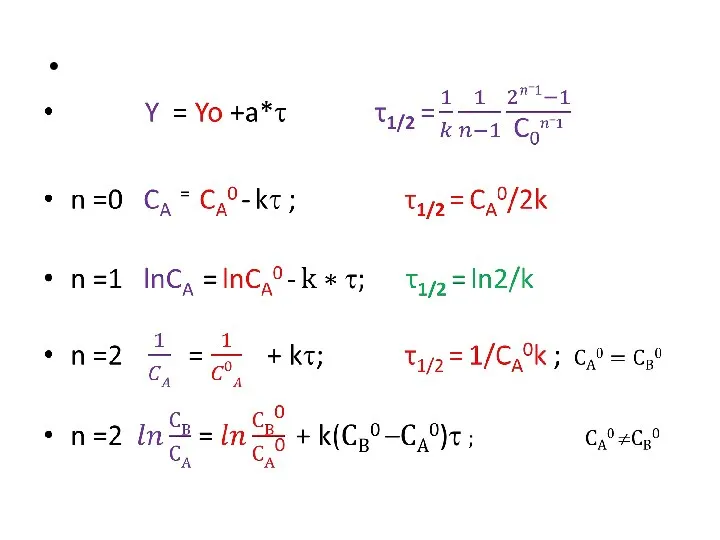

 Измерение объёма тела
Измерение объёма тела Оборудование для ремонта бытовых электроприборов
Оборудование для ремонта бытовых электроприборов Применение первого начала термодинамики к изопроцессам
Применение первого начала термодинамики к изопроцессам Устройство, работа, возможные неисправности системы охлаждения двигателя КамАЗ -740. ТО системы охлаждения
Устройство, работа, возможные неисправности системы охлаждения двигателя КамАЗ -740. ТО системы охлаждения Лазерно-индуцированное формирование наночастиц из ультратонких пленок металлов
Лазерно-индуцированное формирование наночастиц из ультратонких пленок металлов Работа в термодинамике
Работа в термодинамике Физика в игрушках
Физика в игрушках Расчет пути и времени движения
Расчет пути и времени движения Приспособления малой механизации
Приспособления малой механизации Свободное падение 10-9
Свободное падение 10-9 Плавление и кристаллизация
Плавление и кристаллизация Бобрышев Анатолий Васильевич учитель физики Школа №30, г. Старый Оскол
Бобрышев Анатолий Васильевич учитель физики Школа №30, г. Старый Оскол Распространение электромагнитного излучения в молекулярной атмосфере
Распространение электромагнитного излучения в молекулярной атмосфере Термодинамика
Термодинамика Экспериментальные данные и вероятность событий
Экспериментальные данные и вероятность событий Механика. Теория механизмов и машин. Общие понятия. Структурный анализ по Л. В. Ассура
Механика. Теория механизмов и машин. Общие понятия. Структурный анализ по Л. В. Ассура Мощность реактора. Задача
Мощность реактора. Задача Напряжение в точке включения реактора. Распределение напряжения по линии. Задача
Напряжение в точке включения реактора. Распределение напряжения по линии. Задача Электромагниты и их пременения
Электромагниты и их пременения Решение задач. Сила Ампера
Решение задач. Сила Ампера Изучение магнитных явлений
Изучение магнитных явлений Силы упругости. Закон Гука
Силы упругости. Закон Гука Трубки газоразрядные
Трубки газоразрядные Последовательное и параллельное соединение проводников в электрической цепи. Закон Ома для полной цепи
Последовательное и параллельное соединение проводников в электрической цепи. Закон Ома для полной цепи Презентация на тему Шкала электромагнитных волн
Презентация на тему Шкала электромагнитных волн  Магнитные свойства вещества
Магнитные свойства вещества موج طرح
موج طرح Внешний фотоэффект. Изучение законов внешнего фотоэффекта
Внешний фотоэффект. Изучение законов внешнего фотоэффекта