Слайд 2Яковлева Т.Ю.
Молекулярная физика
Химия есть правая рука физики, математика – глаза.

М.В. Ломоносов
Слайд 3Яковлева Т.Ю.
Закон сохранения массы
Русский учёный Михаил Васильевич Ломоносов (1711-65) в 1748 г.

создал при Петербургской Академии наук первую в России химическую лабораторию. Тогда же он впервые сформулировал, а в 1756 г. экспериментально подтвердил на примере обжигания металлов в запаянных сосудах закон сохранения массы (веса):
Общая масса (вес) веществ, вступивших в химическую реакцию, равна общей массе (весу) веществ, образующихся в результате реакции.
Слайд 4Яковлева Т.Ю.
Русский учёный
Михаил Васильевич Ломонóсов
(19.11.1711–15.04.1765)

Слайд 5Яковлева Т.Ю.
Закон сохранения массы
В 1789 г. (через 41 год после Ломоносова) более

строгий вариант закона сохранения массы был установлен французским химиком Антуаном Лораном Лавуазье (1743-94), который показал, что при химических реакциях сохраняется не только общая масса веществ, но и масса каждого из элементов, входящих в состав взаимодействующих веществ.
Слайд 6Яковлева Т.Ю.
Французский химик
Антуан Лоран Лавуазьé
(Antoine-Laurent Lavoisier)
(26.08.1743–8.05.1794)

Слайд 7Яковлева Т.Ю.
Связь массы и энергии
В 1905 г. немецкий физик Альберт Эйнштейн (Albert

Einstein, 1879-1955) показал, что между массой тела (m) и его энергией (E) существует связь, выражаемая уравнением Эйнштейна:
где c0 – скорость света в вакууме (3·108 м/с).
Слайд 8Яковлева Т.Ю.
Немецкий (американский) физик
Альберт Эйнштéйн (Albert Einstein)
(14.03.1879–18.04.1955)

Слайд 9Яковлева Т.Ю.
Размеры и массы
атомов и молекул
Размер молекулы настолько мал, что представить

его можно только с помощью сравнений.
Например, молекула воды во столько раз меньше крупного яблока, во сколько раз яблоко меньше земного шара.
Линейные размеры простых атомов и молекул составляют около 10-10 м.
Масса атома водорода составляет 1,674ׁׂ·10-27 кг, кислорода — 2,667 · 10-26 кг, углерода — 1,993 · 10-26 кг.
Слайд 10Яковлева Т.Ю.
Атомная единица массы вещества
Атомная масса измеряется в атомных единицах массы.
Атомная

единица массы (а.е.м.) или дáльтон (Да) – единица массы, равная 1/12 массы изотопа углерода 12C (нуклида углерода с атомной массой 12), что в единицах системы СИ составляет (1,6605655 ± 0,0000086)∙10–27 кг (на 1980 год).
mед = 1 а.е.м. = (масса 12C) /12 ≈ 1,66∙10–27 кг
Слайд 11Яковлева Т.Ю.
Относительная молекулярная (атомная) масса вещества
Относительная молекулярная (или атомная) масса вещества —

отношение массы молекулы (или атома) данного вещества к 1/12 массы атома углерода 12С (1 а.е.м.)
Mr = m0 / ( m0С /12)
Mr = m0 / 1 а.е.м.
где m0 – масса молекулы (или атома) данного вещества,
m0C – масса атома углерода.
Относительная молекулярная (атомная) масса выражается в атомных единицах массы.
Слайд 12Яковлева Т.Ю.
Опыты, позволившие открыть закон Авогадро. Закон объёмных отношений.
Измеряя объёмы газов,

вступающих в реакцию и образующихся в результате реакции, французский физик Жозеф Луи Гей-Люссáк (1778-1850) 31 декабря 1808 г. пришёл к установлению закона простых объёмных отношений («химическому» закона Гей-Люссака):
Объёмы вступающих в реакцию газов относятся друг к другу и к объёмам образующихся газообразных продуктов реакции как небольшие целые числа.
Слайд 13Яковлева Т.Ю.
Французский физик
Жозеф Луи Гей-Люссáк
(Joseph Louis Gay-Lussac)
(6.12.1778-9.05.1850)

Слайд 14Яковлева Т.Ю.
Закон Авогадро
В равных объёмах различных газов при одинаковых условиях (одинаковых

температурах и давлениях) содержится одинаковое число молекул.
Слайд 15Яковлева Т.Ю.
Итальянский физик и химик
Амедео Авогáдро (Amedeo Avogadro)
(9.08.1776-9.07.1856)
Закон Авогадро открыт А.Авогадро

в 1811 году, однако только с 1860 года стал широко применяться в физике и химии.
Слайд 16Яковлева Т.Ю.
Моль
Слово «моль» придумал в начале 20 века немецкий физико-химик лауреат Нобелевской

премии Вильгельм Оствальд (1853–1932); оно содержит тот же корень, что и слово «молекула» и происходит от латинского moles – громада, масса с уменьшительным суффиксом.
Моль – единица количества вещества ν в системе СИ.
Моль – это количество вещества системы, содержащей столько же структурных элементов, сколько содержится атомов в 0,012 кг изотопа углерода 1 2 C.
При применении моля структурные элементы должны быть специфицированы и могут быть атомами, молекулами, ионами, электронами и другими частицами или специфицированными группами частиц. Другими словами, в 1 моле содержится столько молекул (атомов, ионов и каких-либо других структурных элементов вещества), сколько атомов содержится в 0,012 кг изотопа углерода 1 2 C.
Раньше молем или грамм-молекулой называли количество вещества, численно равное относительной молекулярной массе, но выраженное в граммах.
Слайд 17Яковлева Т.Ю.
Постоянная Авогадро
Число молекул (число структурных единиц) в одном моле любого вещества

называется постоянной Авогадро
NА= 6,0221367·1023 (моль-1).
Постоянная Авогадро настолько велика, что с трудом поддается воображению.
Например, если футбольный мяч увеличить в NА раз по объему, то в нем поместится земной шар. Если же в NА раз увеличить диаметр мяча, то в нем поместится самая большая галактика, содержащая сотни миллиардов звезд!
Если вылить стакан воды в море и подождать, пока эта вода равномерно распределится по всем морям и океанам, до самого их дна, то, зачерпнув в любом месте Земного шара стакан воды, в него обязательно попадет несколько десятков молекул воды, которые были когда-то в стакане.
Слайд 18Яковлева Т.Ю.
Молярная масса
Массу одного моля вещества (количество вещества ν = 1 моль)

называют молярной массой и обозначают μ или М:
Молярная масса — величина, равная отношению
массы вещества m к количеству вещества ν.
M = m / ν.
В общем случае молярная масса вещества, выраженная в г/моль, численно равна относительной атомной или относительной молекулярной массе этого вещества:
M = Mr (г/моль), M = Mr∙10 - 3 (кг/моль),
M = m0∙NA = Mr∙mе д∙NA ,
m0 - масса одной молекулы или атома.
Слайд 19Яковлева Т.Ю.
Количество вещества
ν = N/NA = m/M
ν — количество вещества, [ν] =

моль,
N - общее число молекул,
NA - число Авогадро, NA = 6,02·102 3 (1/моль),
m — общая масса вещества,
M — молярная масса, [M] = кг/моль,
Слайд 20Яковлева Т.Ю.
Следствие из закона Авогадро
При одинаковых условиях равные количества различных газов

занимают равные объёмы.
В частности, при нормальных условиях (н. у.)
[температуре Т0 = 273,15 K = 0 °С и
давлении р0 = 1,01325 · 105 Па =1 атм = 760 мм. рт. ст.]
1 моль любого газа (близкого по свойствам к идеальному газу), занимает один и тот же объём VM = 22,4 л.
Эта физическая постоянная VM называется молярный (мольный) объём газа при нормальных условиях. Точное значение молярного объёма газа 22.4135 ± 0.0006 л/моль.
Слайд 21Яковлева Т.Ю.
Следствие из закона Авогадро
Плотности ρ2 и ρ1 двух идеальных газов при

одних и тех же давлении и температуре прямо пропорциональны их молярным массам M2 и M1 :
ρ2 / ρ1 = M2 / M1
или
Молярная масса первого газа равна произведению молярной массы второго газа на относительную плотность первого газа по второму:
M1 = M2(ρ1/ρ2)
Слайд 22Яковлева Т.Ю.
Следствие из закона Авогадро
Третье следствие закона Авогадро относится к реакциям с

участием газов, его часто называют законом объемных отношений:
Объемы реагирующих и образующихся в результате реакции газов, если они измерены при одинаковых условиях, относятся так же, как и коэффициенты в уравнении реакции.
Например, для реакции горения метана СН4 + 2О2 = СО2 + 2Н2О
на основании этого закона можно утверждать, что с одним объемом метана прореагирует два объема кислорода, в результате получится один объем углекислого газа, если все объемы измерены при одинаковых условиях.
Слайд 24Яковлева Т.Ю.
Вопросы
- Каковы порядковые величины диаметра и массы молекул?
- Что называют

относительной молекулярной массой?
- Что называют количеством вещества?
- Какова единица количества вещества? Дайте определение этой единицы.
- Что такое молярная масса вещества?
- Что называют постоянной Авогадро?
- Чему равна постоянная Авогадро?























 Физическая природа изображений
Физическая природа изображений Весы циферблатные
Весы циферблатные Презентация на тему Приливы, отливы, их использование
Презентация на тему Приливы, отливы, их использование  Постоянный электрический ток и его характеристики
Постоянный электрический ток и его характеристики 671210
671210 Общие сведения о системах первичного электроснабжения РЭС
Общие сведения о системах первичного электроснабжения РЭС Молекулярная физика
Молекулярная физика ВКР: Разработка технологии ремонта форсунок дизельных двигателей автомобилей
ВКР: Разработка технологии ремонта форсунок дизельных двигателей автомобилей Ядерные реакции под действием нейтронов. (Тема 2.6)
Ядерные реакции под действием нейтронов. (Тема 2.6) Применение ядерной энергии в различных отраслях. Доза радиоактивного излучения
Применение ядерной энергии в различных отраслях. Доза радиоактивного излучения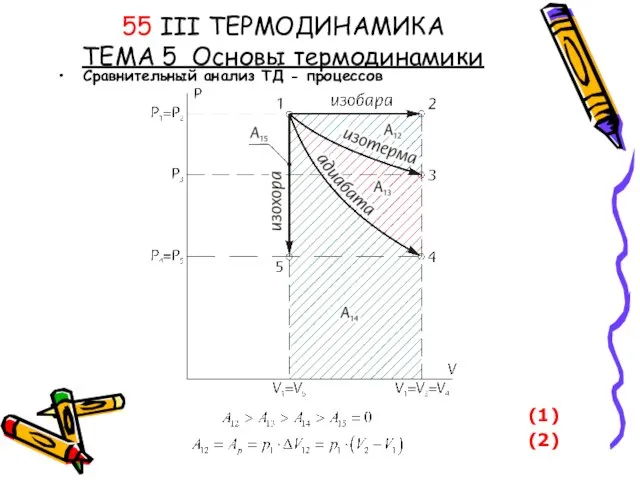 55 III ТЕРМОДИНАМИКА ТЕМА 5 Основы термодинамики Сравнительный анализ ТД - процессов
55 III ТЕРМОДИНАМИКА ТЕМА 5 Основы термодинамики Сравнительный анализ ТД - процессов Вес тела. Единицы веса
Вес тела. Единицы веса Презентация на тему: основы термодинамики
Презентация на тему: основы термодинамики Разработка привода руля направления транспортного самолета
Разработка привода руля направления транспортного самолета Тепловое движение_Температура
Тепловое движение_Температура Основное уравнение статики атмосферы. Барометрические формулы (лекция № 16,17)
Основное уравнение статики атмосферы. Барометрические формулы (лекция № 16,17) Характеры линейных групп
Характеры линейных групп Анализ видов и кинематических параметров движений
Анализ видов и кинематических параметров движений Амперметр. Измерение силы тока
Амперметр. Измерение силы тока Механическое движение. Масса тела. Плотность вещества
Механическое движение. Масса тела. Плотность вещества Механическая работа. Единицы работы
Механическая работа. Единицы работы Нагрузки на балку. Расчет
Нагрузки на балку. Расчет Презентация-повторение курса физики 8 класса
Презентация-повторение курса физики 8 класса Пневматика
Пневматика Механика: кинематика
Механика: кинематика Геометрическая оптика. Часть С. Подготовка к ЕГЭ
Геометрическая оптика. Часть С. Подготовка к ЕГЭ Примеры некорректных задач. Уравнения математической физики. Режимы с обострением
Примеры некорректных задач. Уравнения математической физики. Режимы с обострением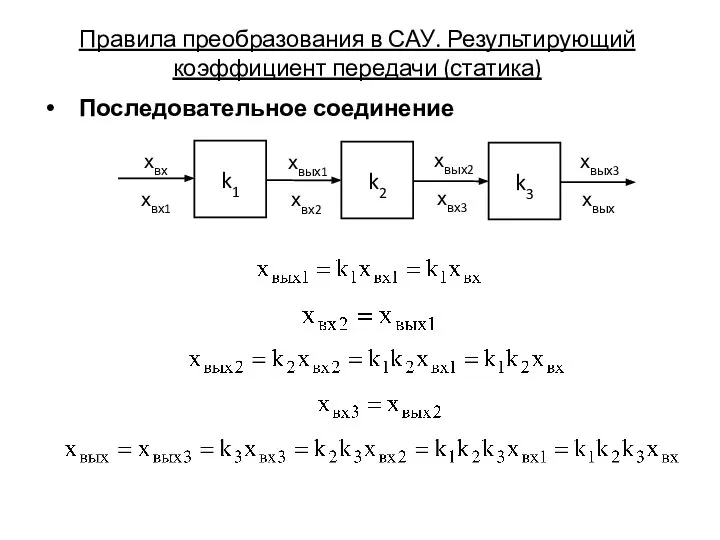 Правила преобразования в САУ. Результирующий коэффициент передачи (статика)
Правила преобразования в САУ. Результирующий коэффициент передачи (статика)