Содержание
- 2. НУЛЕВОЕ НАЧАЛО ТЕРМОДИНАМИКИ Нулевое начало термодинамики сформулированное всего около 50 лет назад , по существу представляет
- 3. Первое закон термодинамики Первый закон термодинамика – это закон сохранения энергии, распространенный на тепловые явления. Он
- 4. Невозможность создания вечного двигателя Задолго до открытия закона сохранения энергии Французская Академия наук приняла в 1775г.
- 5. Применение I закона к изопроцессам 1) T=const – изотермический δT=0 Q=A’ δU=0 2) P=const – изобарный
- 6. Второй закон термодинамики Второй закон термодинамики указывает направление возможных энергетических превращений и тем самым выражает необратимость
- 7. И Людвиг Больцман выдвинул спасительную теорию, что Вселенную необходимо рассматривать в целом, поскольку процессы, происходящие в
- 8. Второй закон термодинамики постулирует существование функции состояния , называемой «энтропией» ( что означает от греческого «эволюция»
- 9. Третий закон термодинамики Открытие третьего начала термодинамики связано с нахождением химического средства - величины , характеризующих
- 11. Скачать презентацию
Слайд 2НУЛЕВОЕ НАЧАЛО ТЕРМОДИНАМИКИ
Нулевое начало термодинамики сформулированное всего около 50 лет
НУЛЕВОЕ НАЧАЛО ТЕРМОДИНАМИКИ
Нулевое начало термодинамики сформулированное всего около 50 лет

Слайд 3 Первое закон термодинамики
Первый закон термодинамика – это закон сохранения
Первое закон термодинамики
Первый закон термодинамика – это закон сохранения

Часто вместо работы А внешних тел над системой рассматривают работу А` системы над внешними телами. Учитываю, что А`= -А, первый закон термодинамики в в форме δU = A+Q можно переписать так: Q=δU+A`
Суть первого закона в утверждении: изменение так определенной энергии не зависит от процесса и определяется только начальным и конечным состояниями системы. Это означает, что внутренняя энергия – однозначная функция состояние системы и в замкнутой системе сохраняется.
Слайд 4Невозможность создания вечного двигателя
Задолго до открытия закона сохранения энергии Французская Академия наук
Невозможность создания вечного двигателя
Задолго до открытия закона сохранения энергии Французская Академия наук

Под вечным двигателем первого рода понимают устройство, которое могло бы совершать неограниченное количество работы без затраты топлива или каких-либо других материалов.
Вечные двигатели обычно конструируют на основе использования следующих приёмов или их комбинаций:
1) Подъем воды с помощью архимедова винта;
2) Подъем воды с помощью капилляров;
3) Использование колеса с неуравновешивающимися грузами;
4) Природные магниты;
5) Электромагнетизм;
6) Пар или сжатый воздух.
Слайд 5Применение I закона к изопроцессам
1) T=const – изотермический
δT=0
Q=A’
δU=0
2)
Применение I закона к изопроцессам
1) T=const – изотермический
δT=0
Q=A’
δU=0
2)
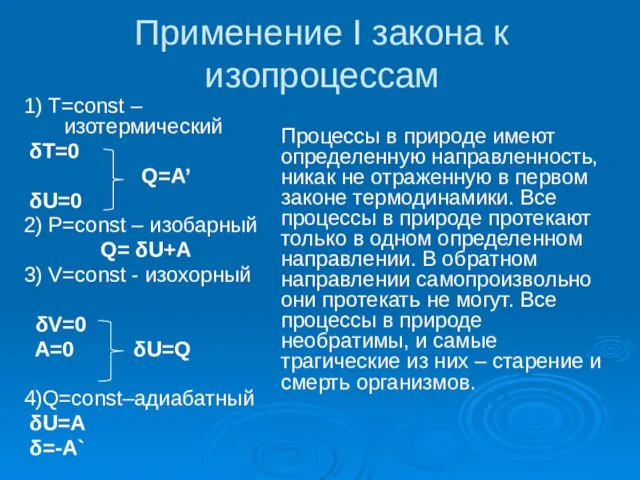
Q= δU+A
3) V=const - изохорный
δV=0
A=0 δU=Q
4)Q=const–адиабатный
δU=A
δ=-A`
Процессы в природе имеют определенную направленность, никак не отраженную в первом законе термодинамики. Все процессы в природе протекают только в одном определенном направлении. В обратном направлении самопроизвольно они протекать не могут. Все процессы в природе необратимы, и самые трагические из них – старение и смерть организмов.
Слайд 6Второй закон термодинамики
Второй закон термодинамики указывает направление возможных энергетических превращений и тем
Второй закон термодинамики
Второй закон термодинамики указывает направление возможных энергетических превращений и тем

Немецкий ученный Р. Клаузиус сформулировал этот закон так: невозможно перевести тепло от более холодной системы к более горячей при отсутствии одновременных изменений в обеих системах или окружающих телах.
Другая формулировка принадлежит английскому ученому У. Кельвину: невозможно осуществить такой периодический процесс, единственным результатом которого было бы получение работы за счет теплоты, взятой от одного источника.
Согласно 2 началу все процессы природы идут в оду сторону, к увеличению беспорядка, уменьшению энергии, а при “полном беспорядке” – напишет Клаузиус – наступит всеобщая смерть – всякое движение прекратится. Это грустный прогноз вызвал бурю возражений.
Слайд 7И Людвиг Больцман выдвинул спасительную теорию, что Вселенную необходимо рассматривать в целом,

Слайд 8Второй закон термодинамики постулирует существование функции состояния , называемой «энтропией» ( что
Второй закон термодинамики постулирует существование функции состояния , называемой «энтропией» ( что

1) Энтропия системы является экстенсивным свойством . Если система состоит из нескольких частей , то полная энтропия системы равна сумме энтропии каждой части .
Изменение энтропии S состоит из двух частей . Обозначим через δS поток энтропии, обусловленный взаимодействием с окружающей средой , а через δS - часть энтропии , обусловленную изменениями внутри системы , имеем δS = δS1 + δS2
Приращение энтропии δS обусловленное изменением внутри системы, никогда не имеет отрицательное значение . Величина δS = 0 , только тогда , когда система претерпевает обратимые изменения , но она всегда положительна , если в системе идут такие же необратимые процессы.
Таким образом:
δS = 0 ( обратимые процессы );
δS > 0( необратимые процессы );
Для изолированной системы поток энтропии равен нулю и выражения обратимого процесса и необратимого процесса сводятся к следующему виду : δS1 = δS > 0 ( изолированная система ).
Слайд 9Третий закон термодинамики
Открытие третьего начала термодинамики связано с нахождением химического средства -
Третий закон термодинамики
Открытие третьего начала термодинамики связано с нахождением химического средства -

 Биомеханика. Кинематика. Относительность движения
Биомеханика. Кинематика. Относительность движения Постоянный электрический ток и его характеристики
Постоянный электрический ток и его характеристики Ядерный реактор
Ядерный реактор Презентация на тему Солнце и другие звезды
Презентация на тему Солнце и другие звезды  Презентация на тему Термометр
Презентация на тему Термометр  Уравнение неразрывности. Лекция 5
Уравнение неразрывности. Лекция 5 Молекулярно-кинетический подход применительно к расчету тепловой нагрузки при пленочном кипении
Молекулярно-кинетический подход применительно к расчету тепловой нагрузки при пленочном кипении Презентация на тему Электрическое поле (8 класс)
Презентация на тему Электрическое поле (8 класс)  Расчет производительности экструдеров
Расчет производительности экструдеров Как уменьшить силу трения
Как уменьшить силу трения Электрическая цепь и её составная часть
Электрическая цепь и её составная часть Тепловое движение
Тепловое движение Презентация к уроку _Инерциальные системы отсчета
Презентация к уроку _Инерциальные системы отсчета Видимое и ультрафиолетовое излучение
Видимое и ультрафиолетовое излучение рух по колу
рух по колу Автор: Тараканова Светлана школа № 14, 8 А класс
Автор: Тараканова Светлана школа № 14, 8 А класс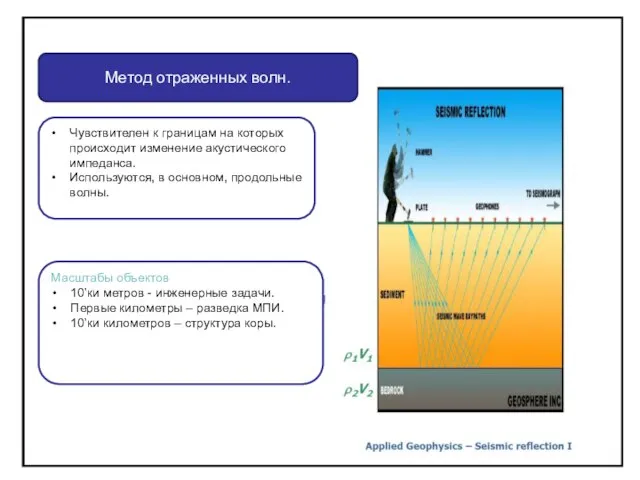 Закон Снеллиуса (отражения) для монотипных волн
Закон Снеллиуса (отражения) для монотипных волн Электромагнитная совместимость в электроэнергетике
Электромагнитная совместимость в электроэнергетике Наглядное пособие для изучения шпоночного и штифтового соединений
Наглядное пособие для изучения шпоночного и штифтового соединений Электрический ток. Задачи
Электрический ток. Задачи Электрический ток в различных средах
Электрический ток в различных средах Явление электромагнитной индукции (эми). 11 класс
Явление электромагнитной индукции (эми). 11 класс Солнечная лаборатория
Солнечная лаборатория Результаты измерений. Лабораторная работа №3 по биофизике
Результаты измерений. Лабораторная работа №3 по биофизике Сила
Сила Изменение агрегатных состояний
Изменение агрегатных состояний Основы медицинской и биологической физики. Лекция 4. Часть 1
Основы медицинской и биологической физики. Лекция 4. Часть 1 Динамика фотоионизации атомов благородных газов между первым и вторым порогом ионизации
Динамика фотоионизации атомов благородных газов между первым и вторым порогом ионизации