Содержание
- 2. 1. Все вещества состоят из молекул между которыми имеются промежутки. Молекулой называют наименьшую частицу вещества, способную
- 3. прямые фотографии отдельных больших молекул органических соединений определение параметров молекул просачивание масла через стенки стального цилиндра
- 4. 2. Молекулы любого вещества непрерывно и хаотически движутся. ПОДТВЕРЖДЕНИЯ: -броуновское движение (1827 г.) - диффузия(зависит от
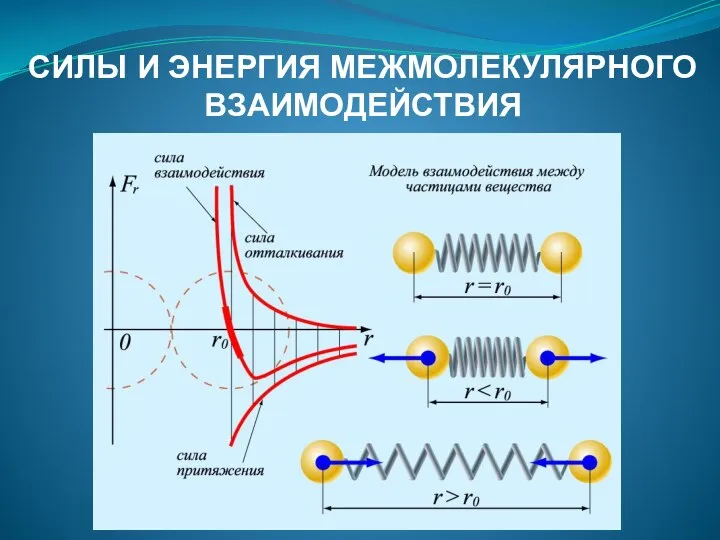
- 5. 3. На небольших расстояниях между молекулами действуют силы притяжения и силы отталкивания, природа этих сил электромагнитная.
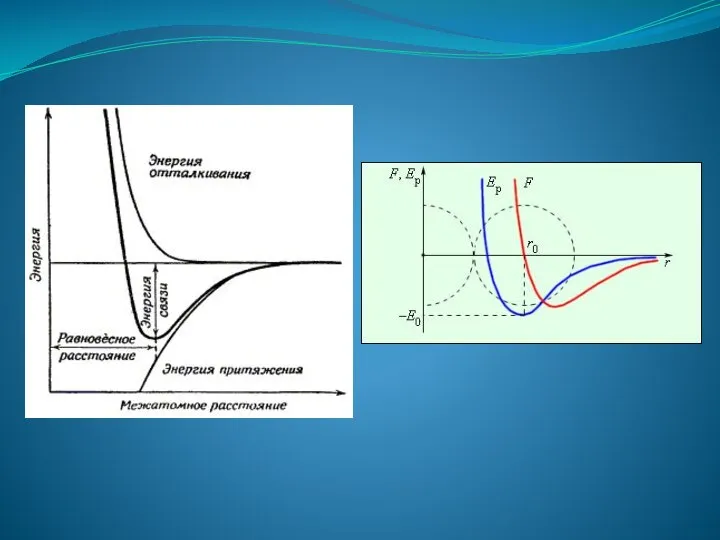
- 7. СИЛЫ И ЭНЕРГИЯ МЕЖМОЛЕКУЛЯРНОГО ВЗАИМОДЕЙСТВИЯ
- 9. АГРЕГАТНЫЕ СОСТОЯНИЯ ВЕЩЕСТВА условия: газообразное - Ек >> Епmin жидкое - Ек ~ Епmin твердое -
- 10. Главную роль в поведении газа играет хаотическое движение его молекул: -между двумя последовательными столкновениями молекулы газа
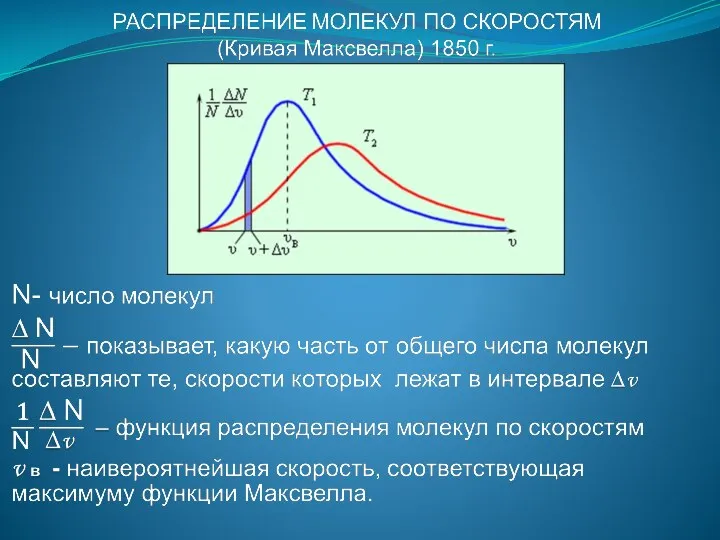
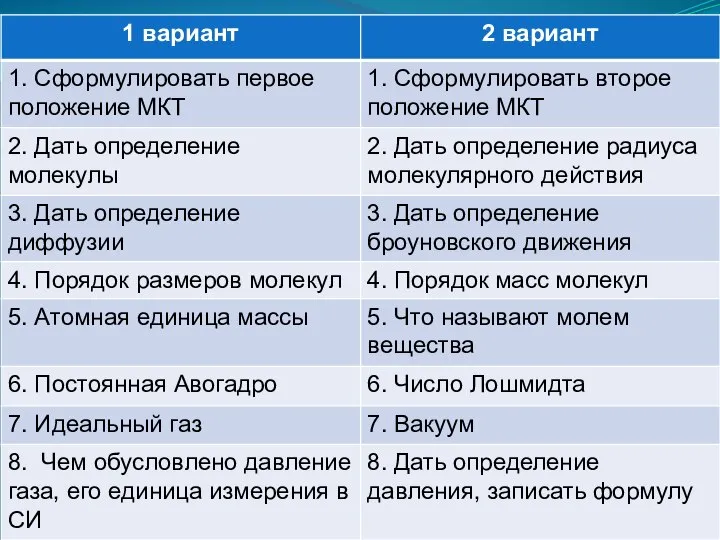
- 11. ЗАНЯТИЕ № 14 СКОРОСТИ ДВИЖЕНИЯ МОЛЕКУЛ И ИХ ИЗМЕРЕНИЕ. МАССА И РАЗМЕРЫ МОЛЕКУЛ И АТОМОВ. ИДЕАЛЬНЫЙ
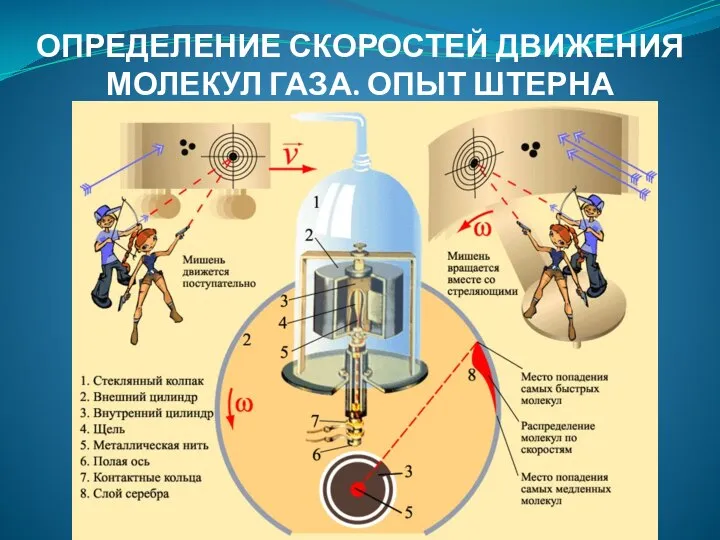
- 12. ОПРЕДЕЛЕНИЕ СКОРОСТЕЙ ДВИЖЕНИЯ МОЛЕКУЛ ГАЗА. ОПЫТ ШТЕРНА
- 15. МАССА И РАЗМЕРЫ МОЛЕКУЛ Многие опыты показывают, что размер молекулы очень мал. Линейный размер молекулы или
- 16. Линейные размеры простых атомов и молекул составляют около 10-10 м. Молекула воды во столько раз меньше
- 18. Массу молекулы можно вычислить путём сложения масс элементов, которые входят в состав молекулы. Например, масса молекулы
- 23. Длина свободного пробега – это расстояние, которое проходит молекула между двумя последовательными столкновениями (при нормальных условиях
- 25. Внесистемные единицы давления: мм.рт.ст., мм.водн.ст., бар, физическая атмосфера, техническая атмосфера. 1аmм = 1,013 х 105 Па
- 26. ПРИБОРЫ ДЛЯ ИЗМЕРЕНИЯ ДАВЛЕНИЯ (манометры, барометры) Наиболее распространены жидкостные (ртутные) барометры . В ртутном барометре атмосферное
- 27. Ртутные барометры: а – чашечный; б – сифонный; в – сифонно-чашечный
- 28. В анероиде атмосферное давление измеряется по величине деформации упругой металлической коробки, из которой откачан воздух; при
- 29. Гипсотермометр – прибор для определения атмосферного давления по температуре кипения воды, зависящей от давления (с понижением
- 30. Как известно, кипение жидкости наступает, когда упругость образующегося в ней пара достигает величины внешнего давления. Когда
- 31. ИДЕАЛЬНЫЙ ГАЗ Идеальным называется газ, молекулы которого принимают за материальные точки, обладающие абсолютной упругостью и невзаимодействующие
- 32. ВАКУУМ О пространстве, в котором давление меньше атмосферного, говорят, что в нем создан вакуум. Под высоким
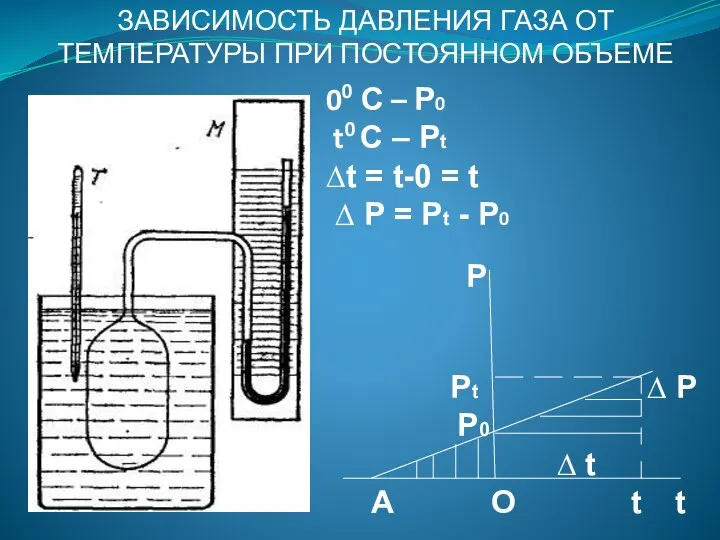
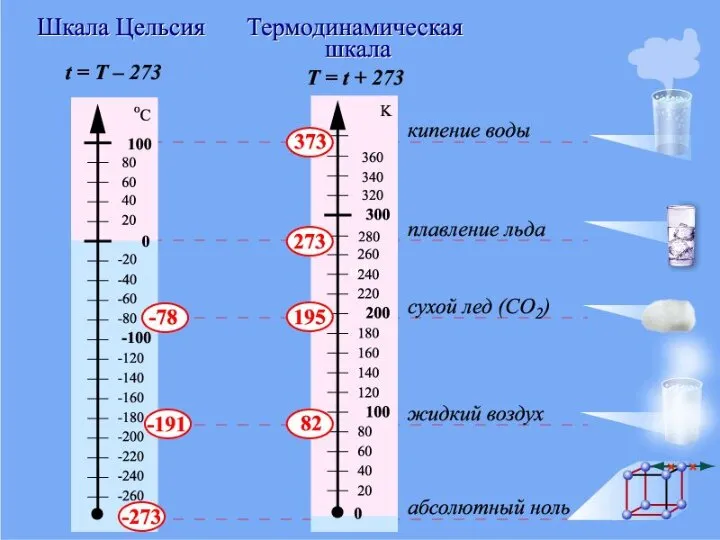
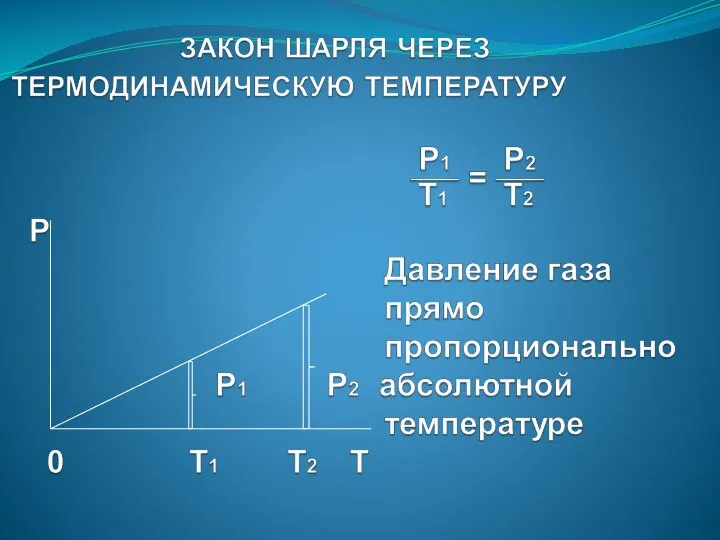
- 34. ЗАНЯТИЕ № 15 ТЕМПЕРАТУРА И ЕЕ ИЗМЕРЕНИЕ. АБСОЛЮТНЫЙ НУЛЬ ТЕМПЕРАТУРЫ. ТЕРМОДИНАМИЧЕСКАЯ ШКАЛА ТЕМПЕРАТУРЫ. СВЯЗЬ МЕЖДУ ДАВЛЕНИЕМ
- 36. 00 С – Р0 t0 C – Рt ∆t = t-0 = t ∆ Р =
- 37. Р0
- 40. 0-11
- 44. 1. Перевести в Кельвины: 10 0С, 27 0С, -10 0С, 0 0С, -273 0С 2. Выразить
- 45. 4. Как изменится давление газа, если при постоянной температуре и объеме число молекул увеличить в два
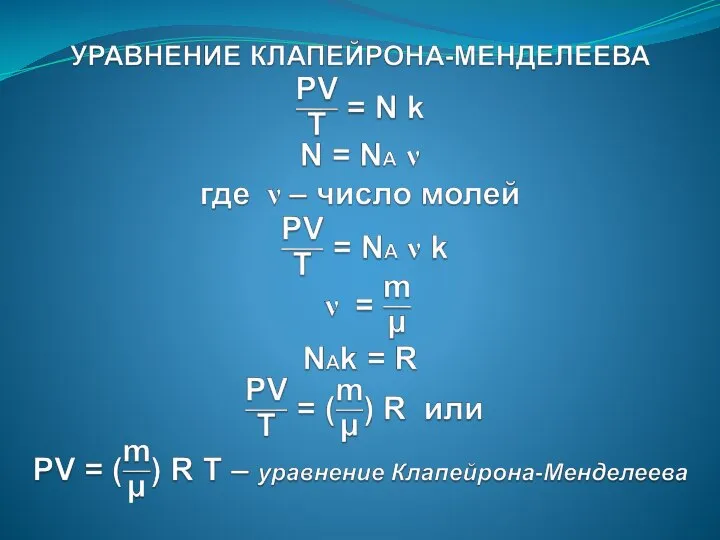
- 46. ЗАНЯТИЕ № 16 УРАВНЕНИЕ СОСТОЯНИЯ ИДЕАЛЬНОГО ГАЗА. МОЛЯРНАЯ ГАЗОВАЯ ПОСТОЯННАЯ. ГАЗОВЫЕ ЗАКОНЫ
- 54. ЗАНЯТИЕ № 18 ВНУТРЕННЯЯ ЭНЕРГИЯ ГАЗА. РАБОТА И ТЕПЛОТА КАК ФОРМА ПЕРЕДАЧИ ЭНЕРГИИ. ТЕПЛОЕМКОСТЬ. УДЕЛЬНАЯ ТЕПЛОЕМКОСТЬ.
- 55. Термодинамика – это наука о тепловых явлениях. В противоположность молекулярно-кинетической теории, которая делает выводы на основе
- 56. Одним из важнейших понятий термодинамики является внутренняя энергия тела. Все макроскопические тела обладают энергией, заключенной внутри
- 57. ВНУТРЕННЯЯ ЭНЕРГИЯ ИДЕАЛЬНОГО ГАЗА Внутренняя энергия идеального газа равна сумме кинетических энергий всех частиц газа, находящихся
- 58. Число степеней свободы — это число независимых переменных, полностью определяющих положение молекулы как системы атомов в
- 61. ИЗМЕНЕНИЕ ВНУТРЕННЕЙ ЭНЕРГИИ ТЕЛ Существуют способы изменения внутренней энергии тела: совершение работы и теплопередача. При совершении
- 62. Нагревание тел может происходить и при ударах, сгибании или разгибании, при деформации. Внутренняя энергия тела возрастает.
- 63. Внутренняя энергия не постоянная величина. Она может изменяться. Если повысить температуру тела, то его внутренняя энергия
- 64. Мерой изменения внутренней энергии тела является количество теплоты. Q = ΔU ΔU =cmΔT, или Q =
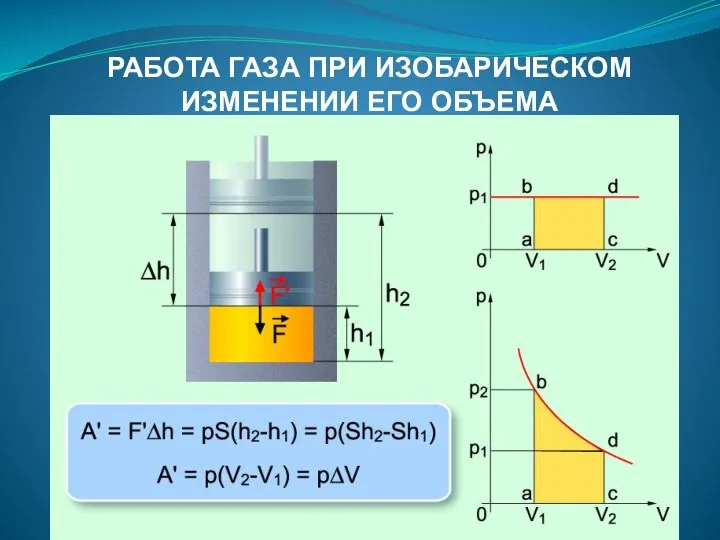
- 67. РАБОТА ГАЗА ПРИ ИЗОБАРИЧЕСКОМ ИЗМЕНЕНИИ ЕГО ОБЪЕМА
- 69. ЗАНЯТИЕ № 19 ПЕРВЫЙ ЗАКОН ТЕРМОДИНАМИКИ. АДИАБАТНЫЙ ПРОЦЕСС. ВТОРОЕ НАЧАЛО ТЕРМОДИНАМИКИ. ПРИНЦИП ДЕЙСТВИЯ ТЕПЛОВОЙ МАШИНЫ. ТЕПЛОВЫЕ
- 70. ПЕРВОЕ НАЧАЛО ТЕРМОДИНАМИКИ Подведенное к системе количество теплоты частично идет на увеличение внутренней энергии системы, а
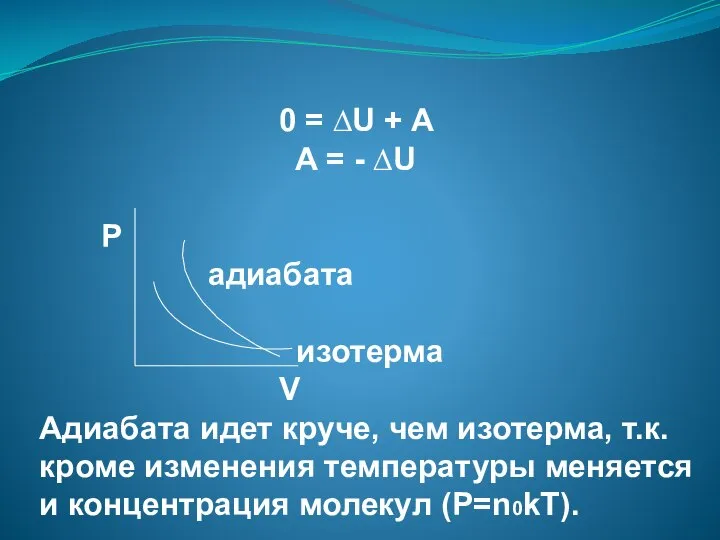
- 72. 0 = ∆U + A A = - ∆U Р адиабата изотерма V Адиабата идет круче,
- 73. ВТОРОЕ НАЧАЛО ТЕРМОДИНАМИКИ 1. Кельвин: Не возможны такие процессы, единственным конечным результатом которых явилось бы отнятие
- 74. ТЕПЛОВЫЕ МАШИНЫ Из первого начала термодинамики вытекает невозможность создания вечного двигателя т.е. устройства, способного совершать неограниченное
- 75. Если после изменений состояния тело приходит снова в свое первоначальное состояние, то это изменение состояния называют
- 76. В используемых на практике двигателях совершивший работу газ или пар выпускают из двигателя и следующий рабочий
- 77. В двигателях внутреннего сгорания повышение температуры происходит в результате сгорания топлива внутри двигателя и нагревателем являются
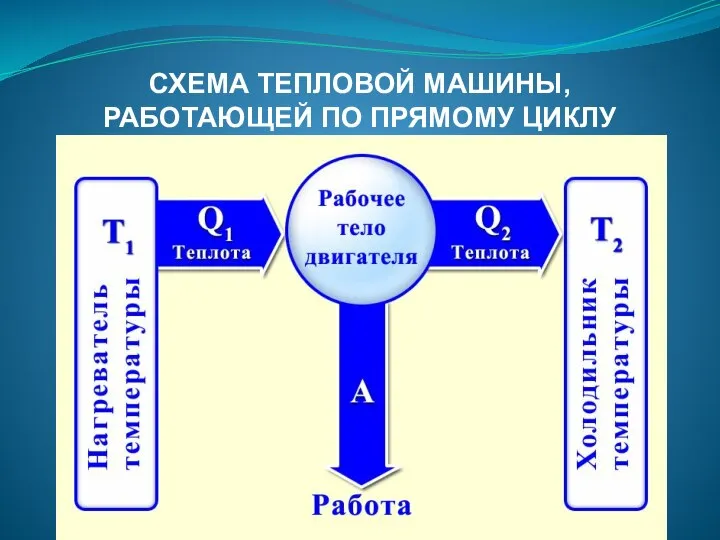
- 78. СХЕМА ТЕПЛОВОЙ МАШИНЫ, РАБОТАЮЩЕЙ ПО ПРЯМОМУ ЦИКЛУ
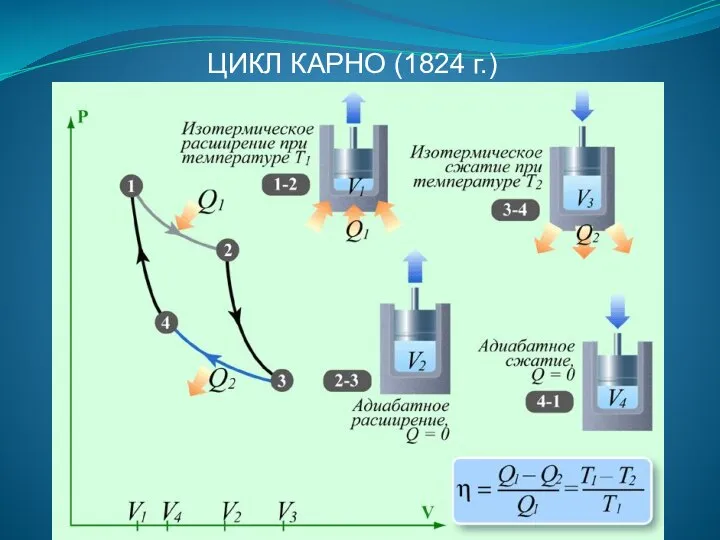
- 80. ЦИКЛ КАРНО (1824 г.)
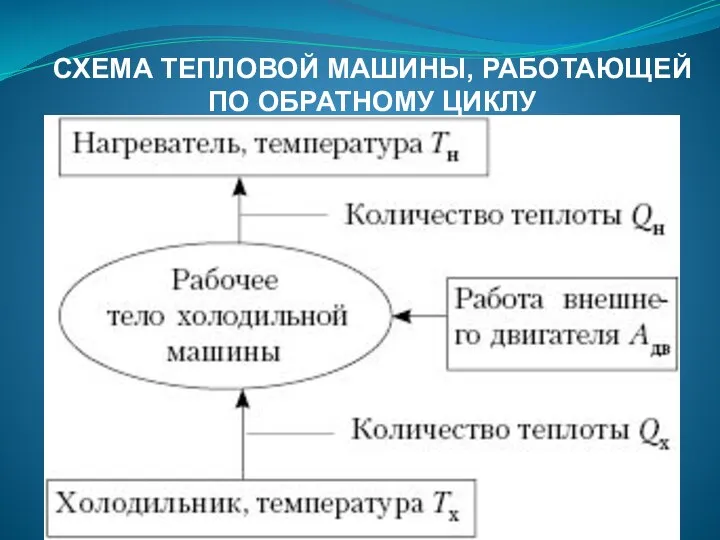
- 82. СХЕМА ТЕПЛОВОЙ МАШИНЫ, РАБОТАЮЩЕЙ ПО ОБРАТНОМУ ЦИКЛУ
- 83. 1. Нагреется или охладится воздух в комнате, если вы забыли закрыть дверцу холодильника. 2. Газ совершает
- 84. ЗАНЯТИЕ № 20 ИСПАРЕНИЕ И КОНДЕНСАЦИЯ. НАСЫЩЕННЫЕ И НЕНАСЫЩЕННЫЕ ПАРЫ. АБСОЛЮТНАЯ И ОТНОСИТЕЛЬНАЯ ВЛАЖНОСТЬ ВОЗДУХА. ТОЧКА
- 85. ИСПАРЕНИЕ И КОНДЕНСАЦИЯ Переход вещества из жидкого состояния в газообразное называется парообразованием, а переход вещества из
- 86. На поверхности жидкости всегда происходит два процесса: испарение и конденсация, если преобладает испарение – жидкость охлаждается,
- 88. ПАРЫ НАСЫЩАЮЩИЕ И НЕНАСЫЩАЮЩИЕ ПРОСТРАНСТВО И ИХ СВОЙСТВА Пар, находящийся в состоянии подвижного равновесия со своей
- 89. 1. Изохорический процесс При изохорическом процессе давление насыщенного пара зависит от его рода и быстро растет
- 90. 2. Изотермический процесс При постоянной температуре давление насыщенного пар не зависит от объема (так как меняется
- 93. Если воздух охладится до t3 = 60С , ρн3 = 0,0073 кг/м3 , то из каждого
- 94. 1. Чем объясняется, что вечером после жаркого дня в низменной местности наблюдается образование тумана? 2. Когда
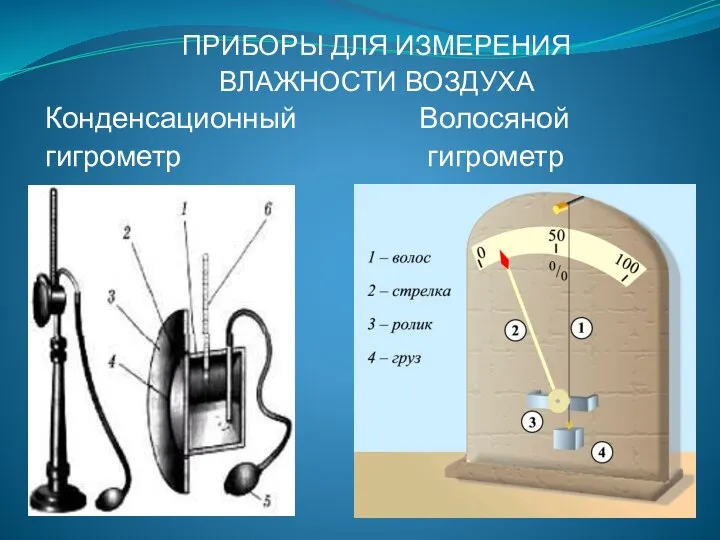
- 95. ПРИБОРЫ ДЛЯ ИЗМЕРЕНИЯ ВЛАЖНОСТИ ВОЗДУХА Конденсационный Волосяной гигрометр гигрометр
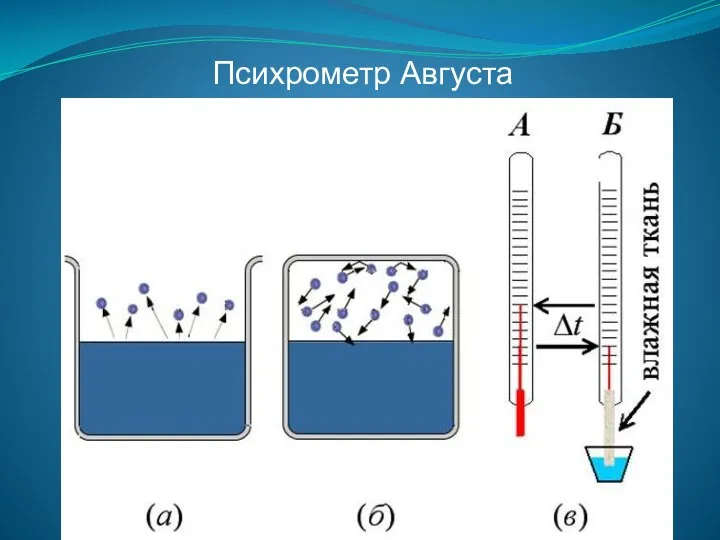
- 96. Психрометр Августа
- 97. ЗАНЯТИЕ № 22 ХАРАКТЕРИСТИКА ЖИДКОГО СОСТОЯНИЯ ВЕЩЕСТВА. ПОВЕРХНОСТНЫЙ СЛОЙ ЖИДКОСТИ. ЭНЕРГИЯ ПОВЕРХНОСТНОГО СЛОЯ. ЯВЛЕНИЯ НА ГРАНИЦЕ
- 98. ХАРАКТЕРИСТИКА ЖИДКОГО СОСТОЯНИЯ Вещество в жидком состоянии сохраняет свой объем и принимает форму сосуда, в который
- 99. -наблюдается ближний порядок в расположении молекул или атомов (упорядочение в небольшом объеме). Жидкости проявляют свойства
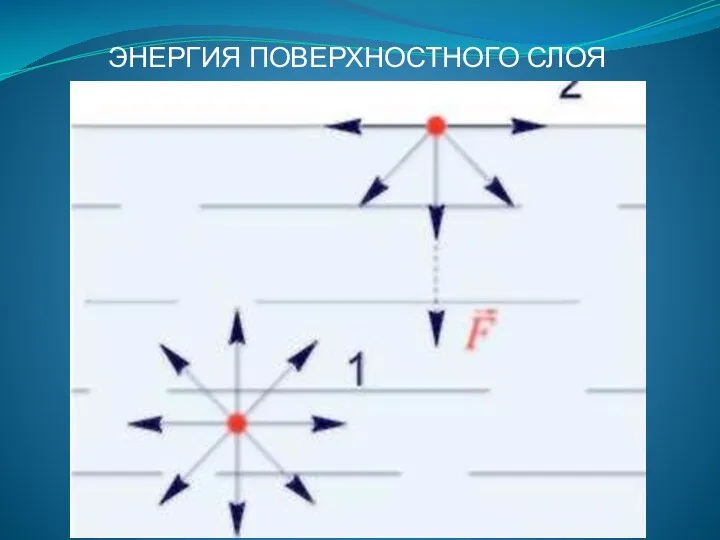
- 100. ЭНЕРГИЯ ПОВЕРХНОСТНОГО СЛОЯ
- 101. Равнодействующая сил, действующих на молекулы, находящиеся внутри жидкости равна нулю. На молекулы поверхностного слоя действует равнодействующая
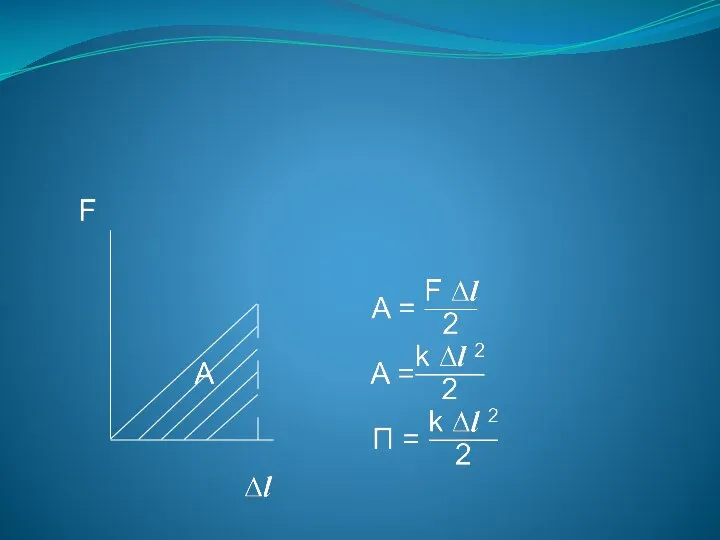
- 102. КОЭФФИЦИЕНТ ПОВЕРХНОСТНОГО НАТЯЖЕНИЯ За счет свободной энергии может быть произведена работа, связанная с уменьшением свободной поверхности
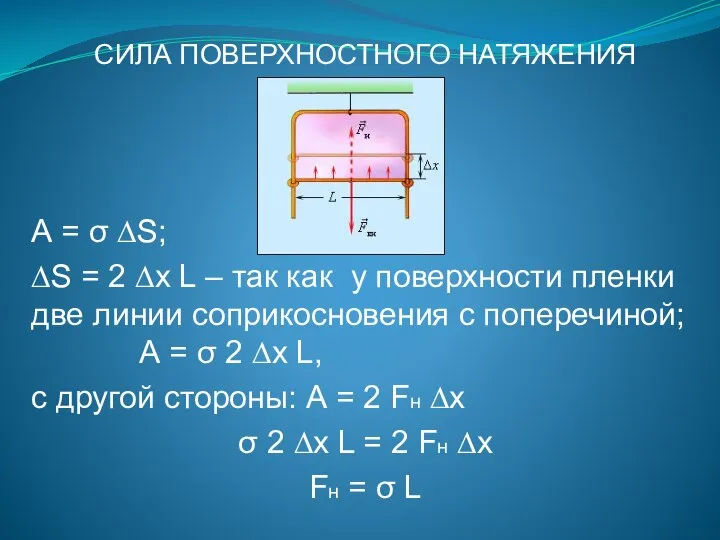
- 104. СИЛА ПОВЕРХНОСТНОГО НАТЯЖЕНИЯ А = σ ∆S; ∆S = 2 ∆х L – так как у
- 106. Возникновение сил поверхностного натяжения является результатом действия молекулярных сил. Свойства сил поверхностного натяжения: 1. Действуют вдоль
- 107. 1. Домашний эксперимент: на поверхность воды положите две спички и куском мыла коснитесь воды между спичками.
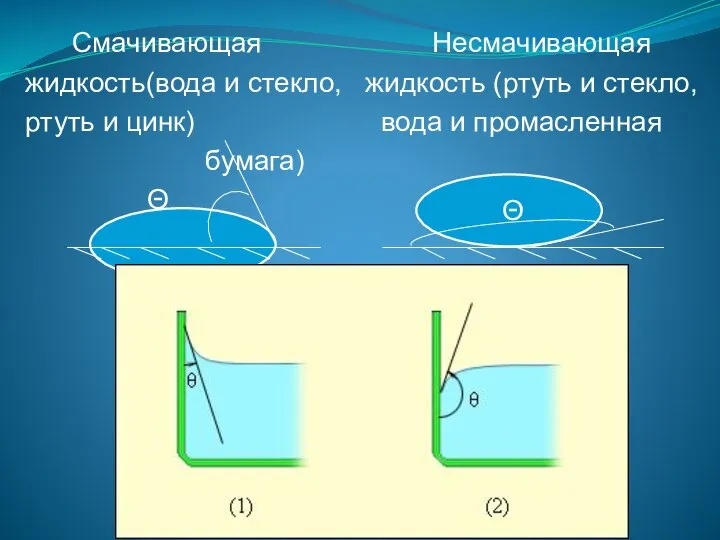
- 108. Смачивающая Несмачивающая жидкость(вода и стекло, жидкость (ртуть и стекло, ртуть и цинк) вода и промасленная бумага)
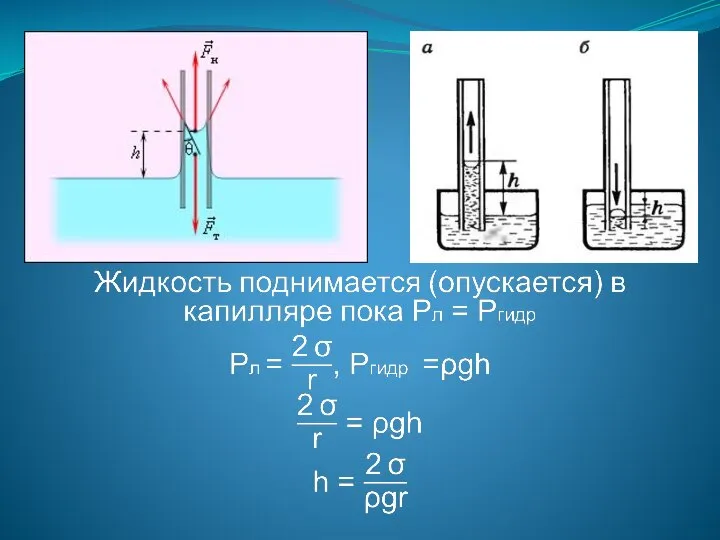
- 109. Θ – краевой угол составлен касательной к поверхности жидкости и поверхностью твердого тела, внутри которого заключена
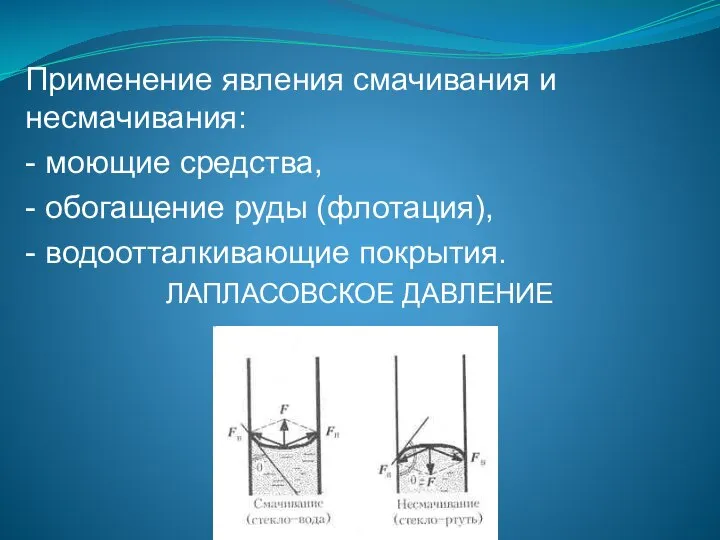
- 110. Применение явления смачивания и несмачивания: - моющие средства, - обогащение руды (флотация), - водоотталкивающие покрытия. ЛАПЛАСОВСКОЕ
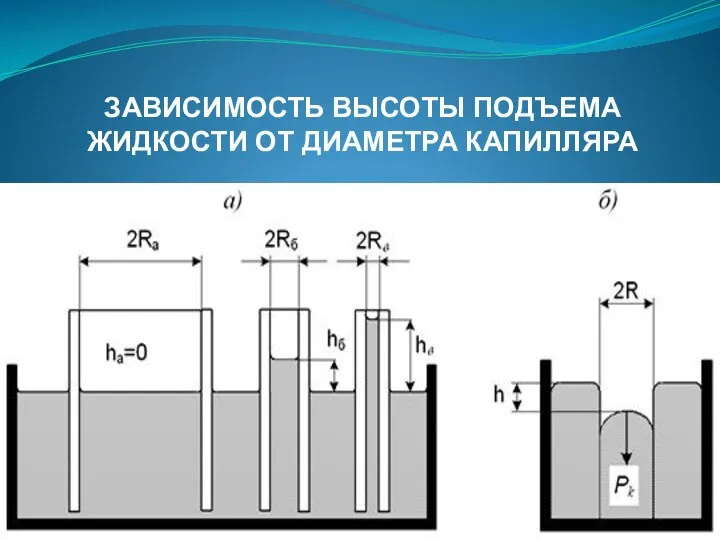
- 113. ЗАВИСИМОСТЬ ВЫСОТЫ ПОДЪЕМА ЖИДКОСТИ ОТ ДИАМЕТРА КАПИЛЛЯРА
- 114. ПРИМЕНЕНИЕ КАПИЛЛЯРНОСТИ В ТЕХНИКЕ, БЫТУ, ПРИРОДЕ - сушка пористых тел, - промакательная бумага, - перья плакатные,
- 115. В США для повышения продуктивности полупустынных пастбищ измельчают кусты и разбрасывают по пастбищу. Они впитывают дождевую
- 116. ЗАНЯТИЕ № 25 КИПЕНИЕ. ЗАВИСИМОСТЬ ТЕМПЕРАТУРЫ КИПЕНИЯ ОТ ДАВЛЕНИЯ. ПЕРЕГРЕТЫЙ ПАР И ЕГО ИСПОЛЬЗОВАНИЕ В ТЕХНИКЕ.
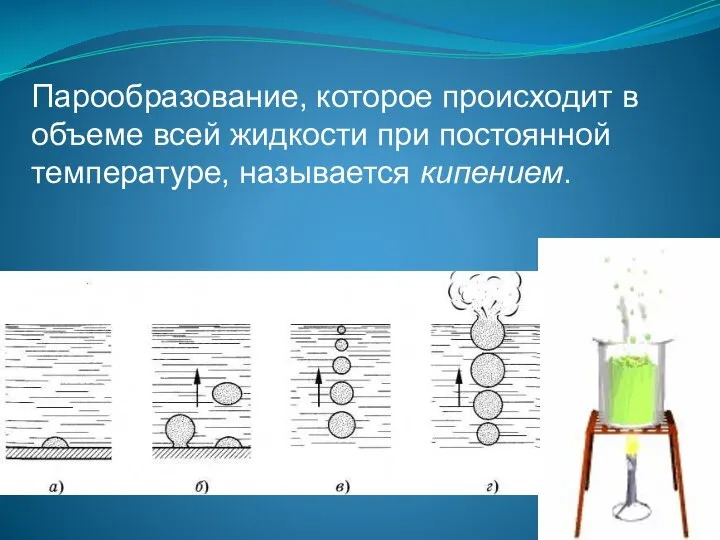
- 117. Парообразование, которое происходит в объеме всей жидкости при постоянной температуре, называется кипением.
- 118. При нагревании воды на дне и стенках сосуда появляются пузырьки газа. При дальнейшем нагревании число пузырьков
- 119. Архимедова сила отрывает пузырек ото дна и поднимает вверх, на месте оторвавшегося находится зародыш нового. 1
- 120. 2 этап. Температура всей жидкости одинакова. Теперь объем пузырьков при подъеме будет возрастать (т.к. давление насыщенного
- 121. Кипение жидкости происходит при одинаковой температуре всей жидкости, когда давление насыщенного пара этой жидкости, равно внешнему
- 122. КРИТИЧЕСКОЕ СОСТОЯНИЕ ВЕЩЕСТВА Критическая температура Tкр — это такая температура, при которой плотность жидкости и плотность
- 123. Давление насыщенного пара какого-либо вещества при его критической температуре называется критическим давлением pкр. Оно является наибольшим
- 125. Выше критической температуры жидкость не образуется даже при очень высоких давлениях. Обычно газом называют вещество в
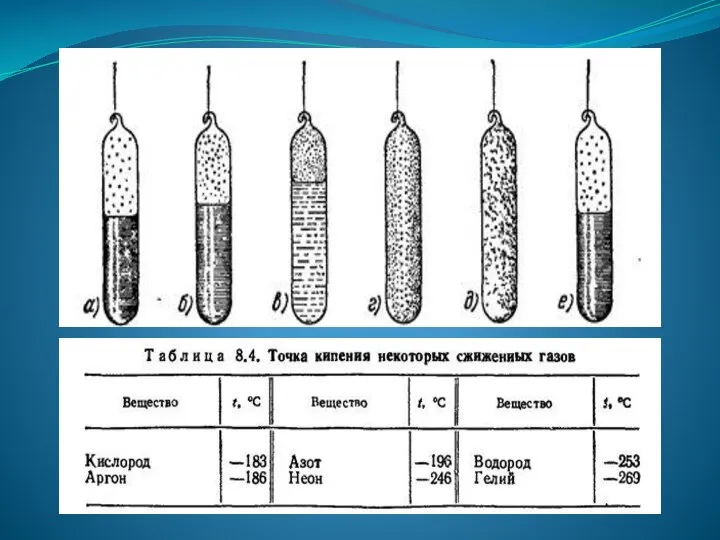
- 126. В настоящее время все газы переведены в жидкое состояние при очень низких температурах. Кислород: -118 °С;
- 127. ИСПОЛЬЗОВАНИЕ СЖИЖЕННЫХ ГАЗОВ 1. Для получения низких температур. 2. Для автогенной сварки (жидкий кислород). 3. На
- 128. ЗАНЯТИЕ № 26 ХАРАКТЕРИСТИКА ТВЕРДОГО СОСТОЯНИЯ ВЕЩЕСТВА. ПЛАВЛЕНИЕ И КРИСТАЛЛИЗАЦИЯ. ТЕПЛОВОЕ РАСШИРЕНИЕ ТВЕРДЫХ ТЕЛ И ЖИДКОСТЕЙ
- 129. Твердые вещества сохраняют форму и объем. По этим внешним признака к твердым относят кристаллические и аморфные
- 130. Аморфные вещества не имеют температуры плавления, так как являются вязкими жидкостями. Кристаллические вещества имеют температуру плавления,
- 132. Дефекты кристаллических решеток: - отсутствие частиц в узлах решетки, - смещение частиц в промежутки между узлами,
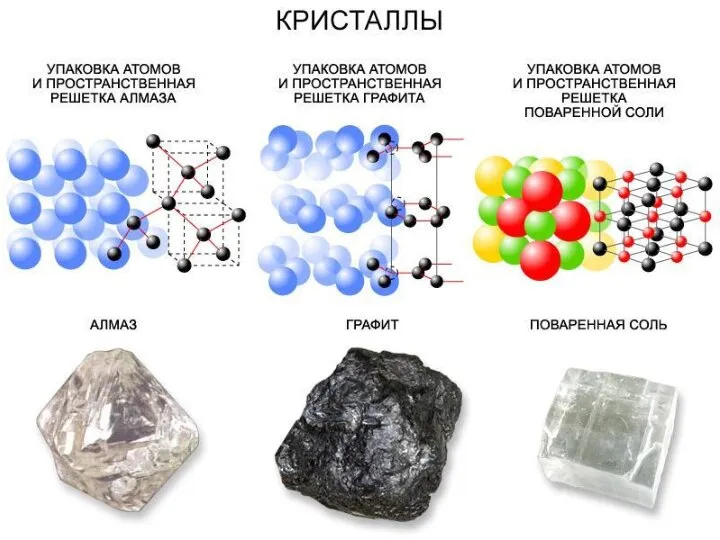
- 133. ТИПЫ КРИСТАЛЛИЧЕСКИХ СТРУКТУР 1. Ионная (поваренная соль) – в узлах решетки положительные и отрицательные ионы, между
- 134. 3. Металлическая (все металлы) – в узлах положительно заряженные ионы металла. Валентные электроны, слабо связанные с
- 135. Жидкие кристаллы – это фазовое состояние, в которое переходят некоторые вещества при определенных условиях (температура, давление,
- 136. ПРИМЕНЕНИЕ ЖИДКИХ КРИСТАЛЛОВ 1. Термография (тепловизионные системы: деятельность организма, пожарные, военные службы, техника, кондиционирование, теплоизоляция; микроболометрические
- 137. 3. Индикаторы для разных диапазонов температур различных конструкций. 4. В медицине как индикаторы (определение воспалений, опухолей).
- 138. Процесс перехода вещества из твёрдого кристаллического состояния в жидкое называют плавлением. Это процесс происходит при повышении
- 139. Процесс фазового перехода из жидкого состояния к твёрдому называется кристаллизацией. В отличие от плавления, когда вещество
- 140. Начальное состояние – a: нагревание льда до температуры плавления 0oC; a – b: процесс плавления при
- 144. 1. Тепловое расширение жидкостей. Тепловое расширение жидкости принято характеризовать его средним коэффициентом объемного расширения в рассматриваемом
- 145. 2. Особенности теплового расширения воды. Примеры расширения воды в природе. Самое распространенное на поверхности Земли вещество
- 146. Увеличение давления тоже понижает температуру наибольшей плотности воды. Особенности расширения воды имеют громадное значение для климата
- 147. 3. Значение теплового расширения. Расширение тел при нагревании и сжатие при охлаждении в природе играют огромную
- 148. Так как такие изменения объема зависят от рода вещества, то в горных породах, имеющих сложный состав,
- 149. В различного рода автоматических устройствах используются биметаллические пластинки. Такая пластинка состоит из двух разнородных металлических полос,
- 150. Такие пластинки используются для автоматического замыкания и размыкания электрических цепей в термостатах, в холодильниках, в противопожарных
- 151. ЗАНЯТИЕ № 27 УПРУГИЕ СВОЙСТВА ТВЕРДЫХ ТЕЛ. ЗАКОН ГУКА. МЕХАНИЧЕСКИЕ СВОЙСТВА ТВЕРДЫХ ТЕЛ.
- 152. ДЕФОРМАЦИИ Изменение объема или формы тела под действием каких-либо причин называется деформацией. Абсолютная деформация – это
- 153. Виды деформаций: - продольного растяжения, - продольного сжатия, - всестороннего растяжения, - всестороннего сжатия, - поперечного
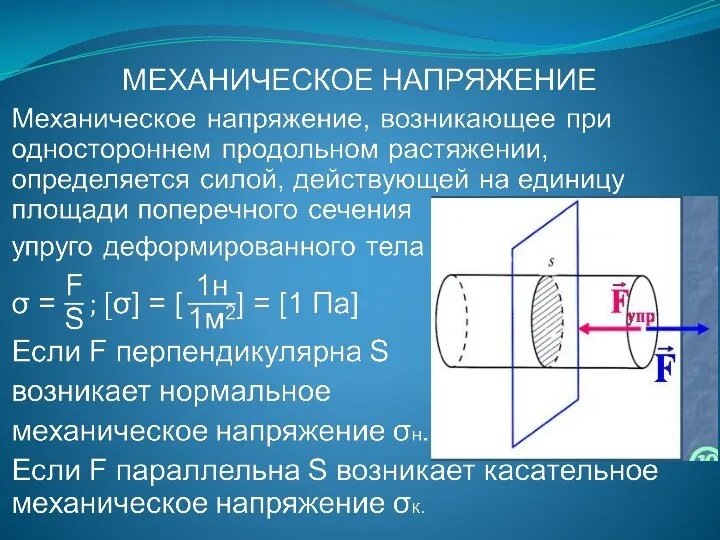
- 157. МЕХАНИЧЕСКОЕ НАПРЯЖЕНИЕ
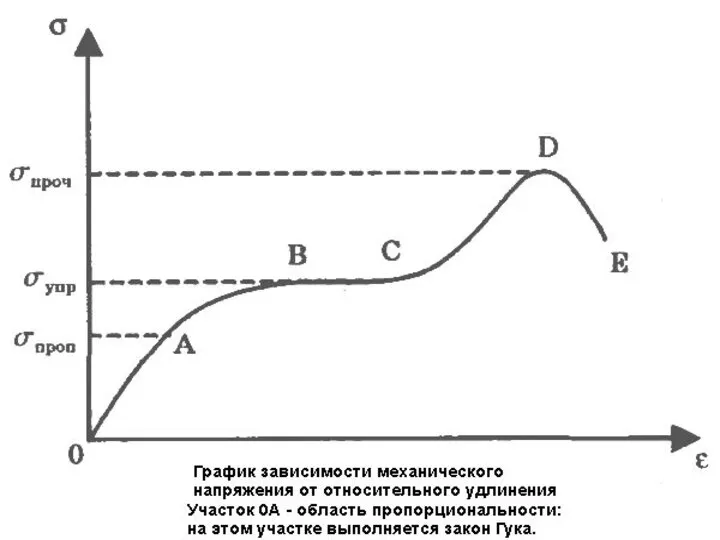
- 162. На диаграмме растяжения: - участок АО, на котором выполняется закон Гука, соответствует упругой деформации σпроп –
- 164. Скачать презентацию





































































































































 Графический материал к выпускной квалификационной (бакалаврской) работе на тему: Электроснабжение части села кучугуры
Графический материал к выпускной квалификационной (бакалаврской) работе на тему: Электроснабжение части села кучугуры Werkstoffkunde 2020-2021
Werkstoffkunde 2020-2021 Химические источники тока. Хит в будущем
Химические источники тока. Хит в будущем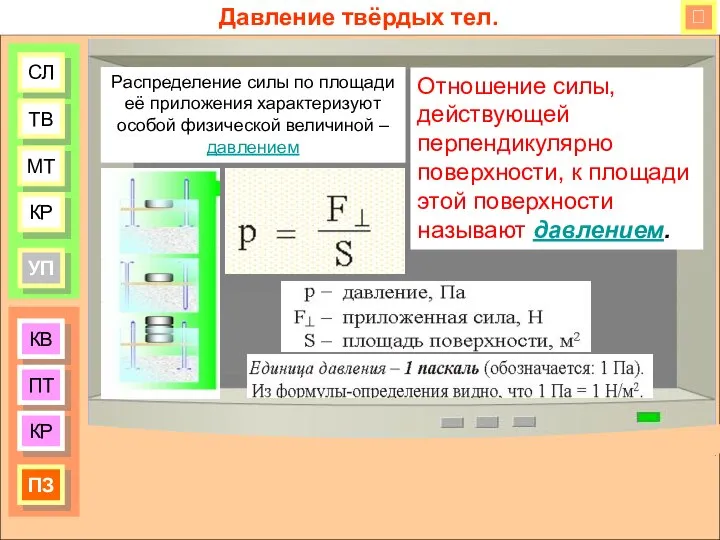 Давление твёрдых тел
Давление твёрдых тел Параметры потребителей и источника электроэнергии
Параметры потребителей и источника электроэнергии Шкала, первый импульс и N-формация
Шкала, первый импульс и N-формация Оптическая сила линзы
Оптическая сила линзы Подвеска
Подвеска Устройство ведущего моста трактора ДТ-75
Устройство ведущего моста трактора ДТ-75 Сила Архимеда – выталкивающая сила
Сила Архимеда – выталкивающая сила Коллективные спасательные средства. Тема 2.3
Коллективные спасательные средства. Тема 2.3 Расчет бункеров
Расчет бункеров Закон Ома. Сопротивление цепи
Закон Ома. Сопротивление цепи Презентация на тему Модели атомов. Опыт Резерфорда
Презентация на тему Модели атомов. Опыт Резерфорда  Магнитное поле
Магнитное поле Кинематика
Кинематика Колесно-моторный блок с МОП качения и ТЭД НБ-514Е
Колесно-моторный блок с МОП качения и ТЭД НБ-514Е Основы энергетики. Строение материи
Основы энергетики. Строение материи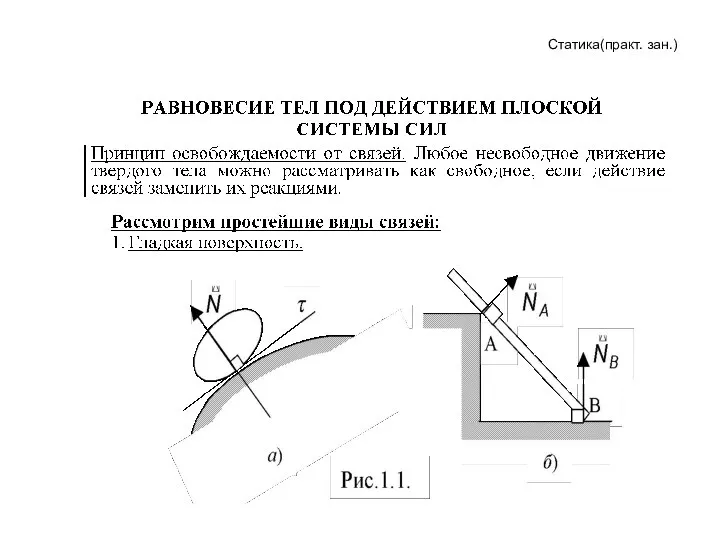 Равновесие тел под действием плоской системы сил
Равновесие тел под действием плоской системы сил Движение искусственных спутников
Движение искусственных спутников Тайны и чудеса зимушки-зимы
Тайны и чудеса зимушки-зимы Теория автоматического управления. Интегрирующие звенья
Теория автоматического управления. Интегрирующие звенья лекция 4_дифр Фраунгофера на ДР
лекция 4_дифр Фраунгофера на ДР Вес воздуха. Атмосферное давление
Вес воздуха. Атмосферное давление Презентация на тему Силы в природе (7 класс)
Презентация на тему Силы в природе (7 класс)  Аккумуляторная батарея
Аккумуляторная батарея Основные и дополнительные средства защиты в сетях напряжением выше 1000 в
Основные и дополнительные средства защиты в сетях напряжением выше 1000 в Применение электромагнитной индукции
Применение электромагнитной индукции