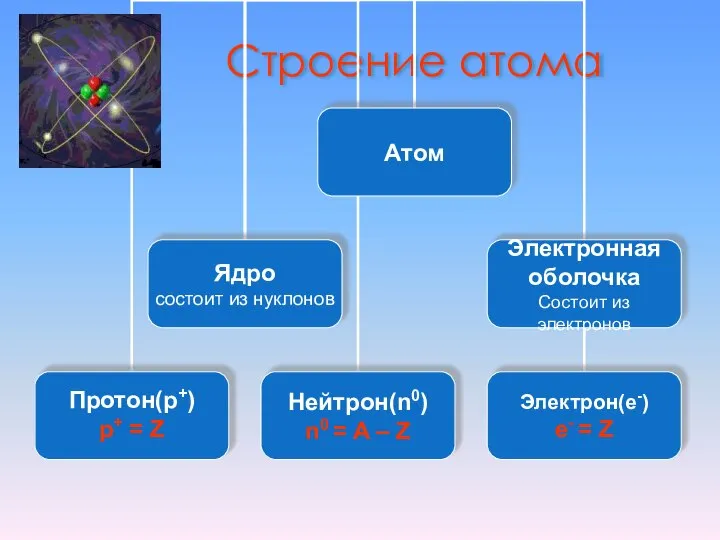
Слайд 2Молекула - наименьшая частица вещества, обладающая его химическими свойствами.
Атом - наименьшая частица химического элемента,

сохраняющая все его химические свойства
Слайд 3Первые представления о том, что вещество состоит из отдельных неделимых частиц, появились

в глубокой древности.
Атомизм - теория, согласно которой чувственно воспринимаемые (материальные) вещи состоят из химически неделимых частиц - атомов. Возникла в древнегреческой философии
Слайд 5Официально утверждено в 1860 году на международном съезде химиков

Слайд 7Долгое время господствовало мнение, что атомы неделимы. Однако в конце 19 века

был установлен ряд факторов, свидетельствующих о сложном составе атомов. Например, английский физик Джон Томсон в 1897 году открыл электрон, установил, что электроны содержатся во всех атомах, имеют отрицательный заряд, но в целом атом электронейтрален. Значит в атоме должны содержаться ещё и положительные частицы. Эти частицы и электрон назвали элементарными
Слайд 9Сумма масс протонов и нейтронов называется массовым числом атома (ядра) и выражает

его атомную массу:
p+ + n0 = А
n0 = А - p+
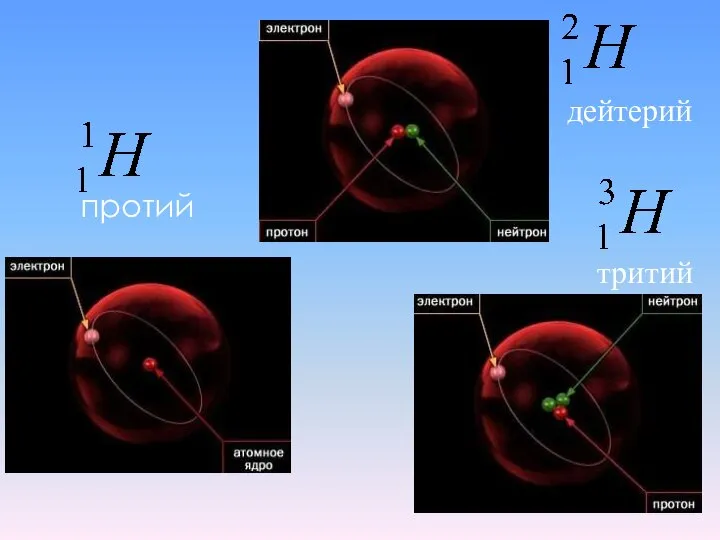
Слайд 10Изотопы - атомы одного и того же элемента с разной массой. Ядра

этих атомов содержат одинаковое число протонов, но разное число нейтронов. Поэтому в Периодической системе Д.И. Менделеева дана средняя арифметическая масса всех природных изотопов с учётом их распространения в природе (дробное число в Периодической системе). Например, встречаются атомы хлора с массой 35 и 37. У водорода изотопы носят индивидуальные названия: 1Н - легкий водород, 2Н - дейтерий (D), 3Н - тритий (Т)
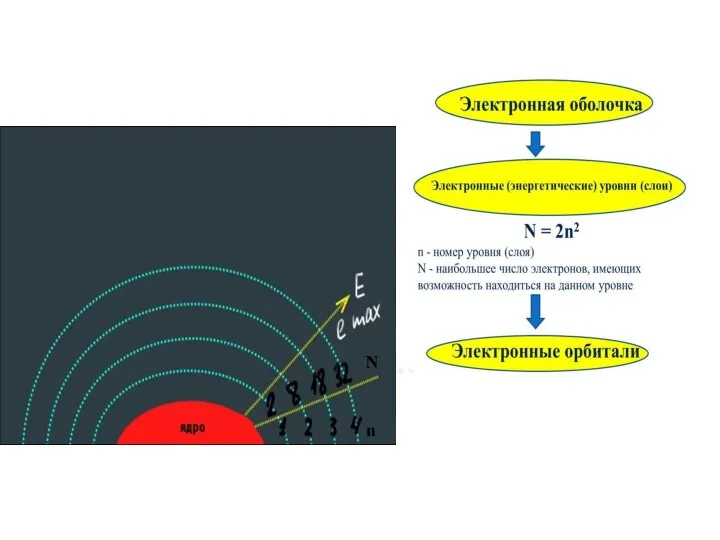
Слайд 14Электронная оболочка атома распадается на несколько энергетических уровней (слоёв). Электроны каждого следующего

слоя находятся на более высоком энергетическом уровне, чем электроны предыдущего слоя. Наибольшее число электронов N, имеющих возможность находиться на данном энергетическом уровне, равно удвоенному квадрату номера уровня:
N = 2n2 , где n - номер уровня (слоя).
Число электронов в наружном слое для всех элементов, кроме палладия, не превышает восьми, а в предпоследнем - восемнадцати.
Электронные уровни, в свою очередь, распадаются на электронные орбитали - область наиболее вероятного местонахождения электрона в пространстве
Слайд 15Электронные орбитали в основном состоянии бывают четырёх типов: s, p, d и
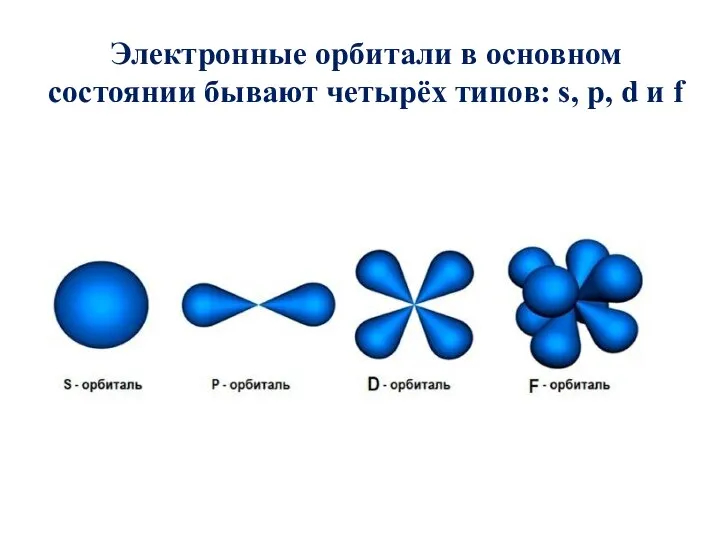
f
Слайд 18Порядковый номер в Периодической системе Д.И. Менделеева - важнейшая константа элемента, выражающая:
а)

общее количество электронов в атоме;
б) заряд атомного ядра;
в) число протонов в ядре.
Номер периода химического элемента в Периодической системе Д.И. Менделеева указывает на число энергетических уровней. Номер группы указывает на число электронов на внешнем энергетическом уровне
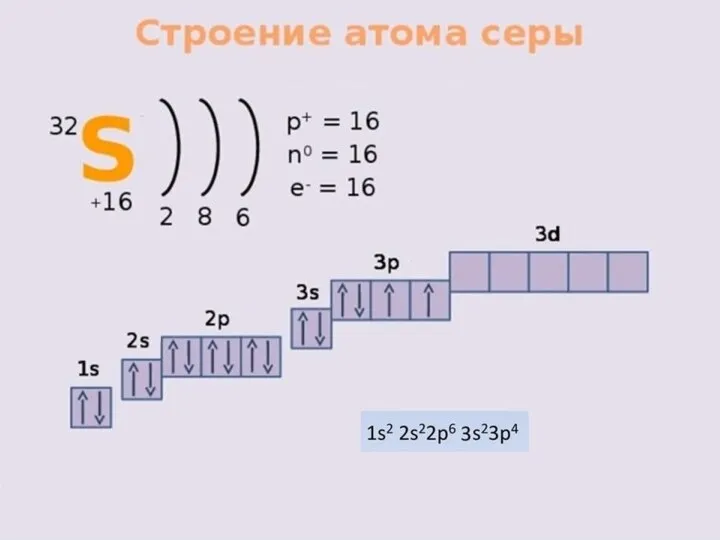
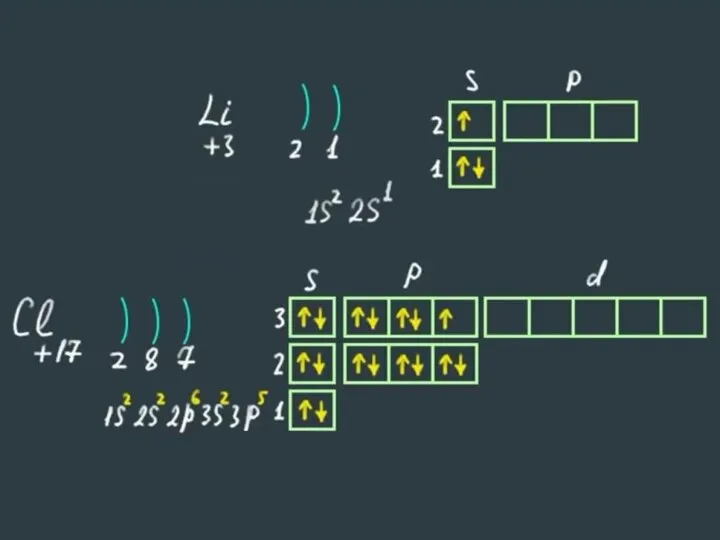
Слайд 19Алгоритм составления электронных формул строения атомов
Записываем знак химического элемента и заряд ядра

его атома (№ элемента).
Определяем количество энергетических уровней (№ периода) и количество электронов на каждом уровне.
Составляем электронную формулу, учитывая номер уровня, вид орбитали и количество электронов на ней
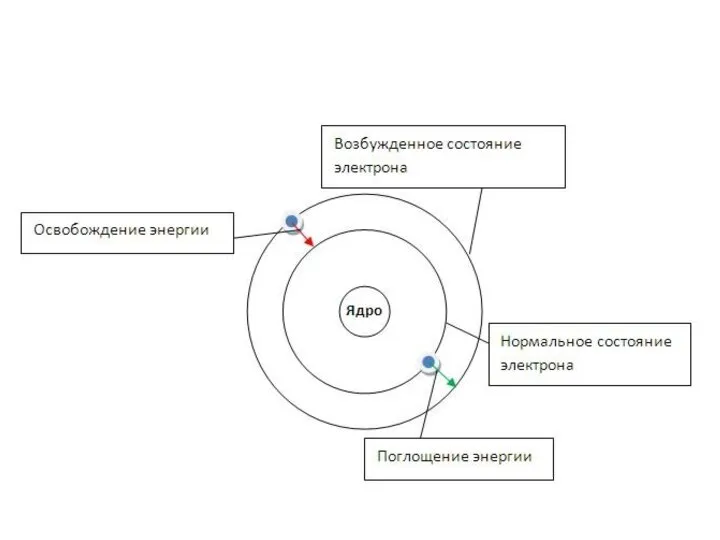
Слайд 23Состояния атомов
Атомы устойчивы лишь в некоторых стационарных состояниях, которым отвечают определенные значения

энергии.
Наинизшее из разрешённых энергетических состояний атома называется основным, а все остальные - возбуждёнными.
Возбужденные состояния атомов образуются из основного состояния при переходе одного или нескольких электронов с занятых орбиталей на свободные (или занятые лишь 1 электроном)
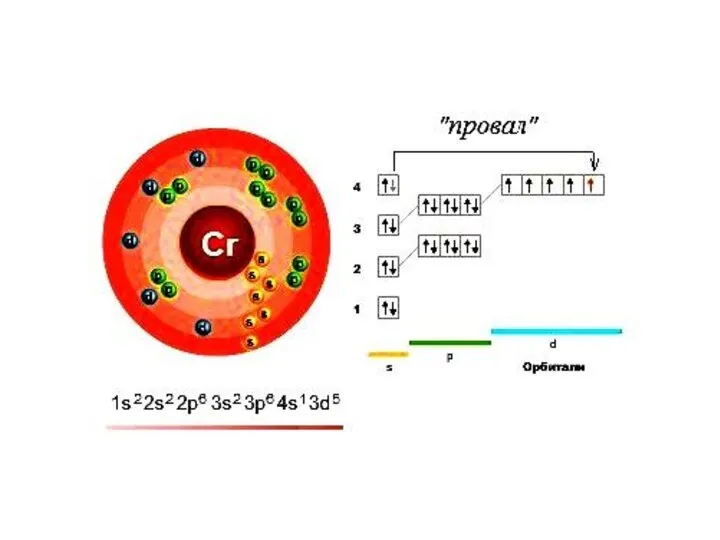
Слайд 25От того, какой энергетический подуровень заполняется электронами последним, различают 4 электронных семейства
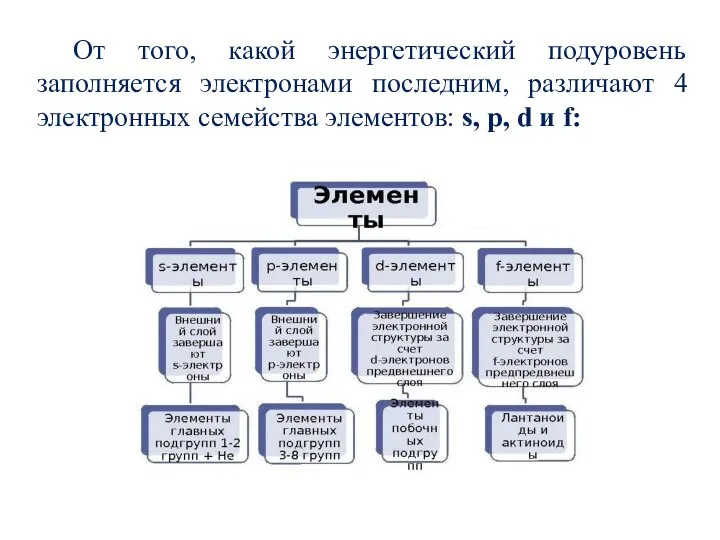
элементов: s, p, d и f:



















 Презентация на тему Трансформаторы (11 класс)
Презентация на тему Трансформаторы (11 класс)  Механическая работа. Единицы работы
Механическая работа. Единицы работы Расчёт режимов разомкнутых сетей
Расчёт режимов разомкнутых сетей Теплотехнология. Приемники энергии
Теплотехнология. Приемники энергии Презентация на тему Физика в картинках
Презентация на тему Физика в картинках  Электрическая емкость
Электрическая емкость Физические явления и интересные факты
Физические явления и интересные факты Презентация на тему Закон Паскаля
Презентация на тему Закон Паскаля  Презентация на тему Трехфазный тиристорный преобразователь
Презентация на тему Трехфазный тиристорный преобразователь  Электромагнитные колебания
Электромагнитные колебания Интенсивность звука в идеальной жидкости
Интенсивность звука в идеальной жидкости Закон Ома для участка цепи
Закон Ома для участка цепи Презентация на тему Люминесцентный анализ
Презентация на тему Люминесцентный анализ  Теплоносители и их свойства. Местная вентиляция и кондиционирование воздуха. (Тема 14)
Теплоносители и их свойства. Местная вентиляция и кондиционирование воздуха. (Тема 14) Основные положения теплопроводности
Основные положения теплопроводности Расчет силы тока и напряжения в электрических цепях
Расчет силы тока и напряжения в электрических цепях Физическая оптика: интерференция и дифракция. Лекция 2
Физическая оптика: интерференция и дифракция. Лекция 2 Окружающие нас тела называются физическими телами. Строение вещества. Молекула
Окружающие нас тела называются физическими телами. Строение вещества. Молекула Материалы, применяемые в машиностроении. II часть
Материалы, применяемые в машиностроении. II часть Гидродинамика. Движение жидкости
Гидродинамика. Движение жидкости Классификация подъемно-транспортных машин
Классификация подъемно-транспортных машин Инструкция по сборке стальной рамы Prusa i3 Steel Pro для модификации 3d принтера Anet A6
Инструкция по сборке стальной рамы Prusa i3 Steel Pro для модификации 3d принтера Anet A6 Что такое мощность
Что такое мощность Электрическое напряжение. Вольтметр. Измерение напряжения
Электрическое напряжение. Вольтметр. Измерение напряжения Физические задачи с литературным содержанием
Физические задачи с литературным содержанием Разбор выполнения заданий
Разбор выполнения заданий Идеальный газ
Идеальный газ Теплопроводность через плоскую и цилиндрическую стенки при граничных условиях третьего рода (теплопередача)
Теплопроводность через плоскую и цилиндрическую стенки при граничных условиях третьего рода (теплопередача)