Слайд 2 Электролиты – это водные растворы солей, кислот, щелочей. Носителями заряда в электролитах

являются положительные и отрицательные ионы.
Слайд 3 Диссоциация – это процесс расщепления молекул электролита на положительные
и отрицательные ионы
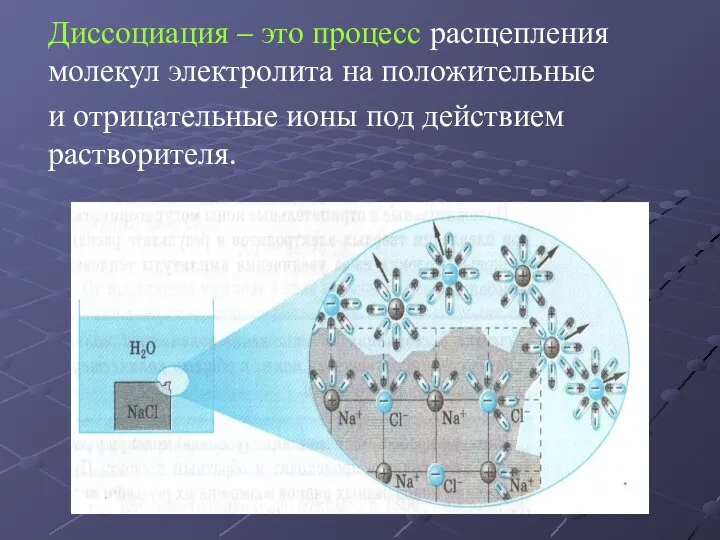
под действием растворителя.
Слайд 4Уравнение диссоциации хлорида меди.

Слайд 5Рекомбинация – это процесс соединение ионов в нейтральную молекулу. Если в электролите
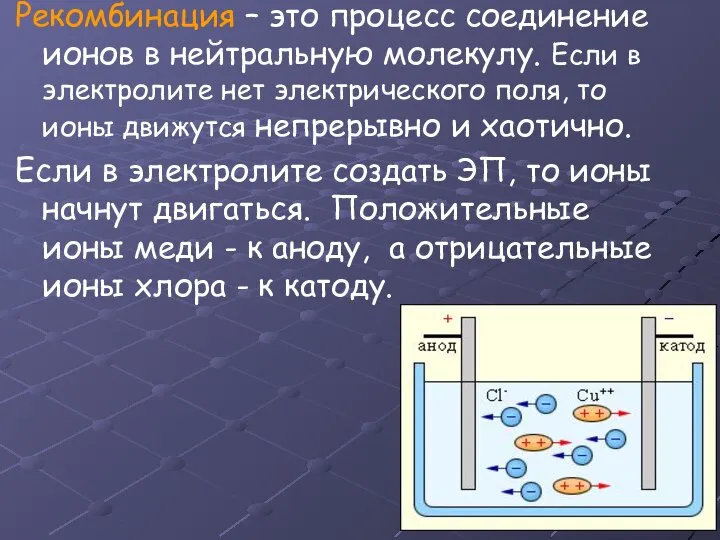
нет электрического поля, то ионы движутся непрерывно и хаотично.
Если в электролите создать ЭП, то ионы начнут двигаться. Положительные ионы меди - к аноду, а отрицательные ионы хлора - к катоду.
Слайд 6Ток в электролитах – это упорядоченное движение
положительных и отрицательных ионов.
+
-
Катод
_
Анод
+
Направление тока в

электролите
Слайд 7 При прохождении электрического тока через электролит наблюдается выделение веществ, входящих в
электролит,

на электродах. Электролиз – это явление выделения на электродах веществ, входящих в состав электролита, при протекании через него электрического тока.
Слайд 8Закон Фарадея для электролиза формулируется так:
Масса m вещества, выделившегося на
электроде, прямо

пропорциональна
заряду q, прошедшему через электролит:
m = kq = kIt.
Величину k называют электрохимическим
эквивалентом и находят для разных веществ в таблице.
Слайд 101.Гальваностегия – это…
декоративное или
антикоррозийное
покрытие металлических
изделий тонким слоем
другого металла

(никелирование,
хромирование,
омеднение, золочение,
серебрение).
Слайд 112.Гальванопластика – это…
электролитическое
изготовление
металлических
копий, рельефных
предметов.

Слайд 123.Электрометаллургия – это…
получение чистых металлов (Al, Na, Mg, Be)
при электролизе расплавленных руд.

Слайд 134.Рафинирование металлов – это…
очистка металлов от примесей с помощью
электролиза, когда
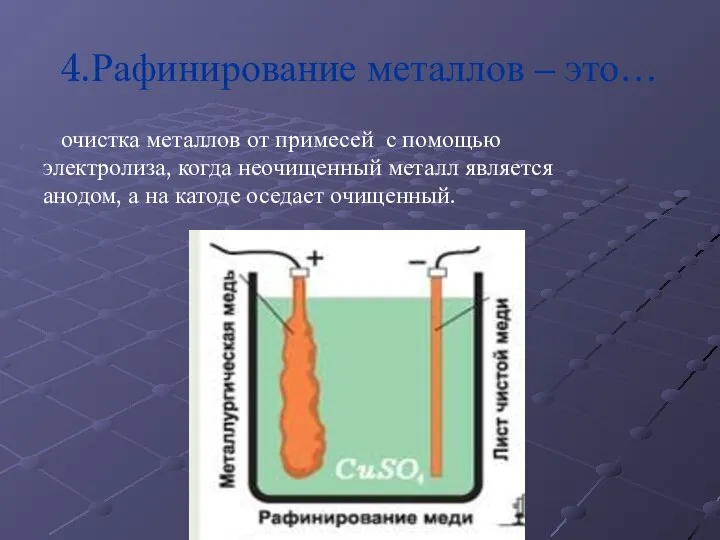
неочищенный металл является
анодом, а на катоде оседает очищенный.
Слайд 14Практическая работа
по теме «Законы Фарадея»














 Решения задач по теме Плавление и отвердевание кристаллических тел
Решения задач по теме Плавление и отвердевание кристаллических тел Презентация ученицы 11 «А» класса Очеретиной Александры
Презентация ученицы 11 «А» класса Очеретиной Александры Характеристические параметры четырехполюсника. Вносимое затухание четырехполюсника. Лекция 11
Характеристические параметры четырехполюсника. Вносимое затухание четырехполюсника. Лекция 11 Radioaktive Strahlung
Radioaktive Strahlung Презентация на тему Три состояния вещества
Презентация на тему Три состояния вещества  Оценка успешности прогнозов волнения
Оценка успешности прогнозов волнения Абсолютный нуль температуры
Абсолютный нуль температуры Реактивное движение в военном деле
Реактивное движение в военном деле Презентация на тему Скорость прямолинейного равноускоренного движения
Презентация на тему Скорость прямолинейного равноускоренного движения  Тайны мыльных пузырей
Тайны мыльных пузырей Виды соединения проводников. Работа тока
Виды соединения проводников. Работа тока Школа №625 11 класс Н.М.Турлакова
Школа №625 11 класс Н.М.Турлакова Практическая работа №4. Введение в химию и технологию
Практическая работа №4. Введение в химию и технологию Звездный час. Урок – игра
Звездный час. Урок – игра Ветрогенератор-фонарь
Ветрогенератор-фонарь Изменения школьного процесса обучения физике в условиях обновления образования
Изменения школьного процесса обучения физике в условиях обновления образования Элемент Вольта
Элемент Вольта Презентация на тему Амперметр
Презентация на тему Амперметр  Применение физических законов при решении задач по астрофизике
Применение физических законов при решении задач по астрофизике Проект по фізиці. Шлях, який проходить вчитель за день
Проект по фізиці. Шлях, який проходить вчитель за день Источники тока
Источники тока Организация технического обслуживания и ремонта и ремонта в автотранспортной организации 1-37 01 06 ТЭА
Организация технического обслуживания и ремонта и ремонта в автотранспортной организации 1-37 01 06 ТЭА Магнит өрісінің. Дивергенция және Роторы
Магнит өрісінің. Дивергенция және Роторы Сравнение КАМАЗ-5490 NEO и КАМАЗ-54901
Сравнение КАМАЗ-5490 NEO и КАМАЗ-54901 1f712686a0a73c13b3172265a60c76b1
1f712686a0a73c13b3172265a60c76b1 Скорость света
Скорость света Закон сохранения массы веществ
Закон сохранения массы веществ Физические величины, используемые в химии
Физические величины, используемые в химии