Содержание
- 2. Кислотно-основным называется титриметрический метод анализа, основанный на использовании протолитических реакций Н3O+ + OH-→ 2H2O условно Н++ОН-
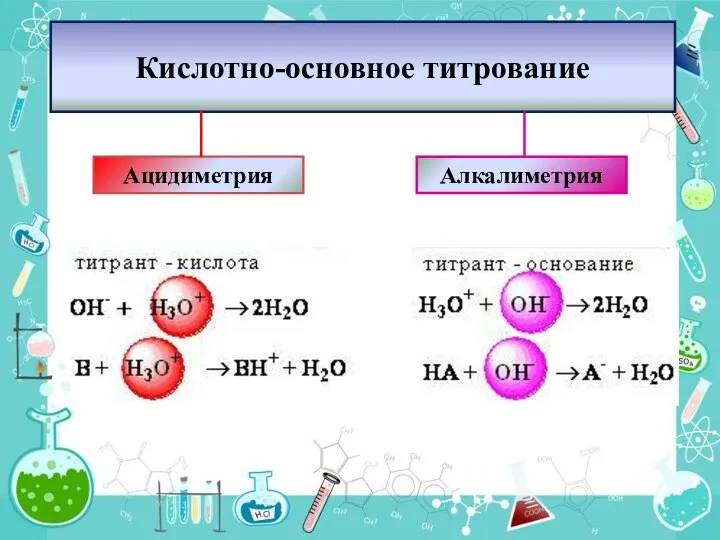
- 3. Кислотно-основное титрование Ацидиметрия Алкалиметрия
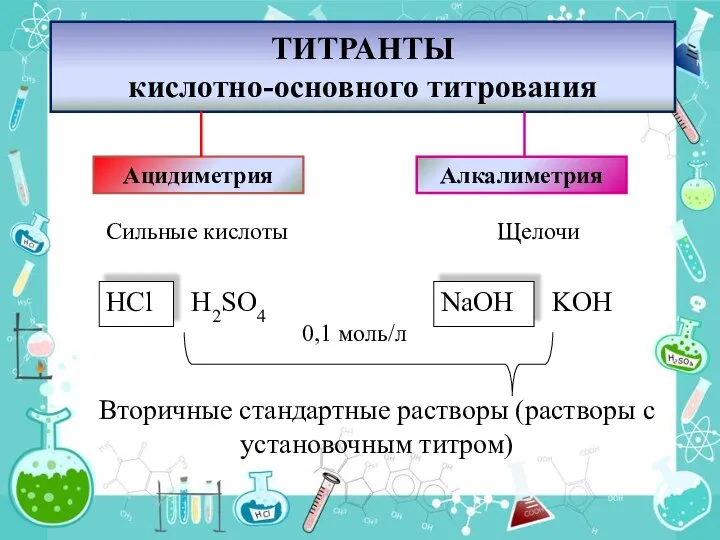
- 4. ТИТРАНТЫ кислотно-основного титрования Ацидиметрия Алкалиметрия Сильные кислоты Щелочи 0,1 моль/л Вторичные стандартные растворы (растворы с установочным
- 5. Приготовить титрованный раствор щелочи по навеске не возможно содержит примеси (механические, карбонаты); растворы поглощают CO2 воздуха
- 6. Приготовить тированный раствор кислоты исходя из концентрированной кислоты невозможно серная кислота гигроскопична, концентрированная соляная кислота выделяет
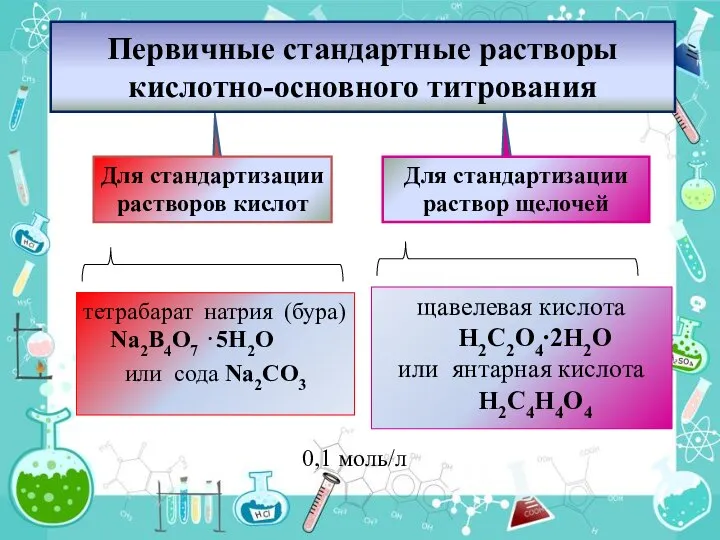
- 7. Первичные стандартные растворы кислотно-основного титрования Для стандартизации растворов кислот Для стандартизации раствор щелочей тетрабарат натрия (бура)
- 8. Точка эквивалентности при реакции нейтрализации не сопровождается каким-либо внешним изменением, поэтому для определения конца реакции применяются
- 9. ИНДИКАТОРЫ (лат. Indicator – указатель)- химические вещества, изменяющие окраску, люминесценцию или образующие осадок при изменении концентрации
- 10. Индикаторы характеризуются интервалом перехода окраски - пределы концентраций ионов водорода, металла или вещества, при которых происходит
- 11. Требования, предъявляемые к кислотно-основным индикаторам 1. Вещества, используемые в качестве индикаторов, должны обладать интенсивной окраской (иметь
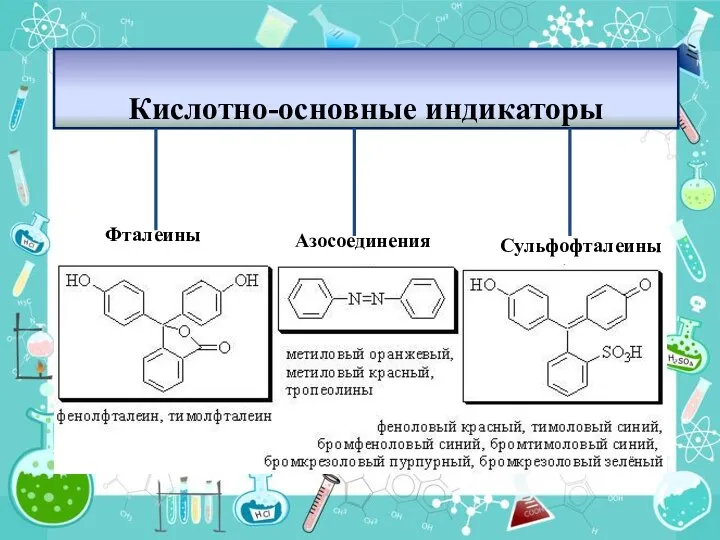
- 12. Кислотно-основные индикаторы Фталеины Азосоединения Сульфофталеины
- 13. Индикаторы методов кислотно-основного титрования
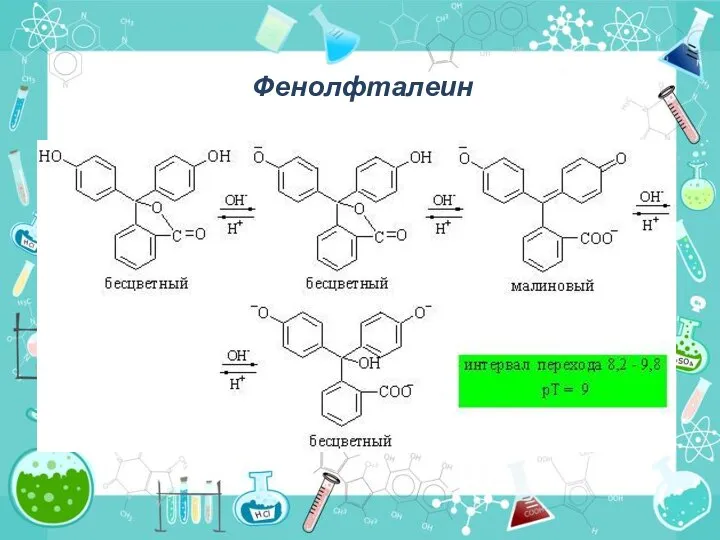
- 14. Фенолфталеин
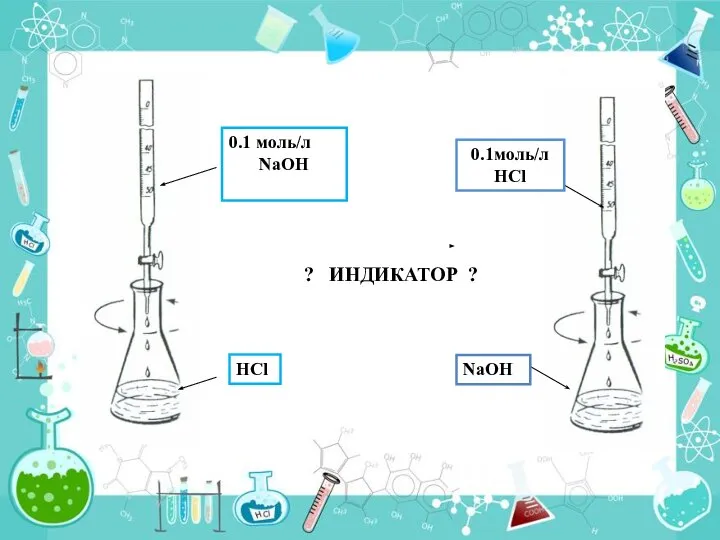
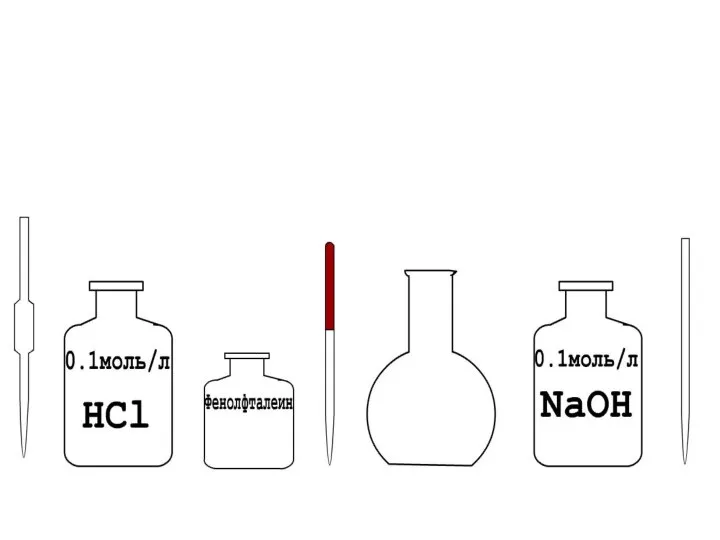
- 15. 0.1моль/л HCl NaOH ? ИНДИКАТОР ?
- 17. Чтобы определить концентрацию одного из растворов, надо знать точно объемы реагирующих растворов, точную концентрацию другого раствора
- 18. Прямое титрование HCl метилоранж На примере Соляной кислоты Титрант NaOH 0,1 моль/л
- 19. РАСЧЕТНАЯ ФОРМУЛА
- 20. VNaOH - среднее арифметическое значение объема раствора гидроксида натрия, пошедшего на титрование; T NaOH/HCl и Кп
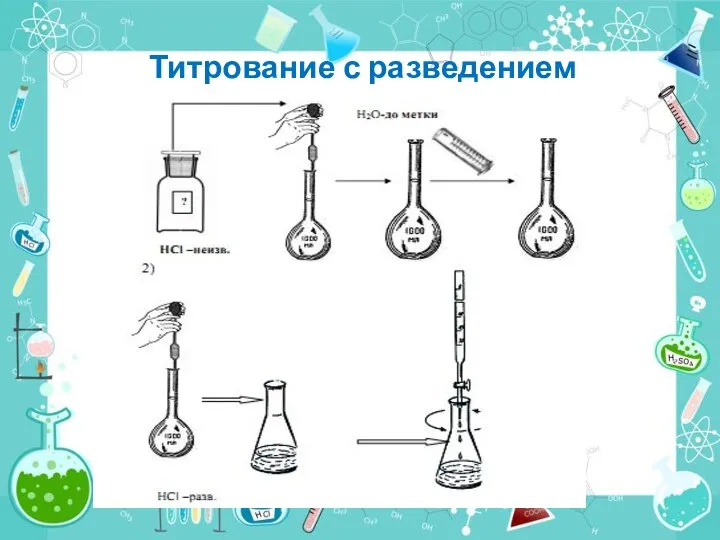
- 21. Титрование с разведением
- 22. РАСЧЕТНАЯ ФОРМУЛА С РАЗВЕДЕНИЕМ
- 23. VNaOH - среднее арифметическое значение объема раствора гидроксида натрия, пошедшего на титрование; T NaOH/HCl и Кп
- 25. Скачать презентацию














 Тренажёр: знаки химических элементов
Тренажёр: знаки химических элементов Алкены. Физические и химические свойства
Алкены. Физические и химические свойства Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Химически опасные объекты Аварии, связанные с выбросом АХОВ
Химически опасные объекты Аварии, связанные с выбросом АХОВ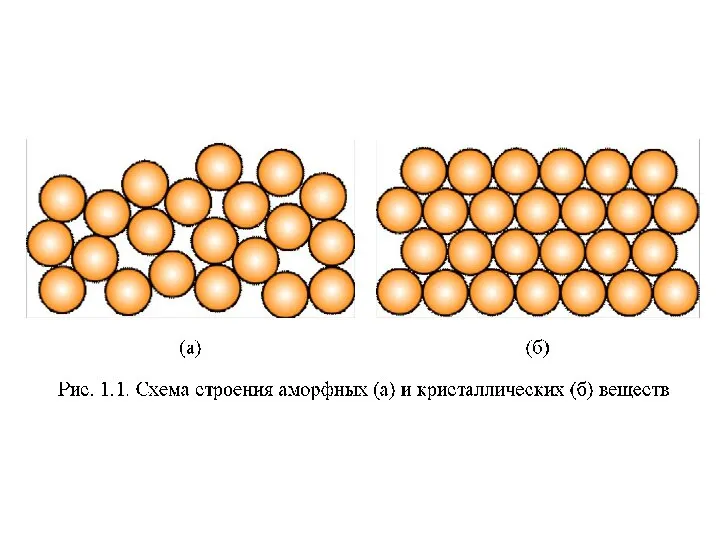 Материаловедение
Материаловедение Синтетические волокна
Синтетические волокна Презентация на тему Неметаллы, особенности строения
Презентация на тему Неметаллы, особенности строения  Электролиз (катод)
Электролиз (катод) Основные принципы работы химических сенсоров
Основные принципы работы химических сенсоров Химическая картина мира
Химическая картина мира Основания: определение, классификация, химические свойства
Основания: определение, классификация, химические свойства Металлы. Общая характеристика, химические свойства. Получение
Металлы. Общая характеристика, химические свойства. Получение Вебинар. Гидролиз солей
Вебинар. Гидролиз солей Свойства радиоактивных элементов
Свойства радиоактивных элементов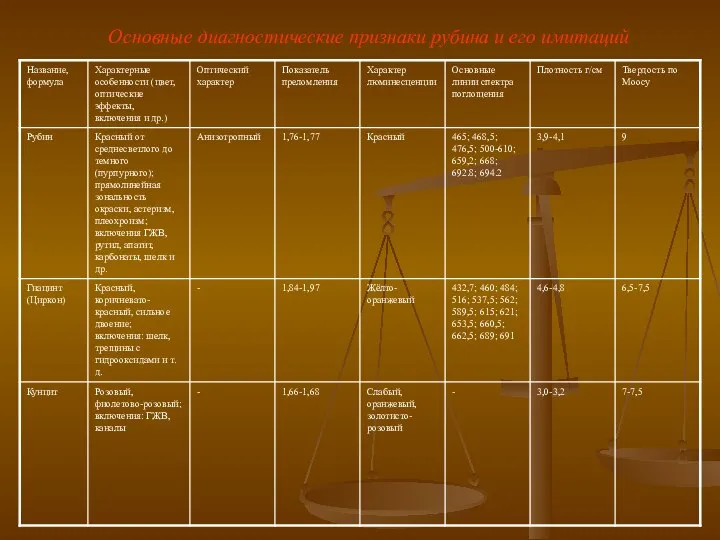 Основные диагностические признаки рубина и его имитаций
Основные диагностические признаки рубина и его имитаций Генетические ряды неорганических соединений
Генетические ряды неорганических соединений Двойные латуни. Диаграмма состояния. Примеси. Структура и свойства
Двойные латуни. Диаграмма состояния. Примеси. Структура и свойства Вуглеводи. Визначення вуглеводів
Вуглеводи. Визначення вуглеводів Галогены. Обобщение знаний
Галогены. Обобщение знаний Подготовка к ГИА по химии
Подготовка к ГИА по химии Предпосылки открытия Периодического закона Д. И. Менделеевым
Предпосылки открытия Периодического закона Д. И. Менделеевым ОВ. Структура и принцип работы параметры ОВ
ОВ. Структура и принцип работы параметры ОВ Абсолютное первенство по химии - 2012
Абсолютное первенство по химии - 2012 строение атома углерода. Валентные состояния атома углерода
строение атома углерода. Валентные состояния атома углерода Общая характеристика элементов IIА группы
Общая характеристика элементов IIА группы Вода… Химические названия
Вода… Химические названия Водород – первый элемент в периодической таблице
Водород – первый элемент в периодической таблице Кристаллы, выращенные учащимися
Кристаллы, выращенные учащимися