Слайд 2Al
13
Алюминий
(лат. (лат. Aluminium(лат. Aluminium)
3
8
2
26,9815
3s2 3p1
Порядковый номер. Химический элемент III группы

главной подгруппы 3-го периода.
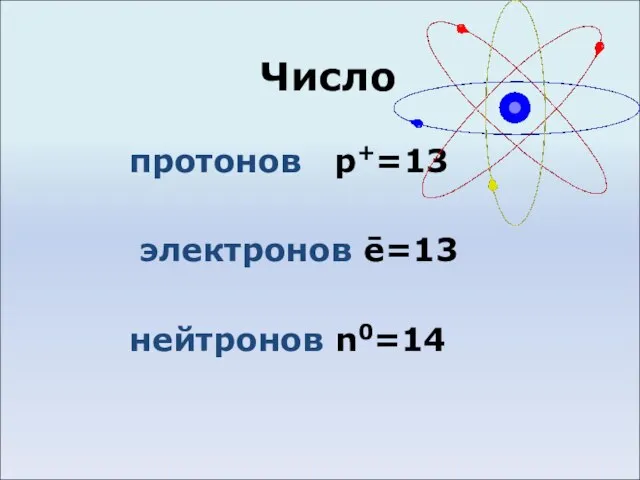
Слайд 3Число
протонов p+=13
электронов ē=13
нейтронов n0=14
Слайд 4Схема расположения электронов на энергетических подуровнях
+13Al 1s2 2s2 2p6 3s2 3p1
1s
2s
2p
3s
3p
в
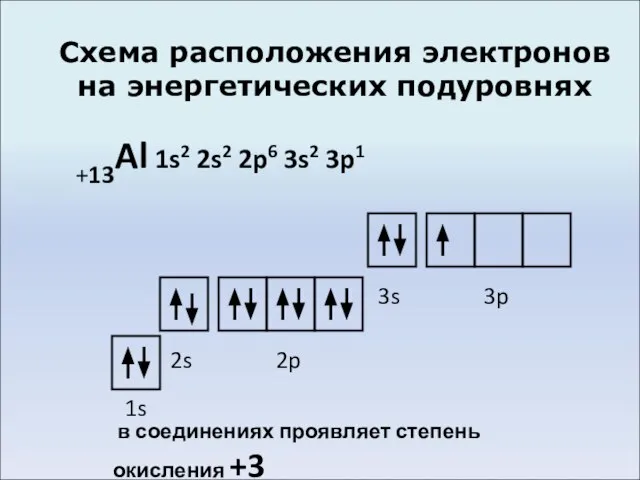
соединениях проявляет степень окисления +3
Слайд 5Al – типичный металл
Восстановительные свойства
Al 0- 3ē Al+3
Тип химической связи -металлическая
Тип

кристаллической решетки – кубическая гранецентрированная
Слайд 6Физические свойства вещества
Al – серебристо-белый металл, пластичный, легкий, хорошо проводит тепло и

электрический ток, обладает хорошей ковкостью, легко поддаётся обработке, образует лёгкие и прочные сплавы.
ρ=2,7 г/см3
tпл.=6600С
Слайд 7Особенности физических и химических свойств алюминия, его нахождения в природе и применения:
Алюминий

– самый распространенный металл земной коры. Его ресурсы практически неисчерпаемы.
Обладает высокой коррозионной стойкостью и практически не нуждается в специальной защите.
Высокая химическая активность алюминия используется в алюминотермии.
Малая плотность в сочетании с высокой прочностью и пластичностью его сплавов делает алюминий незаменимым конструкционным материалом в самолетостроении и способствует расширению его применения в наземном и водном транспорте, а также в строительстве.
Относительно высокая электропроводность позволяет заменять им значительно более дорогую медь в электротехнике.
Слайд 8Алюминий реагирует с простыми веществами - неметаллами
4Al+3O2 = 2Al2O3
Поверхность покрывается

пленкой оксида, в мелкораздробленном виде горит с выделением большого количества теплоты.
2. 2Al + 3Cl2 = 2 AlCl3
3. 2Al + 3S = Al2S3 - при нагревании
4. 4Al + 3С = Al4С3 - при нагревании
Слайд 9Алюминий реагирует со сложными веществами:
Алюминий растворяется в растворах кислот
2Al + 6HCl =

2AlCl3 + 3H2
2Al + 3H2SO4 = Al2(SO4)3 + 3H2
Концентрированная серная и азотная кислоты пассивируют алюминий.
2. Алюминий реагирует с растворами солей менее активных металлов
2Al + 3СuCl2 = 2AlCl3 + 3Cu
Слайд 10Алюминий реагирует со сложными веществами:
3. Алюминий при высокой температуре реагирует с оксидами

менее активных металлов (Алюминотермия – получение металлов: Fe, Cr, Mn, Ti, W и других, путем их восстановления алюминием)
8Al + 3Fe3O4 = 4Al2O3 + 9Fe
Слайд 11Алюминий реагирует со сложными веществами:
4.Так как алюминий – амфотерный металл, он реагирует

с растворами щелочей.
При этом образуется тетрагидроксоалюминат натрия и выделяется водород:
2Al + 2NaOH + 6H2O = 2Na[Al(OH)4] + 3H2
5. При удалении оксидной пленки с поверхности алюминия, он реагирует с водой с образованием гидроксида алюминия и водорода:
2Al + 6H2O = 2Al(OH)3 +3H2
Слайд 12Получение алюминия
Алюминий получают электролизом раствора глинозема в расплавленном криолите (Na3AIF6) и
электролизом расплава

AlCl3
Слайд 14
Соединения алюминия
В природе алюминий встречается только в виде соединений и по

распространенности в земной коре занимает первое место среди металлов и третье – среди всех элементов (после кислорода и кремния). Общее содержание алюминия в земной коре составляет 8,8 % по массе.
Слайд 15Оксид алюминия Al2О3:
Очень твердый (корунд, рубин)в кристаллическом состоянии, порошок белого цвета, тугоплавкий

- 20500С.
Не растворяется в воде.
Амфотерный оксид, взаимодействует:
а) с кислотами Al2O3 + 6H+ = 2Al3+ + 3H2O
б) со щелочами Al2O3 + 2OH- = 2AlO-2 + H2O
Образуется:
а) при окислении или горении алюминия на воздухе
4Al + 3O2 = 2Al2O3
б) в реакции алюминотермии
2Al + Fe2O3 = Al2O3 + 2Fe
в) при термическом разложении гидроксида алюминия 2Al (OH)3 = Al2O3 + 3H2O













 Презентация на тему Алмазы Индии
Презентация на тему Алмазы Индии  Водные биоресурсы и аквакультура. Расчеты в объемном анализе
Водные биоресурсы и аквакультура. Расчеты в объемном анализе Термохимия
Термохимия Исследование снега на общую химическую токсичность методом биотестирования Автор: Милюта Юлия, Тюменская область, Тюменский рай
Исследование снега на общую химическую токсичность методом биотестирования Автор: Милюта Юлия, Тюменская область, Тюменский рай Топливоснабжение источников децентрализованного теплоэнергоснабжения
Топливоснабжение источников децентрализованного теплоэнергоснабжения Ключевые реакции и регуляторные ферменты начальных этапов углеводного обмена
Ключевые реакции и регуляторные ферменты начальных этапов углеводного обмена Исследование химического состава разных сортов картофеля
Исследование химического состава разных сортов картофеля Знаки химических элементов. Периодическая система
Знаки химических элементов. Периодическая система Задачи. Периодическая система. Строение атома. Повторение
Задачи. Периодическая система. Строение атома. Повторение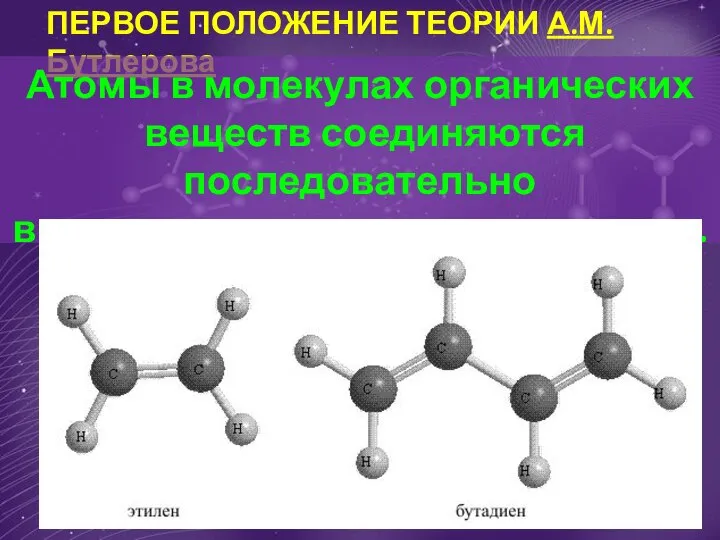 Первое положение теории А.М. Бутлерова Атомы в молекулах органических веществ соединяются последовательно
Первое положение теории А.М. Бутлерова Атомы в молекулах органических веществ соединяются последовательно Презентация на тему Спирты
Презентация на тему Спирты  Окислительно-восстновительные реакции
Окислительно-восстновительные реакции Реакционная система. Схема химической реакции. Закон сохранения массы веществ в химической реакции
Реакционная система. Схема химической реакции. Закон сохранения массы веществ в химической реакции Презентация на тему Химические средства гигиены и косметика
Презентация на тему Химические средства гигиены и косметика  РАСЧЕТЫ по химическим уравнениям
РАСЧЕТЫ по химическим уравнениям Алкены (непредельные углеводороды)
Алкены (непредельные углеводороды) Полимеры. Пластмассы
Полимеры. Пластмассы Переработка каменного угля. Коксование
Переработка каменного угля. Коксование Презентация по Химии "Быль о каучуке"
Презентация по Химии "Быль о каучуке"  Химические свойства и применение этилена
Химические свойства и применение этилена Интегративный подход к обучению на уроках химии
Интегративный подход к обучению на уроках химии Фосфор - светоносный
Фосфор - светоносный Приключение кислорода
Приключение кислорода Щелочно-земельные металлы и магний
Щелочно-земельные металлы и магний Типы химических реакций
Типы химических реакций Гидролиз солей
Гидролиз солей Знакомство с химией
Знакомство с химией Навчальний проект Дослідження зміни концентрації CO2 у класній кімнаті під час занять
Навчальний проект Дослідження зміни концентрації CO2 у класній кімнаті під час занять