Содержание
- 2. Русский язык Химический язык Буквы (33) Знаки химических элементов Слова Химические формулы Предложения Уравнения химических реакций
- 3. Состав веществ выражают химическими формулами Вещества по качественному составу делятся на простые и сложные. Простые вещества
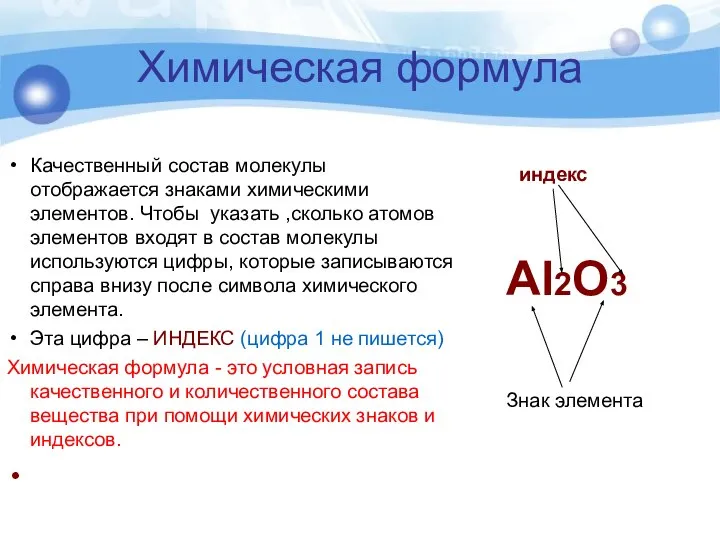
- 4. Химическая формула Качественный состав молекулы отображается знаками химическими элементов. Чтобы указать ,сколько атомов элементов входят в
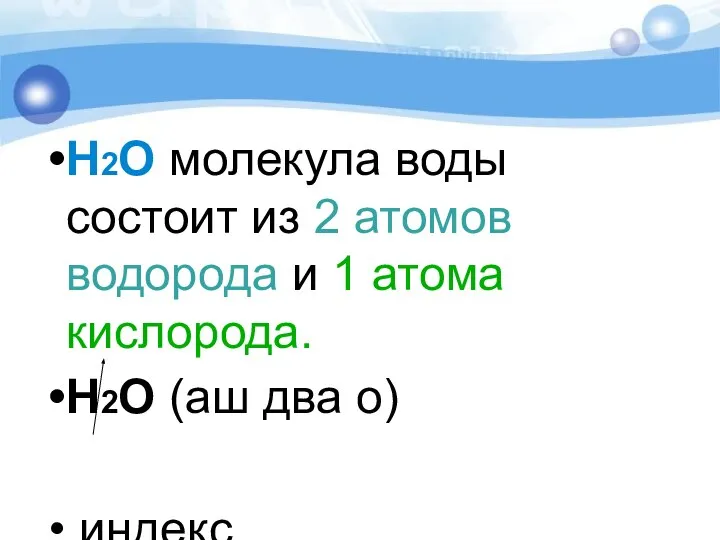
- 5. Н2О молекула воды состоит из 2 атомов водорода и 1 атома кислорода. Н2О (аш два о)
- 6. Прочитайте (произнесите) формулы: SiO2 (силициум о два) CO2 (це о два) HCl (аш хлор) 4Н2О –
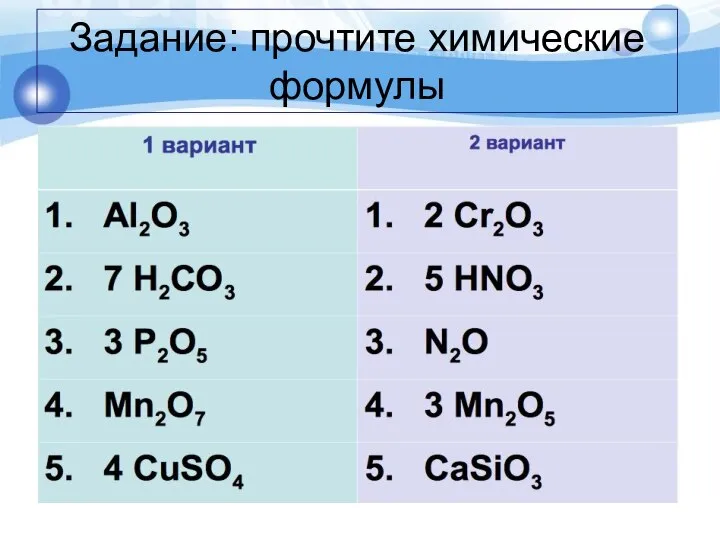
- 7. Задание: прочтите химические формулы
- 8. Относительная атомная масса Пользоваться такими малыми значениями неудобно, поэтому введено понятие об относительной атомной массе Аr
- 9. Относительная атомная масса Масса молекул и атомов очень мала, поэтому ими неудобно, да и невозможно пользоваться.
- 10. Аr - относительная атомная масс элемента А- атомная масс элемента Аr (О) =2,66*10-23 г./1,66*10-24г.=16 А(о)=16 а.е.м.
- 11. Относительная молекулярная масса - Мr Значения относительной молекулярной массы рассчитываются из значений относительной атомной массы с
- 12. Относительная молекулярная масса - Мr Установлено, что молекула N2 Mr (N2) = 2*14 = 28, молекула
- 13. Массовая доля элемента в веществе Определяется по формуле: ω(Э)= где ω(Э) – массовая доля элемента Э
- 14. Массовая доля элемента в сложном веществе Например, для воды H2O wH = 0,11 (11%) и wO
- 15. Закрепление: Назовите новые понятия, с которыми вы познакомились на уроке. Что означают записи: 3F2, F2, 10F
- 16. Домашнее задание
- 18. Скачать презентацию











 Растворы. Часть 2
Растворы. Часть 2 Буферные растворы
Буферные растворы Массовая доля элемента в веществе
Массовая доля элемента в веществе Чистые вещества и смеси. Использование химического анализа
Чистые вещества и смеси. Использование химического анализа Типы изомерии
Типы изомерии Диссоциация кислот
Диссоциация кислот Амфотерность. Амфотерные соединения
Амфотерность. Амфотерные соединения Получение галогенов. Биологическое значение и применение галогенов и их соединений
Получение галогенов. Биологическое значение и применение галогенов и их соединений Кислотные оксиды
Кислотные оксиды Презентация на тему "Азотная кислота"
Презентация на тему "Азотная кислота" Роль органической химии в производстве и повседневной жизни человека
Роль органической химии в производстве и повседневной жизни человека Фосфор. Аллотропия фосфора. Физические и химические свойства фосфора
Фосфор. Аллотропия фосфора. Физические и химические свойства фосфора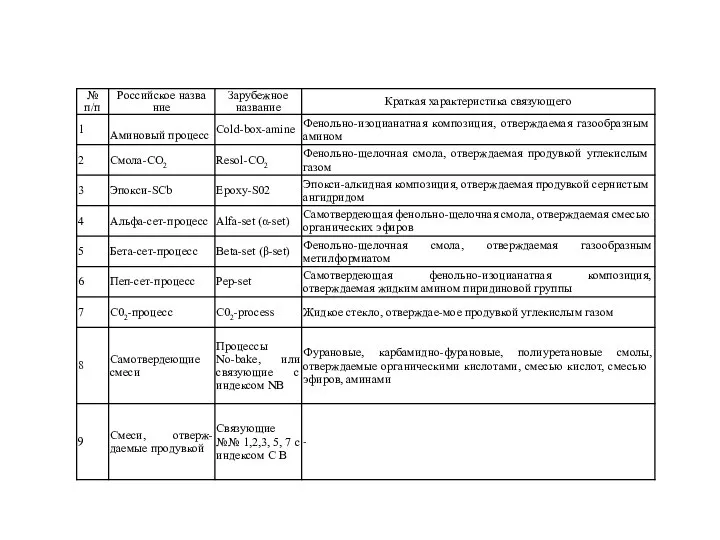 Фенольно-изоцианатная композиция
Фенольно-изоцианатная композиция Карбораны. Особенности строения молекулы. Получение и химические свойства
Карбораны. Особенности строения молекулы. Получение и химические свойства Природные источники углеводородов
Природные источники углеводородов Пространственное строение. Стереоизомерия. Структура и функции биолекул
Пространственное строение. Стереоизомерия. Структура и функции биолекул Простые вещества в стране Химляндии. 8 класс
Простые вещества в стране Химляндии. 8 класс Алканы
Алканы Белки
Белки Современные представления о механизме реакций отщепления. Спектр механизмов E1-E2-E1cB. Диаграммы Дженкса-О’Феррола
Современные представления о механизме реакций отщепления. Спектр механизмов E1-E2-E1cB. Диаграммы Дженкса-О’Феррола Дисперсные системы в пищевой промышленности
Дисперсные системы в пищевой промышленности Все свойства минералов
Все свойства минералов Транспорт веществ
Транспорт веществ Как осуществить цепочку превращений на основании положений теории электролитической диссоциации?
Как осуществить цепочку превращений на основании положений теории электролитической диссоциации? Проект в сфере экологического волонтерства преподавателя химии первой квалификационной категории
Проект в сфере экологического волонтерства преподавателя химии первой квалификационной категории Ионные уравнения реакций
Ионные уравнения реакций Магний(Mg)
Магний(Mg) Фенолы
Фенолы