Содержание
- 2. АЛКАНЫ Строение, номенклатура, изомерия и физические свойства.
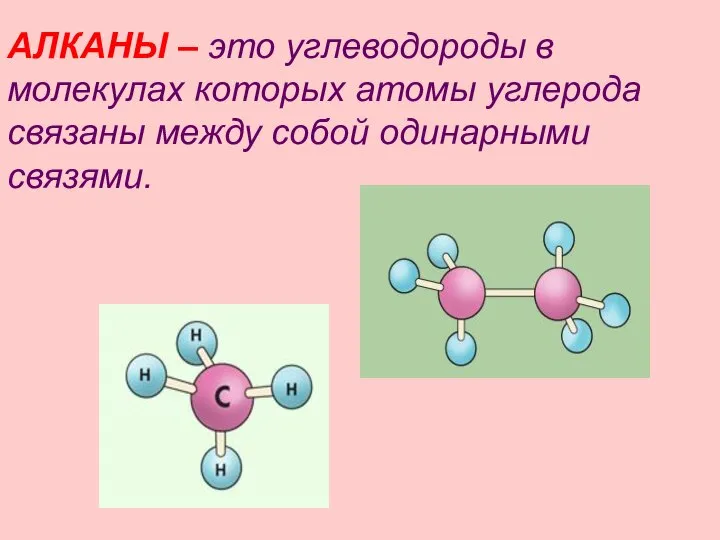
- 3. АЛКАНЫ – это углеводороды в молекулах которых атомы углерода связаны между собой одинарными связями.
- 4. Все алканы отвечают общей формуле СnН2n+2 где n=1, 2, 3…+∞
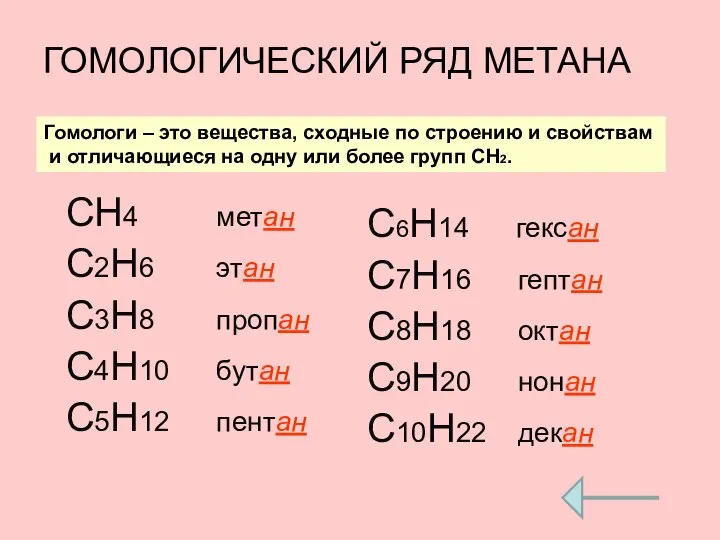
- 5. ГОМОЛОГИЧЕСКИЙ РЯД МЕТАНА СН4 метан С2H6 этан C3H8 пропан C4H10 бутан C5H12 пентан C6H14 гексан C7H16
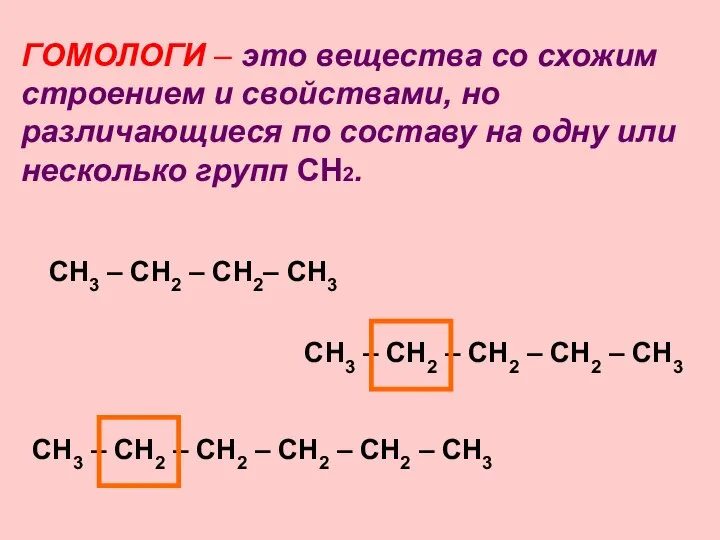
- 6. ГОМОЛОГИ – это вещества со схожим строением и свойствами, но различающиеся по составу на одну или
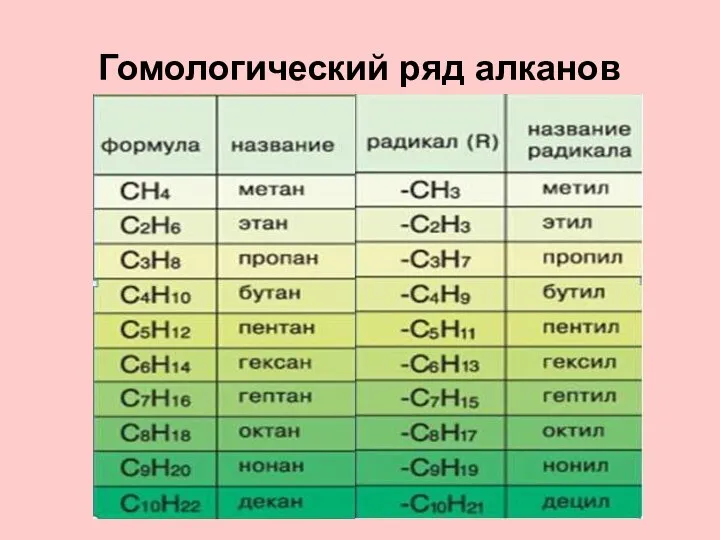
- 7. Гомологический ряд алканов
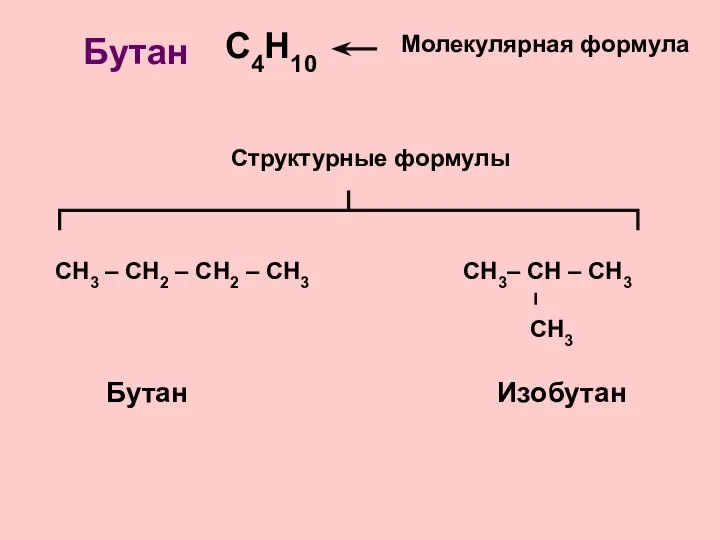
- 8. С4Н10 СН3 – СН2 – СН2 – СН3 Молекулярная формула Структурные формулы Бутан Бутан Изобутан
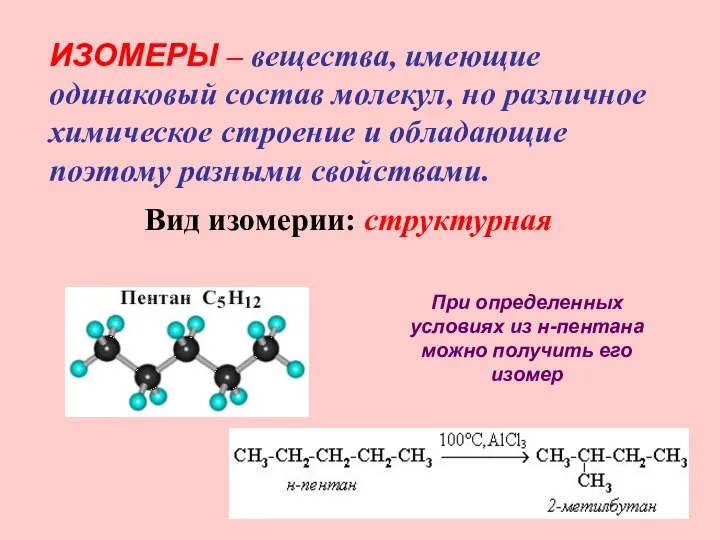
- 9. ИЗОМЕРЫ – вещества, имеющие одинаковый состав молекул, но различное химическое строение и обладающие поэтому разными свойствами.
- 10. НОМЕНКЛАТУРА АЛКАНОВ Алгоритм. Выбор главной цепи: CH3 – CH - CH2 - CH3 │ CH3
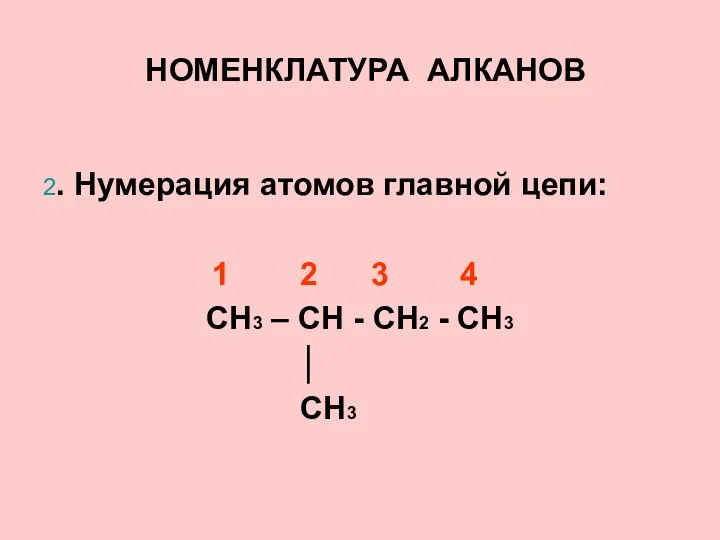
- 11. НОМЕНКЛАТУРА АЛКАНОВ 2. Нумерация атомов главной цепи: 1 2 3 4 CH3 – CH - CH2
- 12. НОМЕНКЛАТУРА АЛКАНОВ 3. Формирование названия: 1 2 3 4 CH3 – CH - CH2 - CH3
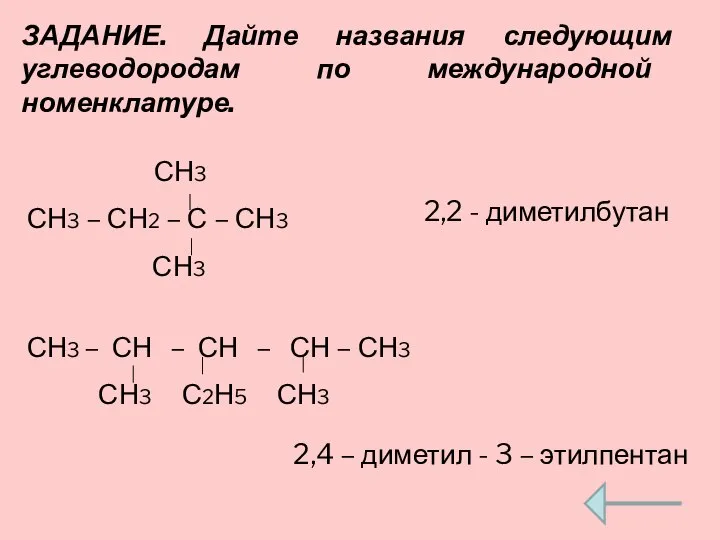
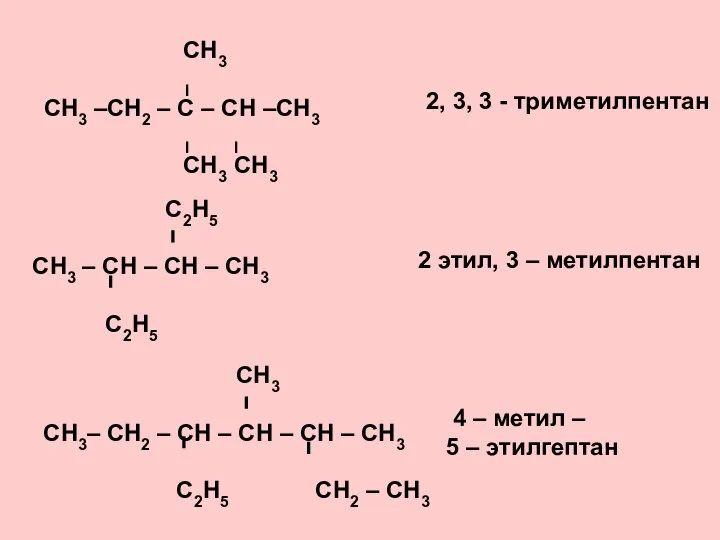
- 13. ЗАДАНИЕ. Дайте названия следующим углеводородам по международной номенклатуре. СН3 СН3 – СН2 – С – СН3
- 14. СН3 І СН3 –СН2 – С – СН –СН3 І І СН3 СН3 2, 3, 3
- 15. Составте структурные формулы следующих веществ и укажите первичные, вторичные и третичные атомы. А) 2,3 – диметилпентан
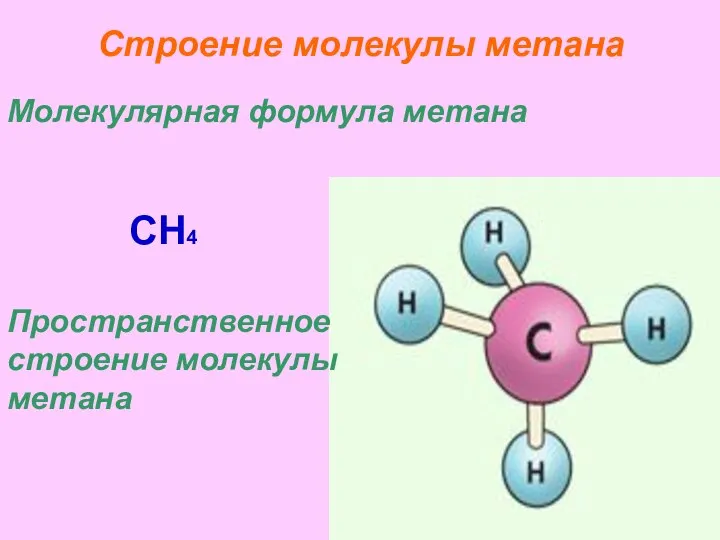
- 16. Строение молекулы метана Молекулярная формула метана CH4 Пространственное строение молекулы метана
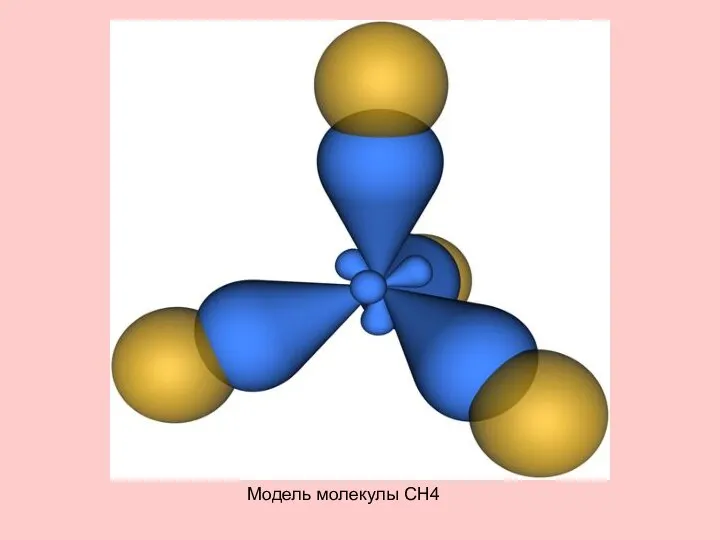
- 17. Модель молекулы CH4
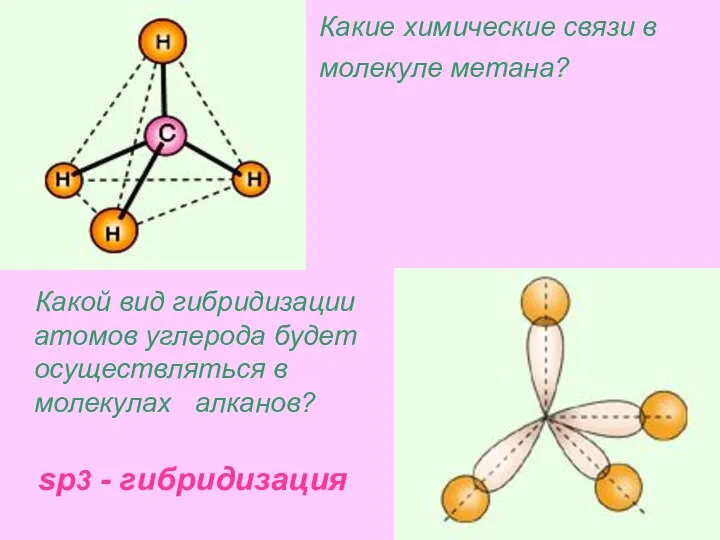
- 18. Какие химические связи в молекуле метана? Какой вид гибридизации атомов углерода будет осуществляться в молекулах алканов?
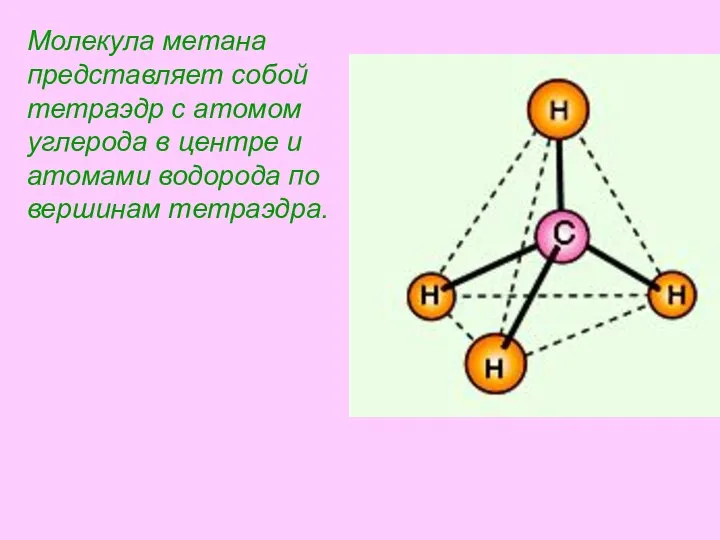
- 19. Молекула метана представляет собой тетраэдр с атомом углерода в центре и атомами водорода по вершинам тетраэдра.
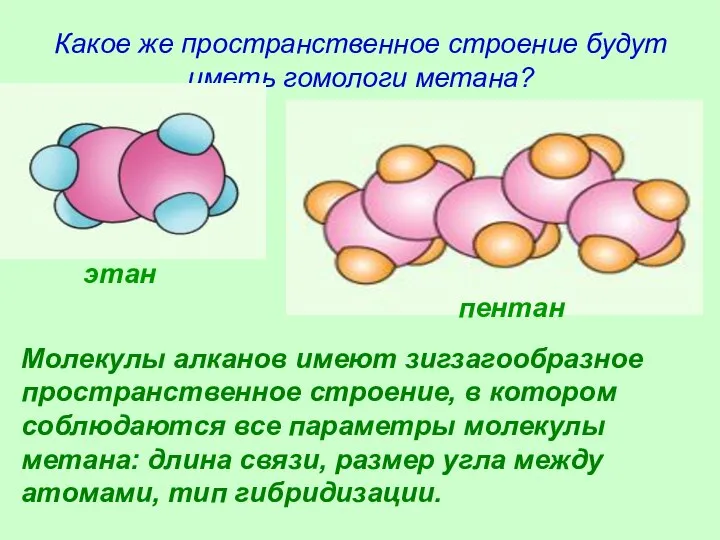
- 20. Какое же пространственное строение будут иметь гомологи метана? Молекулы алканов имеют зигзагообразное пространственное строение, в котором
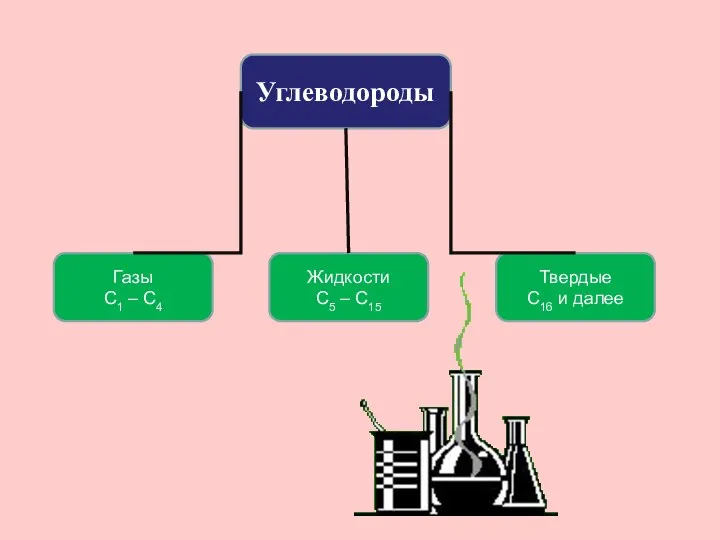
- 21. Углеводороды Жидкости С5 – С15 Газы С1 – С4 Твердые С16 и далее
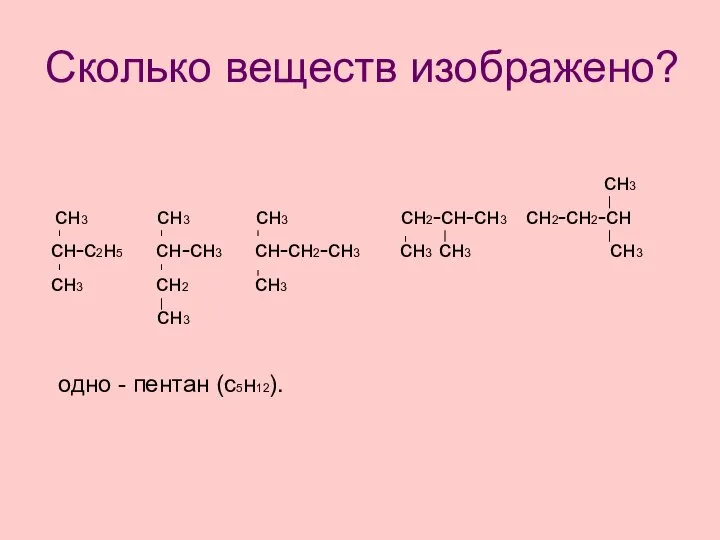
- 22. сн3 сн3 сн3 сн3 сн2-сн-сн3 сн2-сн2-сн сн-с2н5 сн-сн3 сн-сн2-сн3 сн3 сн3 сн3 сн3 сн2 сн3 сн3
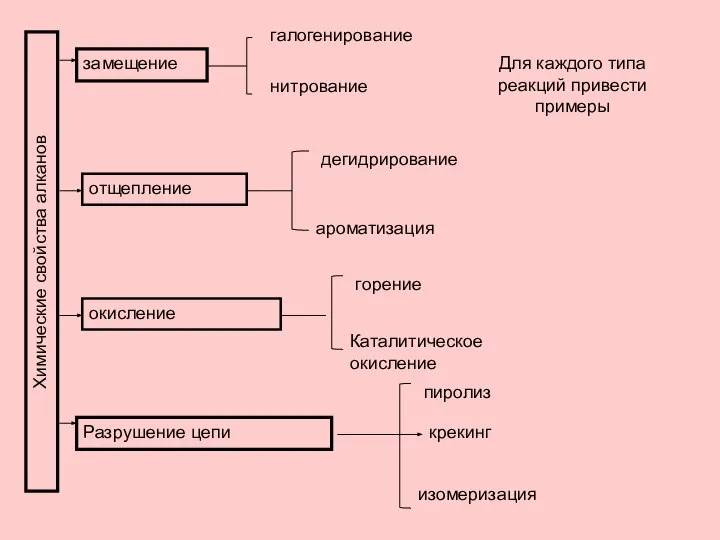
- 23. Химические свойства алканов замещение галогенирование нитрование Для каждого типа реакций привести примеры отщепление дегидрирование ароматизация окисление
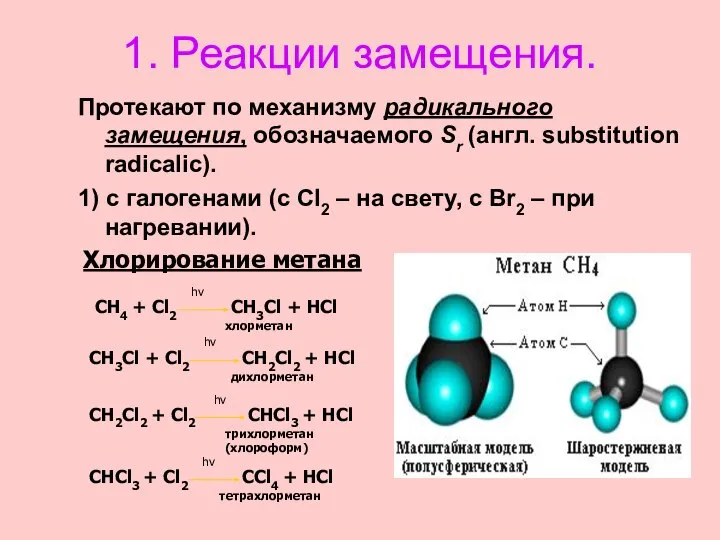
- 24. 1. Реакции замещения. Протекают по механизму радикального замещения, обозначаемого Sr (англ. substitution radicalic). 1) с галогенами
- 25. СН4 + Сl2 CH3Cl + HCl + Q t Реакции протекают по радикальному механизму. С Н
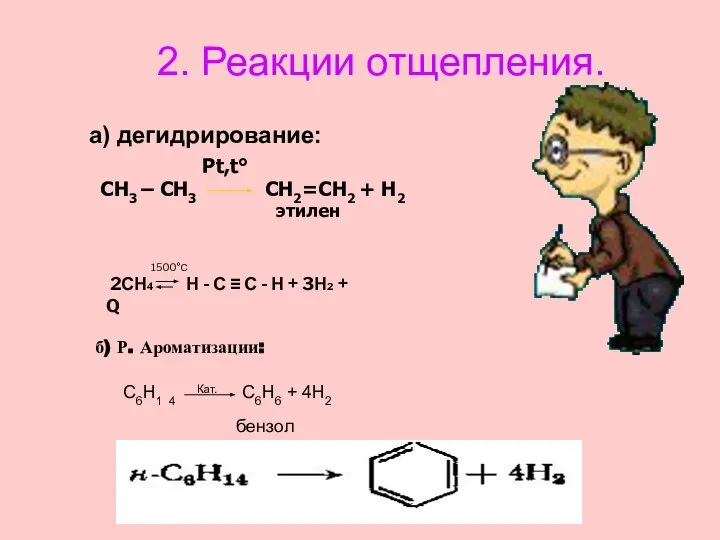
- 26. 2. Реакции отщепления. а) дегидрирование: CH3 – CH3 Pt,t° CH2=CH2 + H2 этилен 2СН4 Н -
- 27. 3. Реакции окисления. а) все алканы горят с образованием углекислого газа и воды : б) при
- 28. Горение алканов:
- 29. РЕАКЦИЯ ГОРЕНИЯ: CH4 + 2O2 → CO2 + 2H2O + Q
- 30. 4. Разрушение цепи. а) для метана характерен пиролиз: СН4 С+ 2Н2 10000
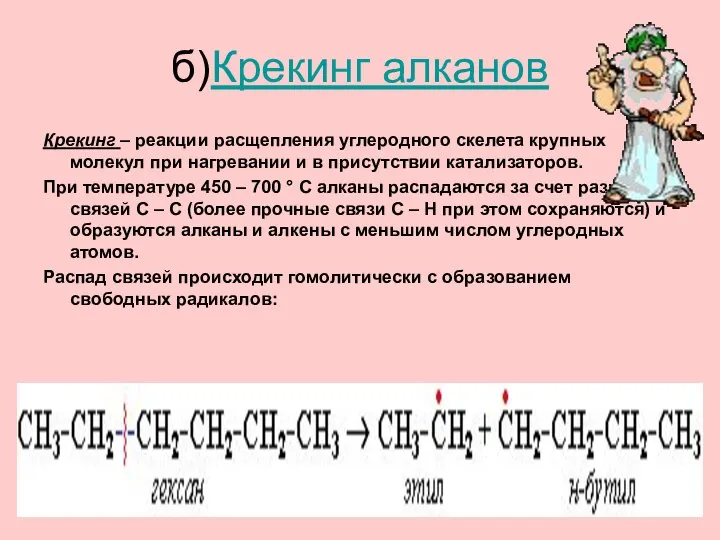
- 31. б)Крекинг алканов Крекинг – реакции расщепления углеродного скелета крупных молекул при нагревании и в присутствии катализаторов.
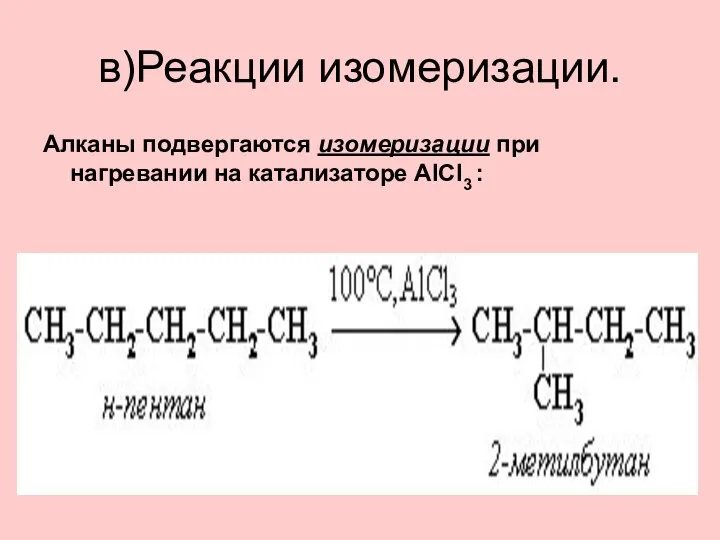
- 32. в)Реакции изомеризации. Алканы подвергаются изомеризации при нагревании на катализаторе AlCl3 :
- 33. МЕТАН – газ, без цвета и запаха, почти в 2 раза легче воздуха, мало растворим в
- 35. Скачать презентацию











 Презентация на тему Ковалентная связь: полярная и неполярная
Презентация на тему Ковалентная связь: полярная и неполярная  Производство нитрата аммония (лекция 16)
Производство нитрата аммония (лекция 16) Презентация на тему В мире индикаторов - исследовательская работа
Презентация на тему В мире индикаторов - исследовательская работа  Современные подходы к преподаванию химии
Современные подходы к преподаванию химии Алюминий. Строение и свойства атома
Алюминий. Строение и свойства атома Жизнь и деятельность Д.И.Менделеева «Если не будешь знать имен, то умрет и познание вещей» К.Линей. Автор: Ватитова А.А. МОУ Еласов
Жизнь и деятельность Д.И.Менделеева «Если не будешь знать имен, то умрет и познание вещей» К.Линей. Автор: Ватитова А.А. МОУ Еласов Природные источники углеводородов
Природные источники углеводородов Химия вокруг нас. 10 класс
Химия вокруг нас. 10 класс Амины. Аминокислоты
Амины. Аминокислоты Соли. Формула соли
Соли. Формула соли Вода. Классы неорганических соединений. 8 класс
Вода. Классы неорганических соединений. 8 класс Ковалентная полярная связь
Ковалентная полярная связь Коллоидные системы Классификация. Получение. Очистка. Свойства. Устойчивость и коагуляция. Применение
Коллоидные системы Классификация. Получение. Очистка. Свойства. Устойчивость и коагуляция. Применение Основные соединения кальция и их применение – вчера, сегодня, завтра.
Основные соединения кальция и их применение – вчера, сегодня, завтра. Вуглеводи. Визначення вуглеводів
Вуглеводи. Визначення вуглеводів Алотропия углерода
Алотропия углерода ÐÐÐÐ ÐÐТÐÐРХÐÐÐЧÐСÐÐÐ¥ Ð ÐÐÐЦÐÐ
ÐÐÐÐ ÐÐТÐÐРХÐÐÐЧÐСÐÐÐ¥ Ð ÐÐÐЦÐÐ Изменения, происходящие с веществами Урок химии 8 класс Учитель химии МОУ «СОШ №7» г. Балаково Саратовская обл.
Изменения, происходящие с веществами Урок химии 8 класс Учитель химии МОУ «СОШ №7» г. Балаково Саратовская обл. Химический процесс: энергетика и равновесие
Химический процесс: энергетика и равновесие Презентация на тему Химическое равновесие
Презентация на тему Химическое равновесие  Атом. Стремление к завершению электронного уровня
Атом. Стремление к завершению электронного уровня Кислоты. Классификация кислот
Кислоты. Классификация кислот Коррозия металлов
Коррозия металлов Теория активированного комплекса
Теория активированного комплекса Л-1-5
Л-1-5 Презентация на тему Фенол и его свойства
Презентация на тему Фенол и его свойства  Процессы растворения твёрдых веществ
Процессы растворения твёрдых веществ Степень окисления. Бинарные соединения
Степень окисления. Бинарные соединения